Składniki aktywne: Interferon beta-1a
AVONEX 30 mikrogramów/0,5 ml roztwór do wstrzykiwań
Ulotki informacyjne Avonex są dostępne dla wielkości opakowań:- AVONEX 30 mikrogramów/0,5 ml roztwór do wstrzykiwań
- AVONEX 30 mikrogramów/0,5 ml roztwór do wstrzykiwań we wstrzykiwaczu
Dlaczego stosuje się Avonex? Po co to jest?
Co to jest AVONEX
Substancją czynną leku Avonex jest białko zwane interferonem beta-1a. Interferony to naturalne substancje, które organizm wytwarza w celu ochrony przed infekcjami i chorobami.Białko zawarte w Avonex ma dokładnie taki sam skład jak interferon beta wytwarzany przez organizm ludzki.
Co to jest AVONEX
Preparat Avonex stosuje się w leczeniu stwardnienia rozsianego (MS). Leczenie preparatem Avonex może pomóc uniknąć pogorszenia, nawet jeśli nie wyleczy SM.
Każdy ma indywidualną różnorodność objawów SM. Możliwe objawy to:
- Zawroty głowy lub brak równowagi, problemy z chodzeniem, sztywność i skurcze mięśni, zmęczenie, drętwienie twarzy, rąk lub nóg
- Ostry lub przewlekły ból, zaburzenia pęcherza lub jelit, problemy seksualne i zaburzenia widzenia
- Trudności z myśleniem i koncentracją, depresja.
Stwardnienie rozsiane również ma tendencję do zaostrzania się od czasu do czasu: zjawisko to nazywa się nawrotem (nawrotem).
(Dodatkowe informacje)
Avonex działa najlepiej, gdy jest przyjmowany regularnie, raz w tygodniu, o tej samej porze. Nie należy przerywać przyjmowania leku Avonex bez wcześniejszej rozmowy z neurologiem.
Avonex może pomóc w zmniejszeniu liczby nawrotów (rzutów) i spowolnić postęp choroby powodującej niepełnosprawność. Lekarz poinformuje pacjenta, jak długo należy przyjmować lek Avonex lub kiedy nadejdzie czas na jego odstawienie.
Jak działa AVONEX
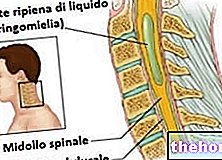
Stwardnienie rozsiane wiąże się z uszkodzeniem nerwów (mózgu lub rdzenia kręgowego). W SM układ odpornościowy reaguje atakując mielinę – „izolacyjną” powłokę otaczającą włókna nerwowe. Uszkodzenie mieliny utrudnia wymianę wiadomości między mózgiem a innymi częściami ciała. To właśnie powoduje objawy SM. Wydaje się, że działanie leku Avonex polega na powstrzymywaniu układu odpornościowego organizmu przed atakowaniem mieliny.
Przeciwwskazania Kiedy nie należy stosować preparatu Avonex
Nie stosować AVONEX:
- Jeśli pacjent ma uczulenie na interferon beta lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6)
- Jeśli jesteś w ciąży, nie rozpoczynaj stosowania leku Avonex
- Jeśli masz ciężką depresję lub myślisz o samobójstwie.
Należy natychmiast poinformować lekarza, jeśli wystąpi którakolwiek z tych okoliczności.
(Dodatkowe informacje)
Avonex i reakcje alergiczne. Ponieważ Avonex zawiera białko, istnieje małe prawdopodobieństwo wystąpienia reakcji alergicznej.
Więcej o depresji. Jeśli u pacjenta występuje ciężka depresja lub myśli samobójcze, nie należy stosować leku Avonex. Jeśli pacjent ma depresję, lekarz może przepisać lek Avonex, ale ważne jest, aby poinformować lekarza, jeśli cierpiał na depresję lub inne podobne zaburzenia nastroju.
Środki ostrożności dotyczące stosowania Informacje ważne przed przyjęciem leku Avonex
Ostrzeżenia i środki
Przed rozpoczęciem stosowania leku Avonex należy porozmawiać z lekarzem, jeśli u pacjenta występują lub występowały w przeszłości następujące problemy:
- Depresja lub problemy z nastrojem
- Myśli samobójcze.
Wszelkie wahania nastroju, myśli samobójcze, niezwykłe uczucia smutku, lęku lub osłabienia należy natychmiast zgłaszać lekarzowi.
- Padaczka lub inne podobne zaburzenia niekontrolowane przez leki
- Ciężkie problemy z nerkami lub wątrobą
- Mała ilość białych krwinek lub płytek krwi, co może zwiększać ryzyko infekcji, krwawienia lub anemii
- Problemy z sercem, które mogą powodować objawy, takie jak ból w klatce piersiowej (dławica piersiowa), zwłaszcza po aktywności fizycznej, obrzęk kostek, duszność (zastoinowa niewydolność serca) lub nieregularne bicie serca (arytmie).
Porozmawiaj z lekarzem, jeśli u pacjenta wystąpi którykolwiek z tych stanów lub jeśli stan się pogorszy podczas stosowania leku Avonex.
Podczas leczenia mogą tworzyć się zakrzepy (skrzepy krwi) wewnątrz małych naczyń krwionośnych. Zakrzepy te mogą mieć wpływ na nerki. Tworzenie zakrzepów może wystąpić kilka tygodni do kilku lat po rozpoczęciu leczenia lekiem Avonex.
Lekarz może zdecydować o zbadaniu ciśnienia krwi, krwi (liczby płytek krwi) i czynności nerek. Należy poinformować lekarza o przyjmowaniu leku Avonex:
- Jeśli musisz wykonać badanie krwi, ponieważ Avonex może zmienić wyniki.
(Dodatkowe informacje)
W niektórych przypadkach konieczne będzie poinformowanie lekarza o stosowaniu leku Avonex. Na przykład, jeśli pacjentowi przepisano inne leki lub konieczne jest wykonanie badania krwi, Avonex może zmienić działanie leków lub wyniki badań.
Interakcje Jakie leki lub pokarmy mogą zmienić działanie leku Avonex
Należy poinformować lekarza o przyjmowaniu jakichkolwiek innych leków, zwłaszcza leków stosowanych w leczeniu padaczki i depresji.Avonex może wpływać na inne leki lub być pod ich wpływem. Dotyczy to każdego leku, także bez recepty.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
Ciąża i karmienie piersią
Jeśli jesteś w ciąży, nie rozpoczynaj stosowania leku Avonex.
- jeśli pacjentka jest w wieku rozrodczym i jest aktywna seksualnie, musi stosować odpowiednią antykoncepcję podczas przyjmowania leku Avonex.
- jeśli pacjentka planuje zajść w ciążę lub zajść w ciążę podczas stosowania leku Avonex, powinna porozmawiać z lekarzem, czy kontynuować leczenie.
- jeśli pacjentka jest już w ciąży lub podejrzewa, że jest w ciąży, należy jak najszybciej skontaktować się z lekarzem.
- jeśli zamierzasz karmić piersią, najpierw porozmawiaj z lekarzem.
Prowadzenie i używanie maszyn
Jeśli czujesz zawroty głowy, nie jedź. U niektórych osób Avonex wywołuje efekt zawrotów głowy. Jeśli tak się stanie lub jeśli wystąpią inne działania niepożądane, które mogą mieć wpływ na twoje zdolności, nie powinieneś prowadzić pojazdów ani obsługiwać maszyn.
Ważne informacje o niektórych składnikach AVONEX
Ten lek jest zasadniczo „wolny od sodu”. Zawiera mniej niż 23 mg (1 mmol) sodu na dawkę tygodniową.
Dawka, sposób i czas podawania Jak stosować Avonex: Dawkowanie
Zalecana dawka dla dorosłych i młodzieży w wieku 12 lat i starszych.
Jedno wstrzyknięcie leku Avonex na tydzień.
Staraj się przyjmować Avonex co tydzień, zawsze tego samego dnia i o tej samej porze.
Nie dla dzieci
Preparatu Avonex nie należy stosować u dzieci w wieku poniżej 12 lat.
W przypadku podjęcia decyzji o rozpoczęciu leczenia lekiem Avonex, lekarz może dostarczyć zestaw do dostosowywania dawki Avostartclip. Avostartclip zatrzaskuje się na strzykawce i umożliwia stopniowe zwiększanie dawki leku Avonex na początku leczenia. Ogranicza to objawy grypopodobne, których doświadczają niektórzy ludzie, gdy zaczynają stosować Avonex. Lekarz lub pielęgniarka nauczy Cię, jak korzystać z zestawu do miareczkowania Avostartclip.
(Dodatkowe informacje)
Rozpoczęcie terapii Avonex
Jeśli pacjent nigdy wcześniej nie przyjmował leku Avonex, lekarz może zalecić stopniowe zwiększanie dawki, aby przyzwyczaić się do działania leku Avonex przed przyjęciem pełnej dawki. Prawdopodobnie otrzymasz zestaw do dostosowywania dawki Avostartclip, który jest zamontowany na strzykawce, umożliwiając podanie zmniejszonej dawki leku Avonex na początku leczenia.Każdy zestaw Avostartclip jest przeznaczony wyłącznie do jednorazowego użytku i należy go następnie wyrzucić wraz z pozostałym preparatem Avonex. Aby uzyskać więcej informacji na temat korzystania z tego urządzenia, zapytaj swojego lekarza.
Wykonaj wstrzyknięcie samodzielnie
Jeśli poinformowano pacjenta, jak to zrobić, można wstrzykiwać lek Avonex bez pomocy lekarza.Instrukcje wstrzykiwania znajdują się na końcu tej ulotki (patrz punkt 7, Jak wstrzykiwać lek AVONEX).
W przypadku problemów z posługiwaniem się strzykawką należy skontaktować się z lekarzem, który może udzielić pomocy.
(Dodatkowe informacje)
Na dole ulotki dołączonej do opakowania znajduje się więcej informacji na temat wstrzykiwania leku Avonex.
Alternatywna igła:
Igła do wstrzykiwań jest już dołączona do opakowania Avonex. Twój lekarz może przepisać krótszą, cieńszą igłę w zależności od twoich cech fizycznych. Jeśli uważasz, że tak jest, porozmawiaj ze swoim lekarzem.
Jeśli masz problemy z posługiwaniem się strzykawką, porozmawiaj z lekarzem o użyciu odpowiedniego narzędzia. To narzędzie składa się z uchwytu zaprojektowanego specjalnie w celu ułatwienia wstrzykiwania leku Avonex. Jak długo stosować lek AVONEX O tym, jak długo należy stosować lek Avonex, zdecyduje lekarz. Ważne jest, aby kontynuować stosowanie leku Avonex. za radą lekarza.
Jak wstrzykiwać AVONEX
Musiałeś już zostać poinstruowany, jak wstrzykiwać Avonex. Te wskazówki to tylko przypomnienie. W przypadku dalszych pytań należy zwrócić się do lekarza lub farmaceuty.
Wybór miejsca wstrzyknięcia
- Avonex jest wstrzykiwany do mięśnia, takiego jak jeden z mięśni górnej części ud. Nie zaleca się wstrzykiwania leku Avonex w pośladki.
- Każdego tygodnia wybieraj inne miejsce wstrzyknięcia. Zmniejsza to ryzyko podrażnienia skóry lub mięśni.
- Nie wybieraj obszarów skóry ze stłuczeniami, zmianami lub infekcjami i nie wstrzykuj w otwartą ranę.
Przygotowanie
- Wyjmij zapieczętowaną tackę z lodówki - Sprawdź datę ważności na wieczku tacki. Nie używaj produktu, jeśli wygasł. - Całkowicie zdejmij pokrywę papieru. Sprawdzić, czy tacka zawiera ampułko-strzykawkę i igłę iniekcyjną (patrz rysunek „Zawartość plastikowej tacki”).
- Pozostawić strzykawkę do ogrzania - Pozostawić strzykawkę w temperaturze pokojowej na pół godziny, dzięki czemu wstrzyknięcie będzie wygodniejsze niż wstrzykiwanie bezpośrednio po wyjęciu z lodówki. Uwaga: Do podgrzewania strzykawki nie należy używać zewnętrznych źródeł ciepła, takich jak gorąca woda.
- Dokładnie umyć ręce wodą z mydłem i wysuszyć.
- Przygotuj chusteczki i plastry nasączone alkoholem (brak w zestawie), jeśli ich potrzebujesz. Poszukaj czystej, twardej powierzchni do ułożenia materiału potrzebnego do iniekcji i połóż na niej tackę.
Przygotowanie zastrzyku
- Sprawdzić płyn w strzykawce, powinien być przejrzysty i bezbarwny. Jeśli roztwór jest mętny lub zabarwiony, lub jeśli widoczne są zawieszone cząstki, nie należy używać ampułko-strzykawki.
- Zdjąć nasadkę strzykawki Strzykawka ma białą nasadkę zabezpieczającą przed manipulacją. Upewnij się, że nasadka jest nienaruszona i nie została otwarta. Jeśli wygląda na to, że nasadka została otwarta, nie należy używać strzykawki. Trzymać strzykawkę białą nasadką skierowaną do góry. Zgiąć nasadkę pod kątem prostym, aż wyskoczy. Nie dotykać stawu. Nie naciskać tłoka.
- Zakładanie igły Otworzyć igłę, aby odsłonić staw. Zachowaj opakowanie ochronne na igle. Nałożyć igłę na strzykawkę Obracać ją zgodnie z ruchem wskazówek zegara aż do zatrzaśnięcia Uwaga: Upewnić się, że igła jest całkowicie włożona do strzykawki, w przeciwnym razie może przeciekać. Jeśli zalecono stopniowe zwiększanie dawki leku Avonex, może być potrzebny zestaw do dostosowywania dawki Avostartclip dostarczony przez lekarza. Aby uzyskać więcej informacji, zapytaj swojego lekarza. Teraz zdejmij opakowanie ochronne z igły. Nie obracaj go. Uwaga: Jeśli obrócisz opakowanie ochronne podczas jego zdejmowania, możesz również przypadkowo usunąć igłę.
Wykonywanie zastrzyku
- Oczyścić i rozciągnąć miejsce wstrzyknięcia. W razie potrzeby przemyć skórę w miejscu wstrzyknięcia gazikiem nasączonym alkoholem Poczekać, aż skóra wyschnie Jedną ręką naciągnąć skórę wokół miejsca wstrzyknięcia. Rozluźnij mięśnie.
- Wykonać wstrzyknięcie. Wbić igłę w mięsień szybkim ruchem prostopadle do skóry. Igła powinna wbić się do końca. Powoli wciskać tłok, aż strzykawka się opróżni.Jeśli używasz strzykawki z Avostartclip, otrzymasz mniejszą dawkę leku Avonex.Strzykawka nie będzie się opróżniać.
- Wyciągnąć igłę Usunąć igłę do wstrzykiwań trzymając skórę mocno naciągniętą lub ściśniętą wokół miejsca wstrzyknięcia W przypadku używania wacików bawełnianych nasączonych alkoholem umieścić jeden na miejscu wstrzyknięcia W razie potrzeby przykleić plaster w miejscu wstrzyknięcia. .
Prawidłowo zutylizuj zużyty materiał
Po wykonaniu wstrzyknięcia umieścić igłę i strzykawkę w odpowiednim pojemniku (pojemniku na ostre przedmioty), a nie na odpadkach domowych. W przypadku zastosowania leku Avostartclip należy wyrzucić strzykawkę (i Avostartclip) po wstrzyknięciu.Niewykorzystanej części leku Avonex nie należy używać ponownie.Papier i waciki można wyrzucić do zwykłego kosza na śmieci.
Przedawkowanie Co zrobić, jeśli pacjent przyjął zbyt dużą dawkę leku Avonex
Jeśli wstrzykniesz za dużo
Potrzebujesz tylko jednego zastrzyku Avonex na tydzień. W przypadku przyjęcia więcej niż jednego wstrzyknięcia leku Avonex w ciągu trzech dni, należy natychmiast zwrócić się o poradę do lekarza lub farmaceuty.
Jeśli zapomnisz o zastrzyku
W przypadku pominięcia zwykłej cotygodniowej dawki należy jak najszybciej wstrzyknąć dawkę. Następnie należy odczekać tydzień przed kolejnym wstrzyknięciem leku Avonex. Kontynuuj zastrzyki w ten nowy dzień co tydzień. Jeśli jest określony dzień tygodnia, w którym wolisz wstrzykiwać, poproś lekarza o instrukcje, jak przywrócić wstrzyknięcie do preferowanego dnia.
Nie należy wstrzykiwać podwójnej dawki w celu uzupełnienia pominiętej dawki.
Skutki uboczne Jakie są skutki uboczne leku Avonex
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
(Dodatkowe informacje)
Chociaż lista możliwych skutków ubocznych wydaje się niepokojąca, możesz nie doświadczyć żadnego z nich.
Poważne skutki uboczne: zasięgnij porady lekarskiej
Ciężkie reakcje alergiczne
Jeśli tak się stanie:
- Obrzęk twarzy, ust lub języka
- Trudności w oddychaniu
- Zaczerwienienie
natychmiast skontaktować się z lekarzem. Nie należy kontynuować stosowania leku Avonex bez powiadomienia lekarza.
Depresja
Jeśli wystąpią objawy depresji:
- Niezwykłe uczucie smutku, niepokoju lub poczucie bezwartościowości
natychmiast skontaktować się z lekarzem.
Problemy z wątrobą
Jeśli tak się stanie:
- Zażółcenie skóry lub białek oczu (żółtaczka)
- Powszechne swędzenie
- Nudności i wymioty
- Łatwość powstawania siniaków należy natychmiast skontaktować się z lekarzem, ponieważ mogą to być objawy problemów z wątrobą.
Działania niepożądane stwierdzone w badaniach klinicznych
(Dodatkowe informacje)
Działania niepożądane stwierdzone w badaniach klinicznych. Są to działania niepożądane zgłoszone w czasie badania preparatu Avonex. Przedstawione liczby są oparte na liczbie osób, które zgłosiły ten efekt i służą do zorientowania się, jak prawdopodobne jest, że dany efekt uboczny może dotyczyć również Ciebie.
Bardzo częste działania niepożądane (u co najmniej 1 na 10 osób)
- objawy grypopodobne - ból głowy, bóle ciała, dreszcze lub gorączka: patrz poniżej Objawy grypopodobne
- bół głowy.
Częste działania niepożądane (dotyczą mniej niż 1 na 10 osób)
- Utrata apetytu
- Uczucie słabości i zmęczenia
- Trudności ze snem
- Depresja
- Zaczerwienienie
- Katar
- Biegunka
- Nudności lub wymioty
- drętwienie lub mrowienie skóry
- Rumień lub siniaki
- Zwiększona potliwość, nocne poty
- Ból mięśni lub stawów, ból ramion, nóg lub szyi
- Skurcze mięśni, sztywność mięśni lub stawów
- Ból, zasinienie i zaczerwienienie w miejscu wstrzyknięcia
- Zmiany w wynikach badań krwi. Objawy, które możesz zauważyć, to zmęczenie, powtarzające się infekcje, siniaki lub niewyjaśnione krwawienie.
Niezbyt częste działania niepożądane (dotyczą mniej niż 1 na 100 osób)
- Wypadanie włosów
- Zmiany w cyklu menstruacyjnym
- Uczucie pieczenia w miejscu wstrzyknięcia.
Rzadkie działania niepożądane (dotyczą mniej niż 1 na 1000 osób)
- Trudności w oddychaniu.
- Problemy z nerkami, w tym blizny, które mogą osłabiać czynność nerek. Jeśli wystąpi którykolwiek lub wszystkie z poniższych objawów: Pienisty mocz Zmęczenie Obrzęk, szczególnie kostek i powiek oraz przyrost masy ciała. Należy poinformować lekarza, ponieważ mogą to być objawy możliwej choroby nerek.
- Zakrzep (skrzepy krwi) w małych naczyniach krwionośnych, które mogą wpływać na nerki (zakrzepowa plamica małopłytkowa lub zespół hemolityczno-mocznicowy).Objawy mogą obejmować nasilone siniaki, krwawienia, gorączkę, skrajne osłabienie, bóle głowy, zawroty głowy lub oszołomienie. zmiany we krwi i czynności nerek W przypadku wystąpienia któregokolwiek z tych działań niepożądanych należy zwrócić się do lekarza.
Inne skutki uboczne
(Dodatkowe informacje)
Efekty te zaobserwowano u osób stosujących preparat Avonex, ale nie wiadomo, jakie jest prawdopodobieństwo ich wystąpienia.
- Niedoczynność lub nadczynność tarczycy
- Nerwowość lub niepokój, niestabilność emocjonalna, irracjonalne myśli lub halucynacje (urojone wizje lub dźwięki), splątanie, myśli samobójcze
- Drętwienie, zawroty głowy, drgawki i migreny
- Świadomość bicia serca (kołatanie serca), przyspieszona lub nieregularna częstość akcji serca, problemy z sercem z następującymi objawami: zmniejszona zdolność do ćwiczeń, niemożność leżenia w łóżku, duszność lub obrzęk kostek
- Problemy z wątrobą, opisane powyżej
- Pokrzywka lub wysypka pęcherzykowa, swędzenie lub zaostrzenie łuszczycy, jeśli je masz
- Obrzęk lub krwawienie w miejscu wstrzyknięcia lub ból w klatce piersiowej po wstrzyknięciu
- Przyrost lub utrata masy ciała
- Zmiany w wynikach badań laboratoryjnych, w tym testów czynności wątroby.
Jeśli którykolwiek z tych objawów niepokoi Cię, porozmawiaj z lekarzem.
Niepożądane skutki wstrzyknięcia
- Uczucie omdlenia: Pierwsze wstrzyknięcie leku Avonex może podać lekarz, ponieważ może to spowodować omdlenie lub wręcz zemdlenie. Jest mało prawdopodobne, aby zdarzyło się to więcej niż raz.
- Bezpośrednio po wstrzyknięciu może wystąpić nadmierne napięcie mięśniowe lub osłabienie mięśni – efekt przypominający nawrót SM. Jest to rzadkie, występuje tylko w momencie wstrzyknięcia i mija wkrótce po. Jednak to działanie niepożądane może wystąpić w dowolnym momencie po rozpoczęciu leczenia preparatem Avonex.
- W przypadku zauważenia jakichkolwiek podrażnień lub problemów skórnych po wstrzyknięciu należy skontaktować się z lekarzem.
Objawy grypopodobne
(Dodatkowe informacje)
Trzy proste sposoby na zmniejszenie nasilenia objawów grypopodobnych:
- Avonex należy wstrzykiwać tuż przed snem, aby w przypadku wystąpienia efektów ubocznych zasnąć.
- Weź acetaminofen lub ibuprofen na pół godziny przed wstrzyknięciem Avonex i kontynuuj przyjmowanie ich przez jeszcze jeden dzień. Uzyskaj poradę dotyczącą odpowiedniej dawki od swojego lekarza lub farmaceuty.
- Jeśli masz gorączkę, pij dużo wody, aby utrzymać nawodnienie organizmu.
Po wstrzyknięciu dawki leku Avonex niektóre osoby mają wrażenie grypy.Objawy to:
- Bół głowy
- Bóle mięśni
- Dreszcze lub gorączka.
Objawy te nie wynikają z prawdziwej grypy.
Z tego powodu nie powinien bać się zarażania innych ludzi. Objawy tego typu są częstsze na początku leczenia lekiem Avonex.Twój lekarz może dostarczyć zestaw do dostosowywania dawki Avostartclip, który umożliwia stopniowe zwiększanie dawki na początku leczenia, co pomaga ograniczyć objawy grypopodobne. W miarę kontynuowania zastrzyków objawy grypopodobne stopniowo ustępują.
Zgłaszanie skutków ubocznych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe działania niepożądane niewymienione w tej ulotce, należy porozmawiać z lekarzem lub farmaceutą. Działania niepożądane można również zgłaszać bezpośrednio za pośrednictwem krajowego systemu zgłaszania wymienionego w załączniku V. Zgłaszanie działań niepożądanych może pomóc w uzyskaniu większej ilości informacji na temat bezpieczeństwa tego leku.
Wygaśnięcie i przechowywanie
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na etykiecie.Termin ważności oznacza ostatni dzień podanego miesiąca. C.
Przechowywać w oryginalnym opakowaniu (zamkniętej plastikowej tacce), aby chronić lek przed światłem. Przechowywać w lodówce (między 2°C a 8°C). Nie zamrażać.
Avonex można również przechowywać w temperaturze pokojowej (od 15°C do 30°C) nie dłużej niż tydzień.
NIE WOLNO stosować leku Avonex, jeśli zauważysz, że:
- ampułko-strzykawka jest uszkodzona.
- zamknięta plastikowa taca jest uszkodzona lub otwarta.
- roztwór nie jest bezbarwny lub widoczne są zawieszone cząstki.
- nasadka zabezpieczająca przed manipulacją została zerwana.
Nie należy wyrzucać żadnych leków do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa.Pomoże to chronić środowisko.
Skład i postać farmaceutyczna
Co AVONEX
Substancją czynną jest: interferon beta-1a, 30 mikrogramów/0,5 ml
Pozostałe składniki to: sodu octan trójwodny, lodowaty kwas octowy, chlorowodorek argininy, polisorbat 20 i woda do wstrzykiwań.
Jak wygląda lek AVONEX i co zawiera opakowanie
Avonex Solution for Injection składa się z gotowych do użycia zastrzyków.
Opakowanie leku Avonex zawiera cztery lub dwanaście gotowych do użycia (napełnionych) strzykawek, z których każda zawiera 0,5 ml przezroczystego, bezbarwnego płynu.Nie wszystkie wielkości opakowań mogą być dostępne w obrocie.Każda strzykawka jest zapakowana na tacce z zapieczętowanego plastiku. Do każdego opakowania dołączona jest również igła iniekcyjna.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO
AVONEX 30 MCG / 0,5 ML ROZTWÓR DO WSTRZYKIWAŃ
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY
Każda ampułko-strzykawka o pojemności 0,5 ml zawiera 30 mikrogramów (6 milionów jm) interferonu beta-1a.
Stężenie wynosi 30 mcg na 0,5 ml.
Stosując Międzynarodowy Standard Światowej Organizacji Zdrowia (WHO) dla interferonu, 30 mcg AVONEX zawiera 6 milionów IU aktywności przeciwwirusowej. Działalność związana z innymi normami nie jest znana.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
03.0 POSTAĆ FARMACEUTYCZNA
Roztwór do wstrzykiwań.
Przejrzysty i bezbarwny roztwór.
04.0 INFORMACJE KLINICZNE
04.1 Wskazania terapeutyczne
AVONEX jest wskazany w leczeniu:
• Pacjenci zdiagnozowani z nawracającym stwardnieniem rozsianym (MS). W badaniach klinicznych charakteryzowało się to dwoma lub więcej ostrymi zaostrzeniami (nawrotami) w ciągu ostatnich trzech lat bez dowodów na ciągłą progresję między nawrotami; AVONEX spowalnia postęp niepełnosprawności i zmniejsza częstotliwość nawrotów.
• Pacjenci z pojedynczym epizodem demielinizacyjnym z aktywnym procesem zapalnym, jeśli zdarzenie to jest na tyle poważne, że wymaga leczenia dożylnymi kortykosteroidami, wykluczono inne rozpoznania i jeśli ustalono, że pacjenci są obarczeni wysokim ryzykiem rozwoju klinicznie zdefiniowanego stwardnienia rozsianego (patrz punkt 5.1).
AVONEX należy przerwać u pacjentów, u których rozwinie się postępujące stwardnienie rozsiane.
04.2 Dawkowanie i sposób podawania
Leczenie należy rozpocząć pod nadzorem lekarza doświadczonego w leczeniu choroby.
Dawkowanie
Dorośli ludzie: zalecana dawka w leczeniu nawracających postaci stwardnienia rozsianego wynosi 30 mikrogramów (0,5 ml roztworu), podawana we wstrzyknięciu domięśniowym (im) raz w tygodniu (patrz punkt 6.6). Nie wykazano dodatkowych korzyści przy podawaniu większej dawki (60 mcg) raz w tygodniu.
Miareczkowanie: Aby pomóc pacjentom w zmniejszeniu częstości występowania i nasilenia objawów grypopodobnych (patrz punkt 4.8), na początku leczenia można przeprowadzić dostosowywanie dawki.
Dostosowanie dawki można osiągnąć za pomocą BIOSET lub ampułko-strzykawki, rozpoczynając leczenie w przyrostach o 1/4 tygodniowych dawek, aż do osiągnięcia pełnej dawki (30 mikrogramów na tydzień) do 4. tygodnia.
Alternatywny schemat zwiększania dawki można uzyskać, rozpoczynając terapię około ½ dawki preparatu AVONEX raz w tygodniu przed osiągnięciem pełnej dawki. Aby osiągnąć odpowiednią skuteczność terapii, po początkowym okresie dostosowywania dawki należy osiągnąć i utrzymać dawkę 30 mikrogramów na tydzień.
Zestaw do miareczkowania AVOSTARTCLIP został zaprojektowany do użytku wyłącznie z ampułko-strzykawką. Może być stosowany do uzyskania przyrostu dawki o ¼ lub ½. Każdy AVOSTARTCLIP należy użyć jeden raz, a następnie wyrzucić wraz z pozostałą w strzykawce zawartością AVONEX.
Przed wstrzyknięciem i przez kolejne 24 godziny po każdym wstrzyknięciu zaleca się stosowanie przeciwgorączkowego leku przeciwbólowego w celu zmniejszenia objawów grypopodobnych związanych z podawaniem preparatu AVONEX.Objawy te zwykle występują w ciągu pierwszych miesięcy leczenia.
Populacja pediatrycznaBezpieczeństwo i skuteczność preparatu AVONEX u młodzieży w wieku od 12 do 16 lat nie zostały jeszcze ustalone.Obecnie dostępne dane opisano w punktach 4.8 i 5.1, ale nie można sformułować zaleceń dotyczących dawkowania.
Bezpieczeństwo i skuteczność preparatu AVONEX u dzieci w wieku poniżej 12 lat nie zostały jeszcze ustalone.Brak dostępnych danych.
Starsi mieszkańcy: badania kliniczne nie obejmowały wystarczającej liczby pacjentów w wieku 65 lat i starszych, aby ustalić, czy reagują oni inaczej niż osoby młodsze. Jednak w oparciu o sposób klirensu substancji czynnej nie ma teoretycznego powodu, dla którego konieczne jest dostosowanie dawki u pacjentów w podeszłym wieku.
Sposób podawania
Miejsce wstrzyknięcia domięśniowego należy zmieniać co tydzień (patrz punkt 5.3).
Lekarz może przepisać igłę o średnicy 25 na 25 mm pacjentom, u których należy używać tej igły do wstrzyknięcia domięśniowego.
Obecnie nie wiadomo, jak długo pacjent powinien być leczony. Pacjentów należy poddać ocenie klinicznej po dwóch latach leczenia, a decyzję o dłuższym leczeniu powinien podejmować indywidualnie lekarz prowadzący. Leczenie należy przerwać, jeśli u pacjenta rozwinie się przewlekle postępujące stwardnienie rozsiane.
04.3 Przeciwwskazania
- Rozpoczęcie leczenia w ciąży (patrz punkt 4.6).
- Pacjenci z nadwrażliwością na naturalny lub rekombinowany interferon beta lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1.
- Pacjenci z ciężką depresją i (lub) trwającymi myślami samobójczymi (patrz punkty 4.4 i 4.8).
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania
AVONEX należy stosować ostrożnie u pacjentów z obecnym lub przebytym zespołem depresyjnym lub innymi zaburzeniami nastroju, szczególnie u pacjentów z myślami samobójczymi w wywiadzie (patrz punkt 4.3). Wiadomo, że depresja i myśli samobójcze są stanami, które występują częściej u pacjentów ze stwardnieniem rozsianym oraz w związku ze stosowaniem interferonu. Pacjentom należy zalecić, aby niezwłocznie zgłaszali wszelkie objawy depresji i (lub) myśli samobójcze lekarzowi prowadzącemu.
Pacjenci z objawami depresji powinni być ściśle monitorowani podczas leczenia i odpowiednio leczeni. Należy rozważyć przerwanie leczenia produktem AVONEX (patrz również punkty 4.3 i 4.8).
Należy zachować ostrożność podczas podawania produktu AVONEX pacjentom z napadami drgawkowymi w wywiadzie oraz pacjentom leczonym lekami przeciwpadaczkowymi, zwłaszcza jeśli ich padaczka nie jest odpowiednio kontrolowana przez leki przeciwpadaczkowe (patrz punkty 4.5 i 4.8).
Należy zachować ostrożność i rozważyć ścisłe monitorowanie podczas podawania produktu AVONEX pacjentom z ciężkimi zaburzeniami czynności nerek i wątroby oraz pacjentom z ciężką mielosupresją.
Mikroangiopatia zakrzepowa (TMA): Odnotowano przypadki TMA objawiające się zakrzepową plamicą małopłytkową (TTP) lub zespołem hemolityczno-mocznicowym (HUS), w tym przypadki śmiertelne po podaniu interferonu-beta. Zdarzenia były zgłaszane w różnym czasie w trakcie leczenia i mogą wystąpić od kilku tygodni do kilku lat po rozpoczęciu leczenia interferonem beta.Początkowe objawy kliniczne obejmują małopłytkowość, nowo pojawiające się nadciśnienie, gorączkę, objawy dotyczące ośrodkowego układu nerwowego (np. splątanie, niedowład) i upośledzenie czynności nerek Wyniki laboratoryjne sugerujące obecność TMA obejmują zmniejszoną liczbę płytek krwi, zwiększoną dehydrogenazę mleczanową (LDH) w surowicy z powodu hemolizy oraz obecność schistocytów (fragmentacja erytrocytów) w rozmazie krwi. W związku z tym, w przypadku zaobserwowania klinicznych cech TMA, zaleca się dalsze badania poziomu płytek krwi, LDH w surowicy, rozmazów krwi i czynności nerek.Zaleca się natychmiastowe leczenie (z uwzględnieniem wymiany osocza) i natychmiastowe odstawienie produktu Avonex.
Zespół nerczycowy - W trakcie leczenia produktami zawierającymi interferon beta zgłaszano przypadki zespołu nerczycowego z kilkoma podstawowymi nefropatiami, w tym zapadanie się ogniskowego segmentowego stwardnienia kłębuszków nerkowych (FSGS), choroba z minimalnymi zmianami, MCD), błoniasto-proliferacyjne kłębuszkowe zapalenie nerek (błoniastoproliferacyjne kłębuszkowe zapalenie nerek) i błoniaste zapalenie kłębuszków nerkowych (MPN) MGN). Zdarzenia były zgłaszane w różnym czasie w trakcie leczenia i mogą wystąpić po kilku latach leczenia interferonem beta. Zaleca się okresowe monitorowanie pod kątem wczesnych oznak lub objawów, takich jak obrzęk, białkomocz i zaburzenia czynności nerek, szczególnie u pacjentów ze zwiększonym ryzykiem choroby nerek. Zespół nerczycowy należy szybko leczyć i należy rozważyć przerwanie stosowania produktu AVONEX.
Po wprowadzeniu do obrotu zgłaszano przypadki uszkodzenia wątroby, w tym podwyższone stężenie enzymów wątrobowych w surowicy, zapalenie wątroby, autoimmunologiczne zapalenie wątroby i niewydolność wątroby związane ze stosowaniem interferonu beta (patrz punkt 4.8).W niektórych przypadkach reakcje takie występowały. innych produktów leczniczych, które były związane z uszkodzeniem wątroby Nie ustalono możliwości wystąpienia dodatkowych skutków podawania wielu produktów leczniczych lub innych środków hepatotoksycznych (np. alkoholu). Pacjentów należy monitorować pod kątem objawów uszkodzenia wątroby i zachować ostrożność stosowanie interferonów jednocześnie z innymi produktami leczniczymi związanymi z uszkodzeniem wątroby.
Pacjenci z chorobami serca, takimi jak dusznica bolesna, zastoinowa niewydolność serca lub arytmia powinni być ściśle monitorowani pod kątem pogorszenia ich stanu zdrowia podczas leczenia preparatem AVONEX Objawy grypopodobne związane z leczeniem preparatem AVONEX mogą być stresujące dla pacjentów ze współistniejącymi zaburzeniami czynności serca.
Podczas stosowania interferonów mogą wystąpić nieprawidłowości w danych laboratoryjnych, dlatego podczas leczenia preparatem AVONEX, oprócz badań laboratoryjnych wymaganych zwykle do monitorowania pacjentów ze stwardnieniem rozsianym, zaleca się wykonanie pełnej i różnicowej liczby leukocytów, liczby płytek krwi oraz badań krwi, w tym czynności wątroby testy Pacjenci z mielosupresją mogą wymagać bardziej intensywnego monitorowania morfologii krwi z rozmazem i liczbą płytek krwi.
Pacjenci mogą wytworzyć przeciwciała przeciwko AVONEX. Przeciwciała od niektórych z tych pacjentów zmniejszają aktywność interferonu beta-1a in vitro (przeciwciała neutralizujące). Przeciwciała neutralizujące są związane z redukcją in vivo skutków biologicznych AVONEX i potencjalnie może być związany ze zmniejszeniem skuteczności klinicznej Szacuje się, że plateau częstości tworzenia przeciwciał neutralizujących osiągane jest po 12 miesiącach leczenia Ostatnie badania kliniczne przeprowadzone na pacjentach leczonych przez okres do trzech lat z AVONEX sugerują, że około 5% do 8% z nich wytwarza przeciwciała neutralizujące.
Stosowanie różnych metod oznaczania przeciwciał surowicy przeciwko interferonowi ogranicza możliwość porównania antygenowości różnych produktów.
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji
Nie przeprowadzono formalnych badań interakcji u ludzi.
Interakcje preparatu AVONEX z kortykosteroidami lub z hormonem adrenokortykotropowym (ACTH) nie były systematycznie badane.Badania kliniczne wskazują, że pacjenci ze stwardnieniem rozsianym mogą otrzymywać AVONEX i kortykosteroidy lub ACTH podczas rzutów.
Istnieją doniesienia, że interferony zmniejszają aktywność enzymów wątrobowych zależnych od cytochromu P450 u ludzi i zwierząt. Oceniono wpływ podawania dużych dawek produktu AVONEX na metabolizm zależny od P450 u małp i nie zaobserwowano zmian w zdolności metabolizmu wątroby.Należy zachować ostrożność, gdy AVONEX jest podawany w skojarzeniu z produktami leczniczymi o wąskim indeksie terapeutycznym. „klirens” w dużej mierze zależy od układu wątrobowego cytochromu P450, na przykład od niektórych klas leków przeciwpadaczkowych i przeciwdepresyjnych.
04.6 Ciąża i laktacja
Ciąża
Dane dotyczące stosowania produktu AVONEX w ciąży są ograniczone.Dostępne dane wskazują na możliwość zwiększonego ryzyka samoistnego poronienia.Rozpoczęcie leczenia w okresie ciąży jest przeciwwskazane (patrz punkt 4.3).
Kobiety w wieku rozrodczym muszą stosować odpowiednie metody antykoncepcji. Pacjentki, które zaszły w ciążę i planują zajście w ciążę podczas leczenia produktem AVONEX, należy poinformować o potencjalnym ryzyku i rozważyć przerwanie leczenia produktem AVONEX (patrz punkt 5.3). U pacjentek z dużą częstością nawrotów przed rozpoczęciem leczenia należy rozważyć ryzyko poważnego nawrotu po przerwaniu stosowania produktu AVONEX z powodu ciąży w stosunku do możliwego zwiększonego ryzyka samoistnego poronienia.
Czas karmienia
Nie wiadomo, czy AVONEX przenika do mleka ludzkiego. Ze względu na możliwość wystąpienia ciężkich działań niepożądanych u niemowląt karmionych piersią należy podjąć decyzję, czy przerwać karmienie piersią, czy też leczenie AVONEX.
Płodność
Badania płodności i rozwoju przeprowadzono na małpach rezus z pokrewną postacią interferonu beta-1a. U badanych zwierząt po podaniu bardzo dużych dawek zaobserwowano skutki bezowulacyjne i poronne (patrz punkt 5.3).
Brak dostępnych informacji na temat wpływu interferonu beta-1a na płodność mężczyzn.
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Nie przeprowadzono badań nad wpływem preparatu AVONEX na zdolność prowadzenia pojazdów i obsługiwania maszyn Zgłoszone działania niepożądane dotyczące ośrodkowego układu nerwowego mogą mieć niewielki wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn u wrażliwych pacjentów (patrz punkt 4.8).
04.8 Działania niepożądane
Największa częstość występowania działań niepożądanych związanych z terapią AVONEX jest związana z objawami grypopodobnymi.Najczęściej zgłaszanymi objawami grypopodobnymi są: bóle mięśni, gorączka, dreszcze, pocenie się, astenia, ból głowy i nudności. wykazały zmniejszenie nasilenia i częstości występowania objawów grypopodobnych.Objawy grypopodobne wydają się być bardziej nasilone na początku leczenia i stają się rzadsze w trakcie dalszego leczenia.
Po wstrzyknięciu produktu mogą wystąpić przejściowe objawy neurologiczne, które mogą przypominać zaostrzenie SM. W dowolnym momencie leczenia mogą wystąpić przejściowe epizody hipertonii i (lub) ciężkiego osłabienia mięśni, które uniemożliwiają wykonywanie ruchów dowolnych. Epizody te mają ograniczony czas trwania, są czasowo związane z wstrzyknięciami i mogą nawracać po kolejnych wstrzyknięciach. W niektórych przypadkach objawy te są związane z objawami grypopodobnymi.
Częstość obserwowanych działań niepożądanych jest wyrażona w pacjentolat według następujących kategorii:
Bardzo często (≥1/10 pacjentolat);
Często (≥1/100,
Niezbyt często (≥1/1000 do
Rzadko (≥1/10 000,
Bardzo rzadkie (
Nieznana (częstość nie może być określona na podstawie dostępnych danych).
Wskaźnik czasu pacjenta reprezentuje sumę poszczególnych jednostek czasu, przez które pacjent badany był narażony na AVONEX przed wystąpieniem działania niepożądanego. Na przykład 100 osobolat może oznaczać 100 pacjentów leczonych przez jeden rok lub 200 pacjentów leczonych przez pół roku .
W poniższej tabeli wymieniono działania niepożądane z badań (badania kliniczne i obserwacyjne z okresem obserwacji od dwóch do sześciu lat) oraz inne działania niepożądane zidentyfikowane na podstawie spontanicznych zgłoszeń użytkowników o nieznanej częstości.
W każdej klasie częstości działania niepożądane są zgłaszane w porządku malejącym według ciężkości.
* Efekt klasy dla produktów zawierających interferon-beta (patrz punkt 4.4)
+ Efekt klasy dla leków zawierających interferon, patrz poniżej Tętnicze nadciśnienie płucne.
1 Zgłaszano reakcje w miejscu wstrzyknięcia, w tym ból, stan zapalny i bardzo rzadkie przypadki ropnia lub zapalenia tkanki łącznej, które mogą wymagać zabiegu chirurgicznego.
2 Częstotliwość manifestacji jest wyższa na początku terapii.
3 Po wstrzyknięciu preparatu AVONEX może wystąpić omdlenie, ale zwykle jest to odosobniony epizod, który zwykle pojawia się na początku leczenia i nie powraca po kolejnych wstrzyknięciach.
Tętnicze nadciśnienie płucne
Po zastosowaniu produktów leczniczych zawierających interferon beta zgłaszano przypadki tętniczego nadciśnienia płucnego (PAH). Zdarzenia były zgłaszane w różnym czasie, w tym kilka lat po rozpoczęciu leczenia interferonem beta.
Populacja pediatryczna
Nieliczne opublikowane dane sugerują, że profil bezpieczeństwa u młodzieży w wieku 12-16 lat otrzymującej AVONEX 30 mikrogramów domięśniowo (im.) raz w tygodniu jest podobny do obserwowanego u dorosłych.
Zgłaszanie podejrzewanych działań niepożądanych
Zgłaszanie podejrzewanych działań niepożądanych, które występują po dopuszczeniu produktu leczniczego do obrotu, jest ważne, ponieważ umożliwia ciągłe monitorowanie stosunku korzyści do ryzyka produktu leczniczego. Pracownicy służby zdrowia proszeni są o zgłaszanie wszelkich podejrzewanych działań niepożądanych za pośrednictwem Włoskiej Agencji Leków. . Strona internetowa: www.agenziafarmaco.gov.it/it/responsabili.
04.9 Przedawkowanie
Nie zgłoszono żadnych przypadków przedawkowania. Jednak w przypadku przedawkowania pacjent powinien być hospitalizowany w celu obserwacji i otrzymać odpowiednie leczenie wspomagające.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE
05.1 Właściwości farmakodynamiczne
Grupa farmakoterapeutyczna: interferony.
Kod ATC: L03 AB07.
Interferony to rodzina naturalnych białek wytwarzanych przez komórki eukariotyczne w odpowiedzi na infekcje wirusowe i inne induktory biologiczne.Interferony to cytokiny pośredniczące w działaniu przeciwwirusowym, antyproliferacyjnym i immunomodulującym.Wyróżniono trzy główne formy interferonu: interferony alfa, beta i gamma beta są klasyfikowane jako interferony typu I, a interferon gamma jako interferon typu II. Interferony te mają nakładające się, ale wyraźnie rozróżnialne aktywności biologiczne. Mogą również różnić się pod względem komórkowego miejsca syntezy.
Interferon beta jest wytwarzany przez różne typy komórek, w tym fibroblasty i makrofagi. Naturalny interferon beta i AVONEX (interferon beta-1a) są glikozylowane i mają pojedynczą cząsteczkę węglowodanu złożonego związaną z azotem. W przypadku innych białek wiadomo, że glikozylacja wpływa na stabilność krwi, aktywność, dystrybucja biologiczna i okres półtrwania.Jednak wpływ interferonu beta, który jest zależny od glikozylacji, nie jest w pełni określony.
Mechanizm akcji
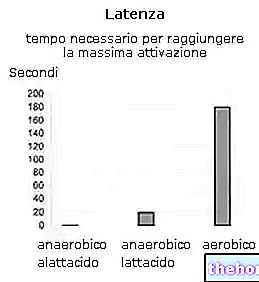
AVONEX wywiera swoje działanie biologiczne poprzez wiązanie się ze specyficznymi receptorami na powierzchni komórek ludzkich. To połączenie inicjuje złożoną kaskadę zdarzeń wewnątrzkomórkowych, prowadzącą do ekspresji licznych produktów genów i markerów indukowanych interferonem. Należą do nich MHC klasy I, białko Mx, 2"/5" - syntaza oligoadenylanowa, mikroglobulina β2 i neopteryna. Niektóre z tych produktów zostały zmierzone we frakcjach surowicy i komórek krwi pobranej od pacjentów leczonych preparatem AVONEX. Po podaniu pojedynczej dawki domięśniowej AVONEX poziom tych produktów w surowicy utrzymuje się na podwyższonym poziomie przez co najmniej cztery dni do tygodnia.
Nie wiadomo, czy mechanizm działania AVONEX w stwardnieniu rozsianym przebiega zgodnie z tą samą sekwencją zdarzeń biologicznych, jak opisano powyżej, ponieważ patofizjologia stwardnienia rozsianego nie jest dobrze poznana.
Skuteczność kliniczna i bezpieczeństwo
Efekty leczenia stwardnienia rozsianego liofilizowanym preparatem AVONEX wykazano w pojedynczym badaniu kontrolowanym placebo z udziałem 301 pacjentów (AVONEX n = 158, placebo n = 143) z nawrotem stwardnienia rozsianego charakteryzującym się co najmniej 2 zaostrzeniami w ciągu ostatnich 3 lat lub co najmniej jednym zaostrzeniem „rok przed przystąpieniem do badania, gdy czas trwania choroby był krótszy niż 3 lata. Do badania włączono pacjentów z wynikiem EDSS na początku badania od 1 do 3,5. Ze względu na projekt badania pacjenci byli obserwowani przez różne okresy czasu. 150 pacjentów leczonych AVONEX ukończyło 1 rok badania, a 85 ukończyło 2 lata badania. W badaniu skumulowany odsetek pacjentów, u których doszło do progresji niepełnosprawności (analiza przeżycia według metody Kaplana-Meiera) pod koniec dwóch lat wynosił 35% w przypadku pacjentów otrzymujących placebo i 22% w przypadku pacjentów leczonych preparatem AVONEX. Progresję niepełnosprawności mierzono jako wzrost o 1,0 punkt w Rozszerzonej Skali Stanu Niepełnosprawności (EDSS), trwający co najmniej sześć miesięcy. Wykazano również zmniejszenie o jedną trzecią rocznego wskaźnika nawrotów. Ten ostatni efekt kliniczny zaobserwowano po ponad roku leczenia.
Randomizowane badanie z podwójnie ślepą próbą porównawcze dawek 802 pacjentów z nawrotowym SM (AVONEX 30 µg n = 402, AVONEX 60 µg n = 400) wykazało brak statystycznie istotnej różnicy lub trendu pomiędzy 30 µg i 60 µg AVONEX w zakresie klinicznym i ogólne parametry magnetycznego rezonansu jądrowego (MRI).
Efekty AVONEX w leczeniu stwardnienia rozsianego zostały również wykazane w randomizowanym, podwójnie zaślepionym badaniu obejmującym 383 pacjentów (AVONEX n = 193, placebo n = 190) z pojedynczym zdarzeniem demielinizacyjnym związanym z co najmniej dwoma zgodnymi zmianami w mózgu wykrytymi w RMN . W grupie leczonej AVONEX zaobserwowano zmniejszenie ryzyka wystąpienia drugiego zdarzenia. Stwierdzono również wpływ na parametry MRI. Szacowane ryzyko wystąpienia drugiego zdarzenia wynosiło 50% w ciągu trzech lat i 39% w ciągu dwóch lat w grupie placebo oraz 35% (trzy lata) i 21% (dwa lata) w grupie leczonej preparatem AVONEX. W analizie post-hoc u pacjentów z co najmniej jedną zmianą ulegającą wzmocnieniu gadolinem i dziewięcioma zmianami w obrazach T2-zależnych w wyjściowym badaniu MRI ryzyko drugiego zdarzenia w ciągu dwóch lat wyniosło 56% w grupie placebo i 21% w grupie leczonej. z AVONEX.Jednak wpływ wczesnego leczenia AVONEX nie jest znany nawet w tej podgrupie wysokiego ryzyka, ponieważ badanie zostało zaprojektowane przede wszystkim w celu oceny odstępu czasu między pierwszym a drugim zdarzeniem, a nie ewolucji. Co więcej, obecnie nie ma dobrze ugruntowanej definicji pacjentów wysokiego ryzyka, chociaż bardziej konserwatywne podejście polega na „akceptacji co najmniej dziewięciu hiperintensywnych zmian w obrazach T2 w początkowym skanie i co najmniej jednej nowej zmiany w obrazach T2 lub jednej nowej zmiany w obrazie kolejne badanie wykonane co najmniej trzy miesiące po pierwszym W każdym przypadku leczenie należy rozważać wyłącznie u pacjentów z grupy wysokiego ryzyka.
Populacja pediatryczna
Nieliczne dane dotyczące skuteczności/bezpieczeństwa preparatu AVONEX uzyskane przez podawanie 15 mikrogramów domięśniowo (im.) raz w tygodniu (n = 8) w porównaniu z grupą nieleczoną (n = 8), z 4-letnią obserwacją, wykazały, że wyniki były zgodne z obserwowane u dorosłych, jednak wyniki w rozszerzonej skali stanu niepełnosprawności (EDSS) wzrosły w leczonej grupie w ciągu 4-letniego okresu obserwacji, wskazując tym samym na progresję choroby.Nie ma bezpośredniego porównania z obecnie zalecaną dawką u dorosłych.
05.2 „Właściwości farmakokinetyczne
Profil farmakokinetyczny preparatu AVONEX oceniano pośrednio metodą pomiaru aktywności przeciwwirusowej interferonu. Ta metoda analizy jest ograniczona, ponieważ jest czuła na interferon, ale nie ma swoistości dla interferonu beta. Alternatywne techniki analizy nie są wystarczająco czułe.
Po domięśniowym podaniu produktu AVONEX, aktywność przeciwwirusowa w surowicy osiąga szczyt pomiędzy 5 a 15 godzinami po leczeniu i zmniejsza się z okresem półtrwania wynoszącym około 10 godzin. Przy odpowiedniej korekcie szybkości wchłaniania z miejsca wstrzyknięcia obliczona biodostępność wynosi około 40%.Wyliczona biodostępność jest większa bez takiej korekty.Podawanie domięśniowe nie może być zastąpione podaniem podskórnym.
05.3 Przedkliniczne dane o bezpieczeństwie
Rakotwórczość: Brak danych dotyczących rakotwórczości dla interferonu beta-1a u zwierząt i ludzi.
Toksyczność przewlekła: W 26-tygodniowym badaniu toksyczności powtórnej u małp rezus, podawanych domięśniowo raz w tygodniu, w skojarzeniu z innym środkiem immunomodulującym, przeciwciałem monoklonalnym przeciwko ligandowi CD40, brak odpowiedzi immunologicznej lub jakiekolwiek oznaki toksyczności wobec interferonu beta-1a.
Tolerancja miejscowa: Podrażnienie domięśniowe nie było oceniane u zwierząt po wielokrotnym podaniu w to samo miejsce wstrzyknięcia.
Mutagenność: Przeprowadzono ograniczone, ale istotne badania mutagenności. Wyniki były negatywne.
Zaburzenie płodności: Badania płodności i rozwoju na małpach rezus przeprowadzono z pokrewną postacią interferonu beta-1a. Przy bardzo dużych dawkach u badanych zwierząt zaobserwowano efekty bezowulacyjne i poronne. Podobny, zależny od dawki wpływ na aktywność reprodukcyjną zaobserwowano również w przypadku innych form interferonów alfa i beta.Nie zaobserwowano działania teratogennego ani wpływu na rozwój płodu, ale dostępne informacje na temat działania interferonu beta-1a w okresie około- i poporodowym są ograniczone.
Brak dostępnych informacji na temat wpływu interferonu beta-1a na płodność mężczyzn.
06.0 INFORMACJE FARMACEUTYCZNE
06.1 Zaróbki
Trihydrat octanu sodu
Lodowaty kwas octowy
Chlorowodorek argininy
Polisorbat 20
Woda do wstrzykiwań
06.2 Niekompatybilność
Nieistotne.
06.3 Okres ważności
3 lata.
06.4 Specjalne środki ostrożności przy przechowywaniu
Przechowywać w lodówce (2°C - 8°C)
NIE ZAMRAŻAĆ.
AVONEX można przechowywać w temperaturze pokojowej (od 15°C do 30°C) do tygodnia.
Przechowywać w oryginalnym opakowaniu (zamkniętej plastikowej tacce) w celu ochrony przed światłem (patrz punkt 6.5).
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania
Ampułkostrzykawka szklana o pojemności 1 ml (Typ I) z nasadką zabezpieczającą przed manipulacją i korkiem tłoka (guma bromobutylowa) zawierająca 0,5 ml roztworu.
Wielkość opakowania: pudełko tekturowe zawierające cztery lub dwanaście ampułko-strzykawek po 0,5 ml. Każda strzykawka jest zapakowana w szczelnie zamkniętą plastikową tackę, która zawiera również igłę iniekcyjną do podania domięśniowego.
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
06.6 Instrukcje użytkowania i obsługi
AVONEX jest dostarczany jako gotowy do użycia roztwór do wstrzykiwań w ampułko-strzykawce.
Po wyjęciu z lodówki AVONEX w ampułko-strzykawce należy ogrzać do temperatury pokojowej (15°C - 30°7C) przez około 30 minut.
Do podgrzewania roztworu AVONEX 30 mcg do wstrzykiwań nie należy używać zewnętrznych źródeł ciepła, takich jak gorąca woda.
Jeśli roztwór do wstrzykiwań zawiera cząstki lub nie jest przezroczysty i bezbarwny, nie należy używać ampułko-strzykawki. Dostarczona jest igła do wstrzykiwań domięśniowych. Preparat nie zawiera konserwantów. Każda ampułko-strzykawka AVONEX zawiera tylko jedną dawkę. Wyrzucić niewykorzystaną część każdej ampułko-strzykawki.
Niewykorzystany lek i odpady pochodzące z tego leku należy usunąć zgodnie z lokalnymi przepisami.
07.0 PODMIOT POZWOLENIA NA DOPUSZCZENIE DO OBROTU
BIOGEN IDEC LIMITED Innovation House 70 Norden Road Maidenhead Berkshire SL6 4AY
Wielka Brytania
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
AIC 033283033
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA
Data pierwszego zezwolenia: 13 marca 1997 r.
Data ostatniego przedłużenia: 13 marca 2007
10.0 DATA ZMIAN TEKSTU
10/2015