Składniki aktywne: Tikagrerol
Brilique 90 mg tabletki powlekane
Dlaczego stosuje się Brilique? Po co to jest?
Co to jest Brilique?
Brilique zawiera substancję czynną o nazwie tikagrelor, która należy do grupy leków zwanych lekami przeciwpłytkowymi.
Jak działa Brilique
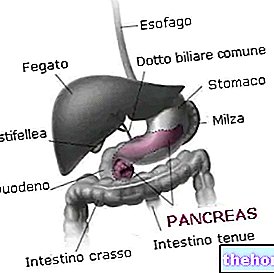
Brilique działa na komórki zwane „płytkami krwi” (zwanymi również trombocytami). Te bardzo małe komórki krwi pomagają zatrzymać krwawienie, zlepiając się, aby zamknąć maleńkie otwory w przerwanych lub uszkodzonych naczyniach krwionośnych.
Jednak płytki krwi mogą również tworzyć skrzepy w chorych naczyniach krwionośnych serca i mózgu, co może być bardzo niebezpieczne, ponieważ:
- zakrzep może całkowicie odciąć dopływ krwi – może to spowodować zawał serca (zawał mięśnia sercowego) lub udar mózgu, lub
- zakrzep może częściowo blokować naczynia krwionośne zaopatrujące serce – to zmniejsza przepływ krwi do serca i może powodować pojawiający się i znikający ból w klatce piersiowej (tzw. „niestabilna dławica piersiowa”). Brilique pomaga blokować zlepianie się płytek krwi, co zmniejsza możliwość tworzenia się zakrzepów krwi, które mogą zmniejszać przepływ krwi.
Do czego służy Brilique
Brilique w skojarzeniu z kwasem acetylosalicylowym (inny lek przeciwpłytkowy) należy stosować wyłącznie u pacjentów dorosłych.
Przepisano jej Brilique, ponieważ miała:
- zawał serca lub
- niestabilna dusznica bolesna (dławica piersiowa lub ból w klatce piersiowej, który nie jest dobrze kontrolowany).
Brilique zmniejsza ryzyko wystąpienia kolejnego zawału serca, udaru lub zgonu z powodu choroby związanej z sercem lub naczyniami krwionośnymi.
Przeciwwskazania Kiedy nie należy stosować leku Brilique
Nie stosować leku Brilique, jeśli:
- jeśli pacjent ma uczulenie na tikagrelor lub którykolwiek z pozostałych składników leku Brilique
- Ciągle krwawi
- Miał udar spowodowany krwawieniem w mózgu.
- Masz umiarkowane lub ciężkie problemy z wątrobą.
- pacjent przyjmuje jeden z następujących leków: ketokonazol (stosowany w leczeniu zakażeń grzybiczych), klarytromycyna (stosowana w leczeniu zakażeń bakteryjnych), nefazodon (lek przeciwdepresyjny), rytonawir i atazanawir (stosowane w leczeniu zakażenia HIV i AIDS).
Nie należy przyjmować leku Brilique, jeśli którakolwiek z powyższych sytuacji dotyczy pacjenta. W razie wątpliwości należy porozmawiać z lekarzem lub farmaceutą przed przyjęciem leku Brilique
Środki ostrożności dotyczące stosowania Informacje ważne przed przyjęciem leku Brilique
Przed przyjęciem leku Brilique należy skontaktować się z lekarzem, farmaceutą lub dentystą, jeśli:
- Masz zwiększone ryzyko krwawienia z powodu:
- niedawna poważna kontuzja
- niedawna operacja (w tym chirurgia stomatologiczna)
- choroba wpływająca na krzepnięcie krwi - niedawne krwawienie z żołądka lub jelit (np. z powodu wrzodu żołądka lub polipów okrężnicy)
- Pacjent planuje poddać się zabiegowi chirurgicznemu (w tym stomatologicznemu) w dowolnym momencie przyjmowania leku Brilique, ponieważ istnieje zwiększone ryzyko krwawienia. Lekarz może zalecić przerwanie stosowania leku Brilique na 7 dni przed zabiegiem chirurgicznym.
- Twoje tętno jest niezwykle niskie (zwykle mniej niż 60 uderzeń na minutę) i nie masz jeszcze wszczepionego instrumentu regulującego rytm serca (stymulatora).
- Masz astmę lub inny problem z płucami lub trudności z oddychaniem.
- Miał już badania krwi, które wykazały więcej kwasu moczowego niż normalnie. Jeśli którakolwiek z powyższych sytuacji dotyczy pacjenta (lub nie ma pewności), przed przyjęciem leku Brilique należy zwrócić się do lekarza, farmaceuty lub stomatologa.
Dzieci i młodzież
Brilique nie jest zalecany dla dzieci i młodzieży w wieku poniżej 18 lat.
Interakcje Jakie leki lub pokarmy mogą zmienić działanie leku Brilique
Należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent przyjmuje, ostatnio przyjmował lub może przyjmować jakiekolwiek inne leki. Dzieje się tak, ponieważ Brilique może wpływać na sposób działania niektórych leków, a niektóre leki mogą mieć wpływ na Brilique.
Należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent przyjmuje którykolwiek z następujących leków:
- więcej niż 40 mg na dobę symwastatyny lub lowastatyny (leki stosowane w leczeniu wysokiego cholesterolu)
- ryfampicyna (antybiotyk), fenytoina, karbamazepina i fenobarbital (stosowane w kontrolowaniu napadów), digoksyna (stosowana w leczeniu niewydolności serca), cyklosporyna (stosowana w celu obniżenia odporności organizmu), chinidyna i diltiazem (stosowane w leczeniu niewydolności serca) nieprawidłowy rytm serca ), beta-adrenolityki i werapamil (stosowany w leczeniu wysokiego ciśnienia krwi).
W szczególności należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent przyjmuje którykolwiek z następujących leków, które zwiększają ryzyko krwawienia:
- „doustne antykoagulanty” często określane jako „rozrzedzacze krwi”, które obejmują warfarynę.
- niesteroidowe leki przeciwzapalne (w skrócie NLPZ), często stosowane jako leki przeciwbólowe, takie jak ibuprofen i naproksen.
- selektywne inhibitory wychwytu zwrotnego serotoniny (w skrócie SSRI) przyjmowane jako leki przeciwdepresyjne, takie jak paroksetyna, sertralina i citalopram.
- inne leki, takie jak ketokonazol (stosowany w leczeniu zakażeń grzybiczych), klarytromycyna (stosowana w leczeniu zakażeń bakteryjnych), nefazodon (lek przeciwdepresyjny), rytonawir i atazanawir (stosowane w leczeniu zakażenia HIV i AIDS), cyzapryd (stosowany w leczeniu zgagi) lub sporysz alkaloidy (stosowane w leczeniu migren i bólów głowy).
Należy również poinformować lekarza, że przyjmowanie leku Brilique może powodować zwiększone ryzyko krwawienia, jeśli lekarz przepisze leki fibrynolityczne, często nazywane „lekami trombolitycznymi”, takie jak streptokinaza lub alteplaza.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
Ciąża i karmienie piersią
Nie zaleca się stosowania leku Brilique w przypadku ciąży lub podejrzenia ciąży.Kobiety powinny stosować odpowiednie metody antykoncepcji, aby uniknąć zajścia w ciążę podczas stosowania tego leku. Jeśli pacjentka karmi piersią, przed przyjęciem leku Brilique należy zwrócić się do lekarza. W tym czasie lekarz omówi z pacjentem korzyści i zagrożenia związane z leczeniem lekiem Brilique.
Jeśli pacjentka jest w ciąży lub karmi piersią, podejrzewa, że może być w ciąży lub planuje mieć dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem tego leku.
Prowadzenie i używanie maszyn
Jest mało prawdopodobne, aby Brilique wpływał na zdolność prowadzenia pojazdów i obsługiwania maszyn. W przypadku wystąpienia zawrotów głowy podczas przyjmowania leku Brilique należy zachować ostrożność podczas prowadzenia pojazdów lub obsługiwania maszyn
Dawka, sposób i czas podawania Jak stosować Brilique: Dawkowanie
Ten lek należy zawsze stosować zgodnie z zaleceniami lekarza lub farmaceuty. W razie wątpliwości skonsultuj się z lekarzem lub farmaceutą.
Ile leku Brilique należy wziąć
- Dawka początkowa to dwie tabletki na raz (dawka wysycająca 180 mg). Ta dawka będzie zwykle podawana w szpitalu.
- Po tej dawce początkowej zwykle stosowana dawka to jedna tabletka 90 mg dwa razy na dobę przez okres do 12 miesięcy, chyba że lekarz zaleci inaczej. Lek Brilique należy przyjmować codziennie o mniej więcej tej samej porze (np. jedną tabletkę rano i jedną wieczorem).
Lekarz zazwyczaj zaleci również przyjmowanie kwasu acetylosalicylowego.Jest to substancja znajdująca się w wielu lekach stosowanych w celu zapobiegania krzepnięciu krwi.Lekarz powie, ile należy przyjmować (zwykle od 75 do 150 mg na dobę).
Jak przyjmować lek Brilique
- Tabletkę można przyjmować z posiłkami lub bez posiłków.
- można sprawdzić, kiedy została przyjęta ostatnia tabletka Brilique, patrząc na blister.Jest słońce (rano) i księżyc (wieczorem). Dzięki temu dowiesz się, czy przyjąłeś dawkę.
W przypadku trudności z połknięciem tabletki (tabletek)
Jeśli masz trudności z połknięciem tabletki (tabletek), możesz je rozkruszyć i wymieszać z wodą w następujący sposób:
- Zmiażdż tabletkę (tabletki) na drobny proszek
- Wsyp proszek do pół szklanki wody
- Zamieszaj i wypij natychmiast
- Aby upewnić się, że nie pozostawiłeś żadnych lekarstw, wypłucz pustą szklankę połową szklanki wody i wypij.
Przedawkowanie Co zrobić w przypadku przyjęcia zbyt dużej dawki leku Brilique
Przyjęcie większej niż zalecana dawki leku Brilique
W przypadku zażycia większej niż zalecana dawki leku Brilique należy natychmiast skontaktować się z lekarzem lub udać się do szpitala, zabierając ze sobą opakowanie leku, ponieważ może wystąpić zwiększone ryzyko krwawienia.
Pominięcie przyjęcia leku Brilique
- W przypadku pominięcia dawki, następną dawkę należy przyjąć jak zwykle.
- Nie należy stosować dawki podwójnej (dwóch dawek jednocześnie) w celu uzupełnienia pominiętej dawki.
Przerwanie stosowania leku Brilique
Nie należy przerywać przyjmowania leku Brilique bez wcześniejszej konsultacji z lekarzem. Lek Brilique należy przyjmować regularnie i tak długo, jak zaleci to lekarz.
Przerwanie stosowania leku Brilique może zwiększyć prawdopodobieństwo wystąpienia kolejnego zawału serca lub udaru mózgu albo zgonu z powodu choroby związanej z problemami z sercem lub naczyniami krwionośnymi.
W razie dalszych pytań dotyczących stosowania tego leku należy zwrócić się do lekarza lub farmaceuty
Skutki uboczne Jakie są skutki uboczne Brilique?
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Podczas stosowania tego leku mogą wystąpić następujące działania niepożądane:
Natychmiast skontaktuj się z lekarzem, jeśli zauważysz którykolwiek z poniższych objawów – możesz potrzebować pilnej pomocy medycznej:
- Krwawienie w mózgu lub wewnątrz czaszki jest rzadkim skutkiem ubocznym i może powodować objawy udaru, takie jak:
- nagłe drętwienie lub osłabienie rąk, nóg lub twarzy, zwłaszcza jeśli tylko po jednej stronie ciała
- nagłe zamieszanie, trudności w mówieniu lub rozumieniu innych
- nagłe trudności w chodzeniu lub utrata równowagi lub koordynacji - nagłe zawroty głowy lub nagły intensywny ból głowy bez znanej przyczyny
- Krwawienie – często występuje pewne krwawienie. Jednak ciężkie krwawienie nie jest częstym zjawiskiem, ale może zagrażać życiu. Można zwiększyć różne rodzaje krwawienia, takie jak:
- krwawienie, które jest ciężkie lub nie może być opanowane
- nieoczekiwane krwawienie lub krwawienie utrzymujące się przez długi czas
- obecność krwi w moczu
- produkcja czarnych stolców lub czerwonej krwi w stolcu
- zaburzenia widzenia spowodowane obecnością krwi w oczach
- uwalnianie zakrzepów krwi poprzez kaszel lub wymioty
- krwawienie wewnątrz stawów powodujące obrzęk i ból
Skontaktuj się z lekarzem, jeśli zauważysz którykolwiek z następujących objawów:
- Zadyszka – to zjawisko powszechne. Może to być spowodowane chorobą serca lub inną przyczyną albo może być działaniem niepożądanym leku Brilique.Jeśli świszczący oddech nasila się lub utrzymuje się z upływem czasu, należy powiedzieć o tym lekarzowi.Lekarz zdecyduje, czy konieczne jest leczenie, czy też podejmie dalsze badania. .
Inne możliwe skutki uboczne
Często (może dotyczyć do 1 na 10 osób)
- Siniaki
- Krwotok z nosa
- Obfite krwawienie z operacji, skaleczeń lub ran
Niezbyt często (może dotyczyć do 1 na 100 osób)
- Reakcja alergiczna – wysypka, swędzenie lub obrzęk twarzy lub warg/języka mogą być objawami reakcji alergicznej
- Bół głowy
- Zawroty głowy lub jakby pokój się wirował
- Ból brzucha
- Biegunka lub niestrawność
- Złe samopoczucie lub złe samopoczucie
- Wysypka
- Swędzący
- Zapalenie żołądka (zapalenie żołądka)
- Krwawienie z pochwy, które jest bardziej nasilone lub występuje w czasie innym niż normalne krwawienie miesiączkowe (miesiączkowe)
- Krwawienie ze ścian żołądka (wrzód)
- Krwawienie z dziąseł
Rzadko (może dotyczyć do 1 na 1000 osób)
- Zaparcie
- Mrowienie
- dezorientacja
- Krew w uszach
- Krwotok wewnętrzny
Zgłaszanie skutków ubocznych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe działania niepożądane niewymienione w tej ulotce, należy porozmawiać z lekarzem lub farmaceutą. Skutki uboczne można również zgłaszać bezpośrednio za pośrednictwem krajowego systemu zgłaszania wymienionego w załączniku V.
Zgłaszając działania niepożądane, możesz dostarczyć więcej informacji na temat bezpieczeństwa tego leku.
Wygaśnięcie i przechowywanie
Nie stosować tego leku po upływie terminu ważności zamieszczonego na blistrze i pudełku po skrócie EXP / EXP. Termin ważności oznacza ostatni dzień podanego miesiąca.Nie należy wyrzucać żadnych leków do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa. Pomoże to chronić środowisko.
Zawartość opakowania i inne informacje
Co zawiera lek Brilique
- Substancją czynną jest tikagrelor. Każda tabletka powlekana zawiera 90 mg tikagreloru.
- Pozostałe składniki to:
Rdzeń tabletu: mannitol (E421), wapnia wodorofosforan dwuwodny, sól sodowa glikolanu skrobi, hydroksypropyloceluloza (E463), magnezu stearynian (E470b)
Powłoka tabletki: hypromeloza (E464), tytanu dwutlenek (E171), talk, glikol polietylenowy 400 i żółty tlenek żelaza (E172).
Opis wyglądu leku Brilique i co zawiera opakowanie
Tabletka powlekana (tabletka): Tabletki są okrągłe, obustronnie wypukłe, żółte, powlekane, z wytłoczoną liczbą „90” nad „T” po jednej stronie.
Brilique jest dostępny w:
- standardowy blister (z symbolami słońca/księżyca) w kartonikach po 60 i 180 tabletek
- blister kalendarzowy (z symbolami słońca / księżyca) w kartonikach po 14, 56 i 168 tabletek
- perforowane blistry jednodawkowe w kartoniku po 100x1 tabletek.
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO
BRILIQUE 90 MG TABLETKI POWLEKANE FOLIĄ
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY
Każda tabletka powlekana zawiera 90 mg tikagreloru.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
03.0 POSTAĆ FARMACEUTYCZNA
Tabletka powlekana (tabletka).
Okrągłe, dwuwypukłe, żółte tabletki z wytłoczonym „90” nad „T” po jednej stronie i gładkie po drugiej stronie.
04.0 INFORMACJE KLINICZNE
04.1 Wskazania terapeutyczne
Brilique w skojarzeniu z kwasem acetylosalicylowym (ASA) jest wskazany w zapobieganiu incydentom miażdżycowo-zakrzepowym u dorosłych pacjentów z ostrym zespołem wieńcowym (niestabilna dusznica bolesna, zawał mięśnia sercowego bez uniesienia odcinka ST [NSTEMI] lub zawał mięśnia sercowego z uniesieniem odcinka ST [STEMI]. ), w tym pacjentów leczonych farmakologicznie i przechodzących przezskórną interwencję wieńcową (PCI) lub pomostowanie aortalno-wieńcowe (CABG).
Więcej informacji można znaleźć w paragrafie 5.1.
04.2 Dawkowanie i sposób podawania
Dawkowanie
Leczenie produktem Brilique należy rozpocząć od pojedynczej dawki nasycającej 180 mg (dwie tabletki 90 mg), a następnie kontynuować 90 mg dwa razy na dobę.
Pacjenci leczeni produktem Brilique powinni również przyjmować ASA codziennie, o ile nie ma szczególnych przeciwwskazań. Po podaniu początkowej dawki ASA produkt Brilique należy przyjmować z dawką podtrzymującą ASA od 75 do 150 mg (patrz punkt 5.1).
Zaleca się leczenie przez okres do 12 miesięcy, chyba że przerwanie leczenia produktem Brilique jest klinicznie wskazane (patrz punkt 5.1).Doświadczenie powyżej 12 miesięcy jest ograniczone.
U pacjentów z ostrym zespołem wieńcowym (ACS) przedwczesne przerwanie jakiegokolwiek leczenia przeciwpłytkowego, w tym leku Brilique, może skutkować zwiększonym ryzykiem zgonu z przyczyn sercowo-naczyniowych lub zawału mięśnia sercowego z powodu choroby podstawowej pacjenta. Dlatego należy unikać przedwczesnego przerwania leczenia.
Należy również unikać przerw w ciągłości leczenia. Pacjent, który pominął dawkę produktu Brilique, powinien przyjąć tylko jedną tabletkę 90 mg (następną dawkę) o zaplanowanej porze.
Jeśli to konieczne, pacjenci leczeni klopidogrelem mogą być przestawieni bezpośrednio na Brilique (patrz punkt 5.1). Nie przeprowadzono badań dotyczących zamiany prasugrelu na Brilique.
Populacje specjalne
Starsi mieszkańcy
Nie ma konieczności dostosowania dawki u pacjentów w podeszłym wieku (patrz punkt 5.2).
Pacjenci z zaburzeniami czynności nerek
Nie ma konieczności dostosowania dawki u pacjentów z zaburzeniami czynności nerek (patrz punkt 5.2). Brak dostępnych informacji dotyczących leczenia pacjentów dializowanych, dlatego nie zaleca się stosowania produktu Briliquen u tych pacjentów.
Pacjenci z zaburzeniami czynności wątroby
Lek Brilique nie był badany u pacjentów z umiarkowanymi lub ciężkimi zaburzeniami czynności wątroby. Dlatego u pacjentów z umiarkowanymi lub ciężkimi zaburzeniami czynności wątroby jego stosowanie jest przeciwwskazane (patrz punkty 4.3, 4.4 i 5.2). Nie ma konieczności dostosowania dawki u pacjentów z łagodnymi zaburzeniami czynności wątroby.
Populacja pediatryczna
Bezpieczeństwo i skuteczność produktu Brilique u dzieci w wieku poniżej 18 lat w zatwierdzonych wskazaniach u dorosłych nie zostały ustalone.Brak dostępnych danych.
Sposób podawania
Do stosowania doustnego.
Brilique można podawać z posiłkami lub między posiłkami.
W przypadku pacjentów, którzy nie są w stanie połknąć tabletki (tabletek) w całości, tabletki Brilique można rozkruszyć na drobny proszek, wymieszać w połowie szklanki wody i natychmiast wypić. Szklankę należy wypłukać dodatkową połową szklanki. zawartość pijany. Mieszaninę można również podawać przez sondę nosowo-żołądkową (CH8 lub większą). Po podaniu mieszaniny ważne jest przepłukanie zgłębnika nosowo-żołądkowego wodą.
04.3 Przeciwwskazania
• Nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1 (patrz punkt 4.8).
• Trwające krwawienie patologiczne.
• Krwotok śródczaszkowy w wywiadzie (patrz punkt 4.8).
• Umiarkowane do ciężkich zaburzenia czynności wątroby (patrz punkty 4.2, 4.4 i 5.2).
• Jednoczesne podawanie tikagreloru z silnymi inhibitorami CYP3A4 (np. ketokonazolem, klarytromycyną, nefazodonem, rytonawirem i atazanawirem) jest przeciwwskazane, ponieważ jednoczesne podawanie może prowadzić do znacznego zwiększenia ekspozycji na tikagrelor (patrz punkt 4.5).
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania
Ryzyko krwawienia
W głównym badaniu klinicznym III fazy (PLATO [PLATelet Inhibition and Patient Outcomes], 18 624 pacjentów) główne kryteria wykluczające obejmowały zwiększone ryzyko krwawienia, klinicznie istotną małopłytkowość lub niedokrwistość, wcześniejsze krwawienie śródczaszkowe, krwawienie z przewodu pokarmowego w ciągu ostatnich 6 miesięcy lub poważna operacja w ciągu ostatnich 30 dni. Pacjenci z ostrym zespołem wieńcowym leczeni preparatem Brilique i ASA wykazywali zwiększone ryzyko poważnych krwawień niezwiązanych z CABG, a bardziej ogólnie krwawień wymagających nadzoru lekarskiego, tj. duże + małe krwawienia według kryteriów PLATO, ale nie krwawienia śmiertelne lub te, które były przyczyną życia -zagrażające (patrz punkt 4.8).
Dlatego stosowanie produktu Brilique u pacjentów ze stwierdzonym zwiększonym ryzykiem krwawienia należy zestawić z korzyściami pod względem zapobiegania incydentom zakrzepicy w przebiegu miażdżycy.Jeśli istnieją wskazania kliniczne, produkt Brilique należy stosować ostrożnie w następujących grupach pacjentów:
• Pacjenci ze skłonnością do krwawienia (np. z powodu niedawnego urazu, niedawnego zabiegu chirurgicznego, zaburzeń krzepnięcia, aktywnego lub niedawnego krwawienia z przewodu pokarmowego). Stosowanie produktu Brilique jest przeciwwskazane u pacjentów z czynnym patologicznym krwawieniem, u pacjentów z krwotokiem śródczaszkowym w wywiadzie oraz u pacjentów z umiarkowanymi lub ciężkimi zaburzeniami czynności wątroby (patrz punkt 4.3).
• Pacjenci, którym jednocześnie podaje się produkty lecznicze, które mogą zwiększać ryzyko krwawienia (np. niesteroidowe leki przeciwzapalne (NLPZ), doustne leki przeciwzakrzepowe i (lub) leki fibrynolityczne) w ciągu 24 godzin po podaniu produktu Brilique.
Nie ma danych dotyczących tikagreloru dotyczących korzyści hemostatycznych przetoczeń płytek krwi; krążąca ilość tikagreloru może hamować przetoczone płytki krwi. Ponieważ jednoczesne podawanie tikagreloru i desmopresyny nie skróciło standardowego czasu krwawienia, jest mało prawdopodobne, aby desmopresyna była skuteczna w klinicznym leczeniu krwawień (patrz punkt 4.5).
Leczenie przeciwfibrynolityczne (kwas aminokapronowy lub kwas traneksamowy) i (lub) rekombinowany czynnik VIIa może nasilać hemostazę Tikagrelor można wznowić po zidentyfikowaniu i opanowaniu przyczyny krwawienia.
Interwencje chirurgiczne
Pacjentom należy zalecić poinformowanie lekarzy i stomatologów o przyjmowaniu leku Brilique przed zaplanowaniem zabiegu chirurgicznego oraz przed przyjęciem jakiegokolwiek nowego leku.
Wśród pacjentów z PLATO poddawanych operacji pomostowania aortalno-wieńcowego (CABG) w ramieniu Brilique występowało więcej krwawień niż klopidogrel, gdy leczenie zostało przerwane w ciągu 1 dnia przed operacją, ale podobny odsetek poważnych krwawień w porównaniu z klopidogrelem, gdy leczenie przerwano 2 lub więcej dni przed zabiegiem chirurgicznym (patrz punkt 4.8). Jeśli pacjent ma zostać poddany planowemu zabiegowi chirurgicznemu, a działanie przeciwpłytkowe nie jest pożądane, produkt Brilique należy odstawić na 7 dni przed zabiegiem (patrz punkt 5.1).
Pacjenci z ryzykiem wystąpienia bradykardii
W wyniku obserwacji w poprzednim badaniu klinicznym, w większości bezobjawowych pauz komorowych, pacjenci ze zwiększonym ryzykiem wystąpienia bradykardii (np. pacjenci bez rozrusznika serca z zespołem chorej zatoki, blokiem przedsionkowo-komorowym II lub III stopnia lub omdleniami związanymi z bradykardią) zostali wykluczeni z głównego badania PLATO. W związku z tym, biorąc pod uwagę ograniczone doświadczenie kliniczne, należy zachować ostrożność podczas stosowania tikagreloru u tych pacjentów (patrz punkt 5.1).
Ponadto należy zachować ostrożność podczas jednoczesnego podawania tikagreloru z produktami leczniczymi, o których wiadomo, że wywołują bradykardię. Jednak w badaniu PLATO nie zaobserwowano klinicznie istotnych dowodów działań niepożądanych po jednoczesnym podaniu z jednym lub więcej produktami leczniczymi, o których wiadomo, że wywołują bradykardię (np. 96% beta-adrenolityki, 33% blokery kanału wapniowego diltiazem i werapamil oraz 4% digoksyna) ( patrz punkt 4.5).
W podbadaniu monitorowania PLATO metodą Holtera u większej liczby pacjentów wystąpiły przerwy komorowe ≥3 sekundy w przypadku tikagreloru niż w przypadku klopidogrelu w ostrej fazie OZW. Wzrost pauz komorowych obserwowany w badaniu Holter z tikagrelorem był większy u pacjentów z przewlekłą niewydolnością serca (CHF) niż w całej badanej populacji podczas ostrej fazy OZW, ale nie po miesiącu leczenia tikagrelorem lub w porównaniu z klopidogrelem. W tej populacji pacjentów nie wystąpiły żadne niepożądane konsekwencje kliniczne związane z tym zaburzeniem równowagi (w tym omdlenie lub zastosowanie stymulatora) (patrz punkt 5.1).
duszność
Epizody duszności zgłaszało 13,8% pacjentów leczonych produktem Brilique i 7,8% pacjentów leczonych klopidogrelem. U 2,2% pacjentów badacze uznali, że duszność ma związek przyczynowy z leczeniem produktem Brilique. Duszność ma zwykle nasilenie łagodne do umiarkowanego i często ustępuje bez konieczności przerwania leczenia.U pacjentów z astmą/POChP może być bezwzględnie zwiększone ryzyko wystąpienia duszności podczas stosowania produktu Brilique (patrz punkt 4.8) Tikagrelor należy stosować ostrożnie u pacjentów z wywiadem astmy i (lub) POChP.
Podwyższenie kreatyniny
Stężenie kreatyniny może wzrosnąć podczas leczenia tikagrelorem (patrz punkt 4.8). Mechanizm nie został wyjaśniony. Czynność nerek należy monitorować po miesiącu, a następnie zgodnie ze standardową praktyką kliniczną, ze szczególnym uwzględnieniem pacjentów w wieku ≥ 75 lat, pacjentów z umiarkowanymi/ciężkimi zaburzeniami czynności nerek oraz pacjentów otrzymujących jednocześnie antagonistów angiotensyny II.
Zwiększony kwas moczowy
W badaniu PLATO pacjenci przyjmujący tikagrelor mieli większe ryzyko hiperurykemii niż pacjenci otrzymujący klopidogrel (patrz punkt 4.8). Należy zachować ostrożność podczas podawania tikagreloru pacjentom z hiperurykemią lub dnawym zapaleniem stawów w wywiadzie. Jako środek ostrożności nie zaleca się stosowania tikagreloru u pacjentów z nefropatią moczanową.
Inne
W oparciu o związek obserwowany w badaniu PLATO pomiędzy dawką podtrzymującą ASA a względną skutecznością tikagreloru w porównaniu z klopidogrelem, jednoczesne podawanie tikagreloru i wysokich dawek podtrzymujących ASA (>300 mg) nie jest zalecane (patrz punkt 5.1).
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji
Tikagrelor jest przede wszystkim substratem CYP3A4 i łagodnym inhibitorem CYP3A4. Tikagrelor jest również substratem glikoproteiny P (P-gp) i słabym inhibitorem P-gp i może zwiększać ekspozycję na substraty P-gp.
Wpływ innych produktów leczniczych na Brilique
Produkty lecznicze metabolizowane przez CYP3A4
Inhibitory CYP3A4
• Silne inhibitory CYP3A4 – Jednoczesne podawanie ketokonazolu i tikagreloru zwiększało Cmax i AUC tikagreloru odpowiednio 2,4 i 7,3-krotnie. Cmax i AUC aktywnego metabolitu zmniejszyły się odpowiednio o 89% i 56% Inne silne inhibitory CYP3A4 (klarytromycyna, nefazodon, rytonawir i atazanawir) mogą wywoływać podobne działanie i dlatego jednoczesne stosowanie silnych inhibitorów CYP3A4 z produktem Brilique jest przeciwwskazane (patrz sekcje 4.3).
• Umiarkowane inhibitory CYP3A4 – Jednoczesne podawanie diltiazemu i tikagreloru zwiększyło Cmax tikagreloru o 69% i AUC 2,7-krotnie oraz zmniejszyło Cmax aktywnego metabolitu o 38%, podczas gdy AUC pozostało niezmienione. Tikagrelor nie ma wpływu na stężenie diltiazemu w osoczu. Inne umiarkowane inhibitory CYP3A4 (np. amprenawir, aprepitant, erytromycyna i flukonazol) mogą wywoływać podobne działanie i można je podawać razem z produktem Brilique.
Induktory CYP3A
Jednoczesne podawanie ryfampicyny i tikagreloru zmniejszyło Cmax i AUC tikagreloru odpowiednio o 73% i 86%.Cmax aktywnego metabolitu pozostała niezmieniona, a AUC zmniejszyło się odpowiednio o 46%. Inne induktory CYP3A (np. fenytoina, karbamazepina i fenobarbital) mogą zmniejszać ekspozycję na tikagrelor.Jednoczesne podawanie tikagreloru z silnymi induktorami CYP3A może zmniejszać ekspozycję i skuteczność na tikagrelor, dlatego nie zaleca się ich jednoczesnego stosowania z produktem Brilique.
Cyklosporyna (inhibitor P-gp i CYP3A)
W obecności cyklosporyna.
Brak danych dotyczących jednoczesnego stosowania tikagreloru z innymi substancjami czynnymi, które są również silnymi inhibitorami glikoproteiny P (P-gp) i umiarkowanymi inhibitorami CYP3A4 (np. werapamil, chinidyna), które również mogą powodować zwiększoną ekspozycję na tikagrelor. Jeśli nie można uniknąć tego związku, należy zachować ostrożność podczas ich jednoczesnego stosowania.
Inni
Kliniczne badania interakcji leków wykazały, że jednoczesne podawanie tikagreloru z heparyną, enoksaparyną i ASA lub desmopresyną nie miało wpływu na profil farmakokinetyczny tikagreloru lub aktywnego metabolitu ani na indukowaną przez ADP agregację płytek krwi w porównaniu z samym tikagrelorem. że zmienną hemostazę należy stosować ostrożnie w połączeniu z tikagrelorem.
Obserwowano dwukrotne zwiększenie narażenia na tikagrelor po codziennym spożyciu dużych ilości soku grejpfrutowego (3 x 200 ml) na dobę. Uważa się, że taka wielkość zwiększenia narażenia nie jest klinicznie istotna u większości pacjentów. .
Wpływ Brilique na inne produkty lecznicze
Produkty lecznicze metabolizowane przez CYP3A4
• Symwastatyna - Jednoczesne podawanie tikagreloru i simwastatyny zwiększało Cmax symwastatyny o 81% i AUC o 56% oraz powodowało zwiększenie Cmax symwastatyny w kwasie o 64% i AUC o 52%, z niektórymi pojedynczymi wzrostami od 2 do 3 razy. Jednoczesne podawanie tikagreloru i symwastatyny w dawkach większych niż 40 mg na dobę może powodować działania niepożądane związane z symwastatyną i należy je rozważyć w stosunku do potencjalnych korzyści.Nie stwierdzono wpływu symwastatyny na stężenie tikagreloru w osoczu. Tikagrelor może wywoływać podobny wpływ na lowastatynę Nie zaleca się jednoczesnego stosowania tikagreloru z dawkami symwastatyny lub lowastatyny większymi niż 40 mg.
• Atorwastatyna - Jednoczesne podawanie atorwastatyny i tikagreloru zwiększało Cmax kwasu atorwastatyny o 23% i AUC o 36%. Podobne zwiększenie wartości AUC i Cmax zaobserwowano dla wszystkich metabolitów kwasu atorwastatyny, które nie są uważane za istotne klinicznie.
• Nie można wykluczyć podobnego wpływu na inne statyny metabolizowane przez CYP3A4. Pacjenci PLATO, którzy otrzymywali tikagrelor, przyjmowali różne statyny, bez problemu powiązania z bezpieczeństwem statyn w 93% kohorty pacjentów PLATO przyjmujących te leki.
Tikagrelor jest łagodnym inhibitorem CYP3A4. Nie zaleca się równoczesnego podawania tikagreloru i substratów CYP3A4 o niskim indeksie terapeutycznym (tj. cyzaprydu lub alkaloidów sporyszu), ponieważ tikagrelor może zwiększać ekspozycję na te produkty lecznicze.
Substraty glikoproteiny P (P-gp) (w tym digoksyna, cyklosporyna)
Jednoczesne podawanie produktu Brilique powodowało zwiększenie Cmax digoksyny o 75% i „AUC” o 28%. Średnie „niższe” stężenia digoksyny były zwiększone o około 30% przy jednoczesnym podaniu tikagreloru, z dwukrotnym maksymalnym indywidualnym wzrostem w obecności digoksyny , Cmax i AUC tikagreloru i jego aktywnego metabolitu nie uległy zmianie.
Dlatego zaleca się odpowiednie monitorowanie kliniczne i (lub) laboratoryjne podczas podawania produktów leczniczych o niskim indeksie terapeutycznym zależnym od P-gp, takich jak digoksyna, jednocześnie z tikagrelorem.
Nie stwierdzono wpływu tikagreloru na stężenie cyklosporyny we krwi Nie badano wpływu tikagreloru na inne substraty P-gp.
Produkty lecznicze metabolizowane przez CYP2C9
Jednoczesne podawanie tikagreloru i tolbutamidu nie powodowało zmiany stężenia żadnego z produktów leczniczych w osoczu, co wskazuje, że tikagrelor nie jest inhibitorem CYP2C9 i jest mało prawdopodobne, aby wpływał na metabolizm produktów leczniczych, takich jak warfaryna i tolbutamid, za pośrednictwem CYP2C9.
Doustne środki antykoncepcyjne
Jednoczesne podawanie tikagreloru i lewonorgestrelu oraz etynyloestradiolu zwiększało ekspozycję na etynyloestradiol o około 20%, ale nie zmieniało profilu farmakokinetycznego lewonorgestrelu. Nie oczekuje się klinicznie istotnego wpływu na skuteczność doustnego środka antykoncepcyjnego po jednoczesnym stosowaniu lewonorgestrelu i etynyloestradiolu oraz tikagreloru.
Leki, o których wiadomo, że wywołują bradykardię
Po zaobserwowaniu w większości bezobjawowych pauz komorowych i bradykardii, należy zachować ostrożność podczas jednoczesnego podawania produktu Brilique z innymi produktami leczniczymi wywołującymi bradykardię (patrz punkt 4.4).Jednak w badaniu PLATO nie zaobserwowano objawów klinicznych działań niepożądanych. z co najmniej jednym produktem leczniczym wywołującym bradykardię (np. 96% beta-adrenolityki, 33% blokery kanału wapniowego diltiazem i werapamil oraz 4% digoksyna).
Inne terapie towarzyszące
W badaniu PLATO Brilique podawano przez długi czas z ASA, inhibitorami pompy protonowej, statynami, beta-blokerami, inhibitorami konwertazy angiotensyny i antagonistami receptora angiotensyny, zgodnie z wymaganiami współistniejących stanów klinicznych, przez długi czas, a także z heparyną drobnocząsteczkową heparyna na masę ciała i krótkotrwałe dożylne inhibitory GpIIb/IIIa (patrz punkt 5.1) Nie zaobserwowano dowodów na klinicznie istotne niepożądane interakcje z tymi produktami leczniczymi.
Jednoczesne podawanie tikagreloru i heparyny, enoksaparyny lub desmopresyny nie ma wpływu na czas częściowej tromboplastyny po aktywacji (aPTT), czas krzepnięcia po aktywacji (ACT) ani na dawki czynnika Xa. Jednak ze względu na potencjalne interakcje farmakodynamiczne należy zachować ostrożność podczas jednoczesnego podawania produktu Brilique z produktami leczniczymi, o których wiadomo, że zaburzają hemostazę.
Po doniesieniach o nieprawidłowych krwawieniach skórnych związanych z SSRI (np. paroksetyną, sertraliną i citalopramem) należy zachować ostrożność podczas podawania SSRI z tikagrelorem, ponieważ może to prowadzić do zwiększonego ryzyka krwawienia.
04.6 Ciąża i laktacja
Kobiety w wieku rozrodczym
Kobiety w wieku rozrodczym muszą stosować odpowiednie środki antykoncepcyjne, aby uniknąć ciąży podczas przyjmowania leku Brilique.
Ciąża
Brak lub ograniczone dane dotyczące stosowania tikagreloru u kobiet w ciąży.
Badania na zwierzętach wykazały szkodliwy wpływ na reprodukcję (patrz punkt 5.3). Brilique nie jest zalecany w okresie ciąży.
Czas karmienia
Dane farmakodynamiczne/toksykologiczne na zwierzętach wykazały przenikanie tikagreloru i jego aktywnych metabolitów do mleka (patrz punkt 5.3).Nie można wykluczyć ryzyka dla noworodków/niemowląt.Należy podjąć decyzję, czy przerwać karmienie piersią czy przerwać karmienie piersią. Terapia Brilique uwzględniająca korzyści z karmienia piersią dla dziecka oraz korzyści z terapii dla matki.
Płodność
Tikagrelor nie ma wpływu na płodność samców ani samic zwierząt (patrz punkt 5.3).
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Brilique nie ma wpływu lub ma nieistotny wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn. Podczas leczenia ostrego zespołu wieńcowego zgłaszano zawroty głowy. Z tego powodu pacjenci, u których występują zawroty głowy, powinni zachować ostrożność podczas prowadzenia pojazdów lub obsługiwania maszyn.
04.8 Działania niepożądane
Podsumowanie profilu bezpieczeństwa
Najczęściej zgłaszanymi działaniami niepożądanymi u pacjentów leczonych tikagrelorem były duszność, stłuczenie i krwawienie z nosa, które występowały częściej niż w grupie klopidogrelu.
Tabela działań niepożądanych
Bezpieczeństwo produktu Brilique u pacjentów z ostrym zespołem wieńcowym (niestabilna dławica piersiowa, NSTEMI i STEMI) oceniano w dużym głównym badaniu III fazy PLATO ([PLATelet hamowanie i pacjent LUBwyniki], 18 624 pacjentów), którzy porównywali pacjentów leczonych produktem Brilique (dawka nasycająca Brilique 180 mg i dawka podtrzymująca 90 mg dwa razy na dobę) z pacjentami leczonymi klopidogrelem (dawka nasycająca 300-600 mg, a następnie 75 mg raz na dobę jako podtrzymująca). dawki), oba podawane w skojarzeniu z kwasem acetylosalicylowym (ASA) i innymi standardowymi terapiami.
Następujące działania niepożądane zostały zidentyfikowane w wyniku badań przeprowadzonych z produktem Brilique lub zostały zgłoszone po wprowadzeniu produktu do obrotu (Tabela 1).
Działania niepożądane są klasyfikowane według częstości występowania i klasyfikacji układów i narządów. Klasy częstości są zdefiniowane zgodnie z następującymi konwencjami: bardzo często (≥1/10), często (≥1/100,
Wiele skorelowanych terminów dotyczących działań niepożądanych pogrupowano w Tabeli e
zawierać terminy medyczne opisane poniżej:
hiperurykemii, zwiększone stężenie kwasu moczowego w surowicy
b krwotok mózgowy, krwotok śródczaszkowy, udar krwotoczny
c duszność, duszność wysiłkowa, duszność spoczynkowa, duszność nocna
d krwotok z przewodu pokarmowego, krwotok z odbytu, krwotok jelitowy, smoliste stolce, krew utajona
krwotok z wrzodów żołądka i żołądka, krwotok z wrzodów żołądka, krwotok z wrzodów dwunastnicy, krwotok z wrzodów trawiennych
f krwiak podskórny, krwotok skórny, krwotok podskórny, wybroczyny
g stłuczenie, krwiak, zasinienie, zwiększona skłonność do siniaków, krwiak pourazowy
h krwiomocz, krew w moczu, krwotok z dróg moczowych
krwotok w miejscu nakłucia, krwiak w miejscu nakłucia naczyniowy, krwotok w miejscu wstrzyknięcia, krwotok w miejscu nakłucia, krwotok w miejscu cewnika
# W badaniu PLATO nie zgłoszono żadnych działań niepożądanych związanych z wylewem krwi do stawów w ramieniu tikagreloru (n = 9235); częstość została obliczona przy użyciu górnej granicy 95% przedziału ufności dla oszacowania punktowego (na podstawie 3 / X, gdzie X reprezentuje całkowitą próbkę, tj. 9235 pacjentów). Oblicza się to jako 3/9 235, co równa się „rzadko " klasa częstotliwości
## Po wprowadzeniu produktu do obrotu zgłaszano przypadki krwotoków śródczaszkowych, które zakończyły się zgonem
Opis wybranych działań niepożądanych
Krwawienie
Ogólne wyniki częstości krwawień w badaniu PLATO przedstawiono w Tabeli 2.
Tabela 2 – Ocena częstości krwawień Kaplana-Meiera jako funkcja leczenia
Definicje kategorii krwawienia:
Poważne krwawienie prowadzące do zgonu/zagrażające życiu: Klinicznie jawne przy obniżeniu stężenia hemoglobiny > 50 g/l lub przetoczeniu ≥ 4 jednostek czerwonych krwinek; lub śmiertelne; lub wewnątrzczaszkowe; o doosierdziowe z tamponadą serca; lub ze wstrząsem hipowolemicznym lub ciężkim niedociśnieniem wymagającym leczenia nadciśnieniowego lub zabiegu chirurgicznego.
Inne Poważne krwawienie: Klinicznie widoczne ze spadkiem stężenia hemoglobiny o 30-50 g/l lub przetoczeniem 2-3 jednostek czerwonych krwinek; lubznacznie wyłączając.
Drobne krwawienie: wymaga interwencji medycznej w celu zatrzymania lub leczenia krwawienia.
Poważne krwawienie wg TIMI: Klinicznie jawne ze obniżoną hemoglobiną > 50 g/l lub krwotokiem śródczaszkowym.
Niewielkie krwawienie wg TIMI: Klinicznie widoczne przy 30-50 g/l spadku stężenia hemoglobiny.
Brilique i klopidogrel nie różniły się w częstości występowania poważnych śmiertelnych/zagrażających życiu krwawień według kryteriów PLATO, poważnych krwawień całkowitych według kryteriów PLATO, poważnych krwawień według skali TIMI lub mniejszych według skali TIMI (tab. 2). Jednak w przypadku tikagreloru wystąpiło więcej połączonych krwawień dużych i mniejszych w skali PLATO niż w przypadku klopidogrelu. Niewielu pacjentów w badaniu PLATO miało śmiertelne krwawienie: 20 (0,2%) dla tikagreloru i 23 (0,3%) dla klopidogrelu (patrz punkt 4.4).
Czynniki takie jak wiek, płeć, masa ciała, rasa, region geograficzny, współistniejący stan fizyczny, równoczesne leczenie i historia choroby, w tym przebyty udar lub przemijający napad niedokrwienny, nie były predyktorami całkowitego lub niezwiązanego z zabiegiem poważnego krwawienia, zdefiniowanego zgodnie z Kryteria Platona. W konsekwencji nie zidentyfikowano żadnej konkretnej grupy zagrożonej określoną kategorią krwawienia.
Krwawienie związane z CABG: W badaniu PLATO 42% z 1584 pacjentów (12% kohorty) poddawanych operacji pomostowania aortalno-wieńcowego (CABG) miało śmiertelne / zagrażające życiu poważne krwawienie zgodnie z kryteriami PLATO, bez różnicy między grupami leczenia. Krwawienie śmiertelne związane z CABG wystąpiło u 6 pacjentów w każdej grupie leczenia (patrz punkt 4.4).
Krwawienie niezwiązane z CABG i krwawienie niezwiązane z żadną procedurą: Brilique i klopidogrel nie różnią się pod względem poważnych śmiertelnych/zagrażających życiu krwawień niezwiązanych z CABG, zdefiniowanych według kryteriów PLATO, podczas gdy całkowite poważne krwawienie według kryteriów PLATO, duże według skali TIMI i duże + małe według skali TIMI. częściej występowały w przypadku tikagreloru. Podobnie w przypadku eliminacji krwawień związanych z zabiegiem, więcej krwawień obserwowano w przypadku tikagreloru niż klopidogrelu (tab. 2). Przerwanie leczenia z powodu krwawienia nieoperacyjnego było częstsze w przypadku tikagreloru (2,9%) niż klopidogrelu (1,2%; p
Krwotoki wewnątrzczaszkowe: Więcej nieoperacyjnych krwawień śródczaszkowych wystąpiło w przypadku tikagreloru (n = 27 krwawień u 26 pacjentów, 0,3%) niż w przypadku klopidogrelu (n = 14 krwawień, 0,2%), w tym 11 krwawień po tikagrelorze i 1 po klopidogrelu zakończyło się zgonem. Nie było różnic w ogólnej liczbie śmiertelnych krwawień.
duszność
U pacjentów leczonych produktem Brilique zgłaszano duszność, uczucie duszności. Zdarzenia niepożądane związane z dusznością (duszność, duszność spoczynkowa, duszność wysiłkowa, napadowa duszność nocna i duszność nocna), jeśli były związane, zgłosiło 13,8% pacjentów leczonych tikagrelorem i 7,8% pacjentów leczonych klopidogrelem. U 2,2% pacjentów przyjmujących tikagrelor i 0,6% pacjentów leczonych klopidogrelem badacze w badaniu PLATO uznali duszność za przyczynowo związaną z leczeniem, a kilka przypadków było ciężkich (0,14% dla tikagreloru; 0,02% dla klopidogrelu) (patrz pkt 4.4). Najczęściej zgłaszane objawy duszności miały nasilenie łagodne do umiarkowanego, a większość zgłaszano jako pojedynczy epizod wkrótce po rozpoczęciu leczenia.
W porównaniu z klopidogrelem, u pacjentów z astmą/POChP leczonych tikagrelorem może występować zwiększone ryzyko wystąpienia nieciężkiej duszności (3,29% dla tikagreloru vs. 0,53% dla klopidogrelu) i ciężkiej duszności (0,38% dla tikagreloru vs. 0,00% dla klopidogrelu). W wartościach bezwzględnych ryzyko to było większe niż w całej populacji objętej badaniem PLATO. Tikagrelor należy stosować ostrożnie u pacjentów z astmą i (lub) POChP w wywiadzie (patrz punkt 4.4).
Około 30% wszystkich epizodów duszności ustąpiło w ciągu 7 dni. Badanie PLATO obejmowało pacjentów z zastoinową niewydolnością serca, przewlekłą obturacyjną chorobą płuc lub astmą na początku badania; ci pacjenci oraz osoby starsze częściej zgłaszały epizody duszności. W grupie Brilique 0,9% pacjentów przerwało stosowanie badanej substancji czynnej z powodu duszności w porównaniu z 0,1% pacjentów otrzymujących klopidogrel. Większa częstość występowania duszności obserwowana podczas stosowania produktu Brilique nie jest związana z wystąpieniem lub pogorszeniem choroby serca lub płuc (patrz punkt 4.4). Brilique nie wpływa na wyniki testów czynnościowych płuc.
Testy diagnostyczne
Zwiększenie stężenia kreatyniny: W badaniu PLATO stężenie kreatyniny w surowicy znacznie wzrosło o ponad 30% u 25,5% pacjentów przyjmujących tikagrelor w porównaniu z 21,3% pacjentów przyjmujących klopidogrel i o ponad 50% u pacjentów przyjmujących tikagrelor.8,3% tikagreloru. pacjentów leczonych klopidogrelem w porównaniu z 6,7% pacjentów leczonych klopidogrelem Wzrost stężenia kreatyniny >50% był bardziej wyraźny u pacjentów w wieku powyżej 75 lat (tikagrelor 13,6% w porównaniu z klopidogrelem 8, 8%), u pacjentów z ciężką niewydolnością nerek na początku badania (tikagrelor 17,8 % w porównaniu z klopidogrelem 12,5%) oraz u pacjentów leczonych jednocześnie antagonistami receptora angiotensyny II (tikagrelor 11,2% w porównaniu z klopidogrelem 7, 1%). W tych podgrupach ciężkie zdarzenia niepożądane dotyczące nerek i zdarzenia niepożądane prowadzące do przerwania leczenia badanym lekiem były podobne w obu grupach leczenia. Całkowita liczba zgłoszonych zdarzeń niepożądanych dotyczących nerek wyniosła 4,9% dla tikagreloru w porównaniu z 3,8% dla klopidogrelu, jednak podobny odsetek pacjentów zgłosił zdarzenia uznane przez badaczy za związane przyczynowo z leczeniem: 54 (0,6%) dla tikagreloru i 43 (0,5%) dla klopidogrel.
Zwiększenie stężenia kwasu moczowego: W badaniu PLATO stężenie kwasu moczowego w surowicy zwiększyło się powyżej górnej granicy normy u 22% pacjentów leczonych tikagrelorem w porównaniu z 13% pacjentów przyjmujących klopidogrel.Średnie stężenie kwasu moczowego w surowicy było zwiększone o około 15% przy tikagreloru w porównaniu do 7,5% w przypadku klopidogrelu i zmniejszył się do około 7% w przypadku tikagreloru po przerwaniu leczenia, podczas gdy nie zaobserwowano zmniejszenia w przypadku klopidogrelu. Zdarzenie niepożądane związane z hiperurykemią zgłoszono u 0,5% dla tikagreloru w porównaniu z 0,2% dla klopidogrelu. Spośród tych zdarzeń niepożądanych, 0,05% dla tikagreloru w porównaniu z 0,02% dla klopidogrelu uznano za związane ze związkiem przyczynowym zależnym od badacza. 0,2% dla tikagreloru wobec 0,1% dla klopidogrelu; żadne z tych działań niepożądanych nie zostało uznane przez badaczy za przyczynowo związane z leczeniem.
Zgłaszanie podejrzewanych działań niepożądanych
Zgłaszanie podejrzewanych działań niepożądanych występujących po dopuszczeniu produktu leczniczego do obrotu jest ważne, ponieważ umożliwia ciągłe monitorowanie stosunku korzyści do ryzyka produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem krajowego systemu zgłaszania. .agenziafarmaco.gov.it/it/responsabili ”.
04.9 Przedawkowanie
Tikagrelor jest dobrze tolerowany w pojedynczych dawkach do 900 mg. Toksyczność żołądkowo-jelitowa ograniczała dawkę w badaniu z eskalacją pojedynczej dawki. Inne klinicznie istotne działania niepożądane, które mogą wystąpić po przedawkowaniu, obejmują duszność i pauzy komorowe (patrz punkt 4.8).
W przypadku przedawkowania mogą wystąpić powyższe potencjalne działania niepożądane i należy rozważyć monitorowanie EKG.
Do chwili obecnej nie jest znane antidotum przeciwdziałające skutkom tikagreloru i zakłada się, że tikagrelor nie podlega dializie (patrz punkt 4.4). Leczenie przedawkowania powinno być zgodne ze standardami lokalnej praktyki medycznej. Oczekiwanym skutkiem podania zbyt dużej dawki leku Brilique jest wydłużenie ryzyka krwawienia związanego z hamowaniem płytek krwi.W przypadku wystąpienia krwawienia należy zastosować odpowiednie leczenie podtrzymujące.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE
05.1 Właściwości farmakodynamiczne
Grupa farmakoterapeutyczna: leki przeciwpłytkowe, z wyłączeniem heparyny.
Kod ATC: B01AC24.
Mechanizm akcji
Brilique zawiera tikagrelor, który należy do chemicznej klasy cyklopentylotriazolopirymidyn
(CPTP), który jest doustnym, bezpośrednim, selektywnym i odwracalnym antagonistą receptora P2Y12 i zapobiega aktywacji i agregacji płytek krwi zależnej od adenozynodifosforanu (ADP).
Tikagrelor nie zapobiega wiązaniu ADP, ale gdy wiąże się z receptorem P2Y12, zapobiega indukowanej przez ADP transdukcji sygnału. Ponieważ płytki krwi odgrywają rolę w powstawaniu i (lub) rozwoju powikłań zakrzepowych miażdżycy, wykazano, że hamowanie czynności płytek zmniejsza ryzyko zdarzeń sercowo-naczyniowych, takich jak zgon, zawał mięśnia sercowego lub udar mózgu.
Tikagrelor zwiększa również lokalne endogenne poziomy adenozyny poprzez hamowanie równowagowego transportera nukleozydów -1 (ENT-1).
Wykazano, że tikagrelor nasila następujące działania indukowane adenozyną u zdrowych osób i pacjentów z OZW: rozszerzenie naczyń (mierzone jako zwiększony przepływ wieńcowy krwi u zdrowych ochotników i pacjentów z OZW; ból głowy), zahamowanie czynności płytek krwi (w pełnej krwi ludzkiej). in vitro) i duszność. Jednak związek między obserwowanym wzrostem adenozyny a wynikami klinicznymi (np. zachorowalność-śmiertelność) nie został wyjaśniony.
Efekty farmakodynamiczne
Początek działania (Początek)
U pacjentów ze stabilną chorobą wieńcową leczonych ASA tikagrelor wywołuje szybki początek działania leku, co wykazano za pomocą średniego „hamowania agregacji płytek krwi (PAH)” dla tikagreloru 0,5 godziny po podaniu dawki nasycającej 180 mg wynoszącej około 41%, z maksymalnym wpływ na PAH wyniósł 89% w ciągu 2-4 godzin po podaniu dawki i utrzymywał się od 2 do 8. 90% pacjentów miało końcowe PAH >70% w ciągu 2 godzin po podaniu.
Odwracalność działania (Offset)
Jeśli planowano operację CABG, ryzyko krwawienia z tikagrelorem jest zwiększone w porównaniu z klopidogrelem, gdy przerwane jest mniej niż 96 godzin przed operacją.
Dane dotyczące zmiany terapii
Zmiana z klopidogrelu na tikagrelor powoduje bezwzględny wzrost PAH o 26,4%, podczas gdy zmiana z tikagreloru na klopidogrel powoduje bezwzględny spadek PAH o 24,5%. Pacjenci mogą zostać przestawieni z klopidogrelu na leczenie tikagrelorem bez przerywania działania przeciwpłytkowego (patrz punkt 4.2).
Skuteczność kliniczna i bezpieczeństwo
Badanie PLATO obejmowało 18 624 pacjentów, którzy zgłosili się w ciągu 24 godzin od wystąpienia objawów niestabilnej dławicy piersiowej (UA), zawału mięśnia sercowego bez uniesienia odcinka ST (NSTEMI) lub zawału mięśnia sercowego z uniesieniem odcinka ST (STEMI) i byli początkowo leczeni. farmakologicznie z przezskórną interwencją wieńcową (PCI) lub pomostowaniem aortalno-wieńcowym (CABG) (patrz punkt 4.1).
Przy tej samej dawce dobowej ASA tikagrelor 90 mg dwa razy na dobę był skuteczniejszy niż klopidogrel 75 mg/dobę w zapobieganiu złożonemu punktowi końcowemu, jakim był zgon z przyczyn sercowo-naczyniowych [CV], zawał mięśnia sercowego [MI] lub udar mózgu, przy czym różnica wynikała ze zmniejszenia zgonów z przyczyn sercowo-naczyniowych i zawału serca Pacjenci otrzymywali albo 300 mg dawkę nasycającą klopidogrelu (dawka 600 mg możliwa do PCI) albo 180 mg tikagreloru.
Wynik uzyskano wcześnie (bezwzględna redukcja ryzyka [ARR] 0,6% i względna redukcja ryzyka [RRR] o 12% po 30 dniach), z efektem leczenia, który utrzymywał się na stałym poziomie przez 12 miesięcy, uzyskując „ARR” 1,9% rocznie oraz RRR wynoszący 16%. Dane te sugerują, że właściwe jest leczenie pacjentów tikagrelorem przez okres do 12 miesięcy (patrz punkt 4.2) Leczenie 54 pacjentów z OZW tikagrelorem zamiast klopidogrelu pozwoliłoby uniknąć wystąpienia 1 zdarzenia zakrzepowego w przebiegu miażdżycy ; leczenie 91 pacjentów pozwoliłoby uniknąć 1 zgonu z przyczyn sercowo-naczyniowych (tab. 3).
Efekt leczenia tikagrelorem w porównaniu z klopidogrelem jest spójny we wszystkich podgrupach pacjentów pod względem cech takich jak masa ciała, płeć, cukrzyca w wywiadzie, przemijający napad niedokrwienny lub udar niekrwotoczny, rewaskularyzacja, jednoczesne terapie, w tym heparyny, inhibitory GpIIb/IIIa i pompa protonowa inhibitorów (patrz punkt 4.5), ostateczne rozpoznanie zdarzenia (STEMI, NSTEMI lub UA) oraz ścieżka leczenia przypisana do randomizacji (inwazyjna lub medyczna).
Zaobserwowano słabo istotną interakcję między leczeniem a regionem geograficznym, przy czym współczynnik ryzyka (HR) dla pierwszorzędowego punktu końcowego faworyzuje tikagrelor w pozostałej części świata, podczas gdy klopidogrel w Ameryce Północnej, który stanowi około 10% globalnego badana populacja (wartość p interakcji = 0,045).
Analizy eksploracyjne wskazują na możliwy związek z dawką ASA, ponieważ zaobserwowano zmniejszoną skuteczność tikagreloru związaną z rosnącymi dawkami ASA.Dobowa przewlekła dawka ASA, podawana razem z produktem Brilique, powinna wynosić od 75 do 150 mg (patrz punkty 4.2 i 4.4). .
Rycina 1 przedstawia szacowane ryzyko pierwszego wystąpienia dowolnego zdarzenia ocenianego w złożonym punkcie końcowym skuteczności.
Brilique zmniejszył wystąpienie pierwszorzędowego złożonego punktu końcowego w porównaniu z klopidogrelem zarówno w populacji UA/NSTEMI, jak i STEMI (tab. 3).
Tabela 3 – Wyniki kliniczne w badaniu PLATO
ARR = bezwzględna redukcja ryzyka; RRR = względna redukcja ryzyka = (1-współczynnik ryzyka) x 100%. Ujemny RRR wskazuje na zwiększone ryzyko względne.
b z wyłączeniem cichego zawału mięśnia sercowego.
c SRI = ciężkie nawracające niedokrwienie; RI = nawracające niedokrwienie; TIA = przejściowy atak niedokrwienny; ATE = zdarzenie miażdżycowe. Całkowity MI obejmuje niemy MI, z datą zdarzenia ustawioną jako data diagnozy.
d wartość istotności nominalnej; wszystkie inne wartości są formalnie istotne statystycznie na podstawie wcześniej zdefiniowanego testu hierarchicznego.
podbadanie Holtera
W celu zbadania początku pauz komorowych i innych epizodów arytmii podczas badania PLATO, badacze przeprowadzili monitorowanie metodą Holtera w podgrupie prawie 3000 pacjentów, z których około 2000 miało dane dotyczące obu ostrych faz zespołu wieńcowego. po miesiącu.Podstawową zmienną będącą przedmiotem zainteresowania był początek pauz komorowych ≥3 sekundy. Pauzy komorowe wystąpiły u większej liczby pacjentów w przypadku tikagreloru (6,0%) niż klopidogrelu (3,5%) w ostrej fazie; oraz odpowiednio 2,2% i 1,6% po 1 miesiącu (patrz punkt 4.4). Zwiększenie pauz komorowych w ostrej fazie OZW było bardziej wyraźne u pacjentów leczonych tikagrelorem z historią CHF (9,2% w porównaniu z 5,4% u pacjentów bez historii CHF; w przypadku pacjentów leczonych klopidogrelem 4, 0% u pacjentów z CHF w wywiadzie w porównaniu z 3,6% u pacjentów bez historii CHF).Tej różnicy nie zaobserwowano po jednym miesiącu: 2,0% w porównaniu z 2,1% odpowiednio u pacjentów leczonych tikagrelorem z i bez historii CHF oraz 3,8% w porównaniu z 1,4% z klopidogrelem W tej populacji pacjentów nie stwierdzono niepożądanych skutków klinicznych związanych z tą różnicą (w tym stosowania stymulatora).
Podbadanie Genetyka badania PLATO
Genotypowanie CYP2C19 i ABCB1 10 285 pacjentów z badania PLATO pozwoliło powiązać wyniki kliniczne badania z rozkładem genotypowym. Na wyższość tikagreloru nad klopidogrelem w ograniczaniu poważnych incydentów sercowo-naczyniowych nie wpływał genotyp CYP2C19 lub ABCB1 pacjenta.Podobnie do ogólnych danych z badania PLATO, częstość występowania poważnych krwawień ogółem według kryteriów PLATO nie różniła się między tikagrelorem i klopidogrelem, niezależnie od genotypu CYP2C19 lub ABCB1. Częstość występowania poważnych krwawień niezwiązanych z CABG PLATO była większa w przypadku tikagreloru w porównaniu z klopidogrelem u pacjentów z jednym lub większą liczbą alleli o obniżonej czynności CYP2C19, ale podobnie jak w przypadku klopidogrelu u pacjentów bez alleli o obniżonej czynności.
Złożone powiązanie skuteczności i bezpieczeństwa
Złożona kombinacja skuteczności i bezpieczeństwa (zgon z przyczyn sercowo-naczyniowych, zawał mięśnia sercowego, udar lub całkowite poważne krwawienie PLATO) wskazuje, że korzyści ze skuteczności produktu Brilique w porównaniu z klopidogrelem nie równoważą zdarzenia związane z dużymi krwawieniami (ARR 1, 4%; RRR 8%; HR 0,92 p = 0,0257) w ciągu 12 miesięcy po NZK.
Populacja pediatryczna
Europejska Agencja Leków uchyliła obowiązek przedstawienia wyników badań produktu Brilique we wszystkich podgrupach populacji pediatrycznej w zatwierdzonym wskazaniu (patrz punkty 4.2 i 5.2).
05.2 Właściwości farmakokinetyczne
Tikagrelor wykazuje liniową farmakokinetykę, a ekspozycja na tikagrelor i aktywny metabolit (AR-C124910XX) jest w przybliżeniu proporcjonalna do dawki do 1260 mg.
Wchłanianie
Wchłanianie tikagreloru jest szybkie, średni t1/2 wynosi około 1,5 h. Tworzenie się głównego krążącego metabolitu, AR-C124910XX (również aktywnego), pochodzącego z tikagreloru, jest szybkie, z t1/2
mediana około 2,5 godziny. Po podaniu doustnym 90 mg tikagreloru na czczo Cmax wynosi 529 ng/ml, a AUC 3451 ng x h/ml Stosunek metabolitów prekursorów wynosi 0,28 dla Cmax i 0,42 dla AUC.
Średnia bezwzględna biodostępność tikagreloru została oszacowana na 36%. Spożycie wysokotłuszczowego posiłku spowodowało 21% wzrost AUC tikagreloru i 22% spadek Cmax aktywnego metabolitu, ale nie miało wpływu na Cmax tikagreloru ani AUC tikagreloru. uważa się, że zmiany mają minimalne znaczenie kliniczne, dlatego tikagrelor można podawać zarówno z posiłkami, jak i bez posiłków. Tikagrelor i jego aktywny metabolit są substratami P-gp.
Tikagrelor w postaci rozkruszonych tabletek zmieszanych z wodą, podawany doustnie lub przez sondę nosowo-żołądkową, ma biodostępność porównywalną do całych tabletek w zakresie AUC i Cmax zarówno tikagreloru, jak i aktywnego metabolitu.Ekspozycja początkowa (0, 5 i 1 godzina po podaniu) dla pokruszonych tabletek tikagreloru zmieszanych w wodzie był wyższy niż dla całych tabletek, z profilem stężenia ogólnie identycznym później (2 do 48 godzin).
Dystrybucja
Objętość dystrybucji tikagreloru w stanie stacjonarnym wynosi 87,5 l. Tikagrelor i jego aktywny metabolit silnie wiążą się z białkami osocza (> 99,0%).
Biotransformacja
CYP3A4 jest głównym enzymem odpowiedzialnym za metabolizm tikagreloru i tworzenie aktywnego metabolitu, a ich interakcje z innymi substratami CYP3A wahają się od aktywacji do hamowania.
Głównym metabolitem tikagreloru jest AR-C124910XX, który również wykazuje aktywność farmakologiczną, jak wykazano in vitro poprzez wiązanie się z płytkowym receptorem P2Y12 ADP Ekspozycja ogólnoustrojowa na aktywny metabolit wynosi około 30-40% ekspozycji obserwowanej w przypadku tikagreloru.
Eliminacja
Główną drogą eliminacji tikagreloru jest metabolizm wątrobowy. Po podaniu tikagreloru znakowanego radioizotopem średni odzysk radioaktywności wynosi około 84% (57,8% w kale, 26,5% w moczu).Odzyskane ilości zarówno tikagreloru, jak i aktywnego metabolitu obecnego w moczu stanowiły mniej niż 1% dawka.
Główną drogą eliminacji aktywnego metabolitu jest prawdopodobnie wydzielanie z żółcią. Średni t1/2 wynosił około 7 godzin dla tikagreloru i 8,5 godziny dla aktywnego metabolitu.
Populacje specjalne
Starsi mieszkańcy
Większą ekspozycję na tikagrelor (około 25% zarówno dla Cmax, jak i AUC) oraz na aktywny metabolit obserwowano u pacjentów w podeszłym wieku (≥75 lat) z OZW w porównaniu z młodszymi pacjentami, na podstawie „analizy farmakokinetyki populacyjnej”. ).
Populacja pediatryczna
Tikagrelor nie był oceniany w populacji dzieci i młodzieży (patrz punkty 4.2 i 5.1).
Seks
Większą ekspozycję tikagreloru i aktywnego metabolitu obserwowano u kobiet niż u mężczyzn. Różnice te nie są uważane za istotne klinicznie.
Upośledzona czynność nerek
Ekspozycja na tikagrelor była o około 20% mniejsza, a ekspozycja na aktywny metabolit była o około 17% większa u pacjentów z ciężkimi zaburzeniami czynności nerek (klirens kreatyniny).
Upośledzona czynność wątroby
Cmax i AUC tikagreloru były o 12% i 23% większe u pacjentów z łagodnymi zaburzeniami czynności wątroby w porównaniu z porównywalną próbą zdrowych osób (patrz punkt 4.2). Tikagrelor nie był badany u pacjentów z umiarkowanymi lub ciężkimi zaburzeniami czynności wątroby i jego stosowanie u tych pacjentów jest przeciwwskazane (patrz punkty 4.3 i 4.4).
Pochodzenie etniczne
Pacjenci pochodzenia azjatyckiego wykazują średnią biodostępność, która jest o 39% wyższa niż pacjenci rasy kaukaskiej. Pacjenci zidentyfikowani jako czarni mieli o 18% niższą biodostępność tikagreloru niż pacjenci rasy kaukaskiej. W badaniach farmakologii klinicznej ekspozycja (Cmax i AUC) na tikagrelor u pacjentów z Japonii była o około 40% (20% po dostosowaniu do masy ciała) większa niż u pacjentów rasy kaukaskiej.
05.3 Przedkliniczne dane o bezpieczeństwie
Dane przedkliniczne dotyczące tikagreloru i jego głównego metabolitu nie wykazały niedopuszczalnego ryzyka wystąpienia działań niepożądanych u ludzi na podstawie konwencjonalnych badań farmakologicznych dotyczących bezpieczeństwa, toksyczności po podaniu jednorazowym lub wielokrotnym oraz potencjału genotoksycznego.
Podrażnienie przewodu pokarmowego zaobserwowano u kilku gatunków zwierząt dla klinicznie istotnych poziomów narażenia (patrz punkt 4.8).
U samic szczurów tikagrelor w dużych dawkach wykazywał zwiększoną częstość występowania guzów macicy (gruczolakoraków) oraz zwiększoną częstość występowania gruczolaków wątroby. Mechanizm powstawania guzów macicy jest prawdopodobnie związany z brakiem równowagi hormonalnej, która może prowadzić do powstania guza u szczurów. Mechanizm leżący u podstaw powstawania gruczolaków wątroby jest prawdopodobnie spowodowany indukcją enzymów wątrobowych specyficznych dla gryzonia. W związku z tym uważa się, że obserwacje dotyczące potencjału rakotwórczego mają mało prawdopodobne znaczenie dla ludzi.
Niewielkie nieprawidłowości rozwojowe zaobserwowano u szczurów po podaniu dawki toksycznej dla matek (margines bezpieczeństwa 5,1). U królików zaobserwowano niewielkie opóźnienie dojrzewania wątroby i rozwoju szkieletu u płodów matek narażonych na duże dawki, bez objawów toksyczności matczynej (margines bezpieczeństwa 4,5).
Badania na szczurach i królikach wykazały toksyczny wpływ na reprodukcję, z niewielkim zmniejszeniem przyrostu masy ciała matki, zmniejszoną żywotnością noworodków i zmniejszeniem masy urodzeniowej z opóźnieniem wzrostu Tikagrelor powodował nieregularne cykle (głównie dłuższe cykle) u samic szczurów, ale nie wpływał na ogólny płodność samców i samic szczurów Badania farmakokinetyczne przeprowadzone z tikagrelorem znakowanym radioizotopem wykazały, że związek macierzysty i jego metabolity przenikają do mleka szczurów (patrz punkt 4.6).
06.0 INFORMACJE FARMACEUTYCZNE
06.1 Zaróbki
Rdzeń tabletu
Mannitol (E421)
Dihydrat wodorofosforanu wapnia
Stearynian magnezu (E470b)
Glikolan sodu skrobi
Hydroksypropyloceluloza (E463)
Powłoka tabletu
Talk
Dwutlenek tytanu (E171)
Żółty tlenek żelaza (E172)
Glikol polietylenowy 400
Hypromeloza (E464)
06.2 Niekompatybilność
Nieistotne.
06.3 Okres ważności
3 lata.
06.4 Specjalne środki ostrożności przy przechowywaniu
Ten produkt leczniczy nie wymaga żadnych specjalnych warunków przechowywania.
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania
• Przezroczysty blister (z symbolami słońca / księżyca) z PVC-PVDC/Al zawierający 10 tabletek; kartony zawierające 60 tabletek (6 blistrów) i 180 tabletek (18 blistrów).
• Przezroczysty blister kalendarzowy (z symbolami słońca / księżyca) w PVC-PVDC/Al zawierający 14 tabletek; kartony zawierające 14 tabletek (1 blister), 56 tabletek (4 blistry) i 168 tabletek (12 blistrów).
• Przezroczysty blister perforowany jednodawkowy z PVC-PVDC/Al zawierający 10 tabletek; kartony po 100x1 tabletek (10 blistrów).
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
06.6 Instrukcje użytkowania i obsługi
Brak specjalnych instrukcji.
07.0 PODMIOT POZWOLENIA NA DOPUSZCZENIE DO OBROTU
AstraZeneca AB
SE-151 85
Södertälje
Szwecja
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
UE / 1/10/655 / 001-006
040546018
040546020
040546032
040546044
040546057
040546069
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA
Data pierwszego zezwolenia: 03 grudnia 2010 r.
Data ostatniego przedłużenia: 17 lipca 2015 r.
10.0 DATA ZMIAN TEKSTU
Lipiec 2015





















.jpg)





