Składniki aktywne: Diflukortolon
TEMETEX 3 mg/g krem hydrofobowy
Ulotki do opakowań Temetex są dostępne dla wielkości opakowań:- TEMETEX 1 mg/g krem hydrofilowy
- TEMETEX 1 mg/g krem hydrofobowy
- TEMETEX 3 mg/g krem hydrofobowy
Wskazania Dlaczego stosuje się Temetex? Po co to jest?
Temetex zawiera substancję czynną diflukortolon, która należy do klasy leków kortykosteroidowych do stosowania miejscowego. Jest wskazany w leczeniu niektórych zapalnych i alergicznych chorób skóry, takich jak wyprysk kontaktowy, kontaktowe zapalenie skóry (alergiczne lub toksyczne z natury, takie jak nadwrażliwość na detergenty lub inne środki chemiczne), wyprysk wulgarny (faza ostra i przewlekła), wyprysk drobnoustrojowy, dermoepidermitis , wyprysk łojotokowy, wyprysk żylaków (jednak nie bezpośrednio na wrzodzie), wyprysk dziecięcy, wyprysk odbytu.
Przeciwwskazania Kiedy nie należy stosować Temetexu
Nie używaj Temetexu:
- Jeśli pacjent ma uczulenie na substancję czynną lub którykolwiek z pozostałych składników tego leku
- W przypadku występowania na leczonym obszarze wtórnych zmian skórnych, takich jak szczepienie, gruźlica, zakażenia grzybicze, bakteryjne lub wirusowe (opryszczka, ospa wietrzna itp.), trądzik różowaty i owrzodzenia skóry. Preparat nie jest przeznaczony do stosowania okulistycznego.
Środki ostrożności dotyczące stosowania Informacje ważne przed przyjęciem leku Temetex
W chorobach skóry, którym towarzyszą infekcje bakteryjne, wskazane jest skojarzenie leczenia z chemioterapią do stosowania miejscowego; w przypadku grzybicy (zakażenia grzybiczego) potrzebne są miejscowe leki przeciwgrzybicze.
Temetex nie jest wskazany do leczenia chorób oczu. Temetexu nie należy nakładać na oczy. W przypadku aplikacji produktu na twarz należy unikać kontaktu produktu z oczami. Stosowanie na skórę kortykosteroidów w leczeniu dermatoz (choroby skóry) przedłużone i/lub długotrwałe, może determinować wtórne zjawiska wchłaniania ogólnoustrojowego, a tym samym determinować początek zaburzeń hormonalnych (zespół Cushinga, zahamowanie osi podwzgórza -przysadka). Zjawisko to występuje częściej u dzieci oraz w przypadku opatrunku okluzyjnego.
W „stosowaniu pediatrycznym fałdy skórne i pielucha mogą działać jak bandaż okluzyjny. Dlatego w leczeniu chorób przewlekłych wymagających długotrwałej terapii, jeśli osiągnięto korzystny efekt terapeutyczny, wskazane będzie zmniejszenie dawki i częstotliwości aplikacji do niezbędnego minimum w celu opanowania objawów i uniknięcia nawrotów poprzez jak najszybsze zaprzestanie stosowania preparatu.
W trakcie terapii konieczne jest monitorowanie stanu pacjenta w celu wykrycia wczesnych oznak i objawów nadmiaru steroidów (astenia (zmęczenie), nadciśnienie tętnicze, zaburzenia elektrolitowe (zmiana ilości niektórych minerałów we krwi itp.) W przypadkach zaleca się ograniczenie stosowania steroidów miejscowych (tj. do stosowania miejscowego) do krótkich okresów czasu.
Dzieci
U niemowląt i dzieci poniżej czwartego roku życia nie zaleca się leczenia przez okres dłuższy niż trzy tygodnie, zwłaszcza w miejscach zakrytych pieluchami. (Patrz „Ostrzeżenia i środki ostrożności”).
Interakcje Jakie leki lub pokarmy mogą zmienić działanie Temetexu
Należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent stosuje, ostatnio stosował lub może stosować jakiekolwiek inne leki.
Nie są znane możliwe interakcje i niezgodności z innymi lekami.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
W chorobach skóry, którym towarzyszą infekcje bakteryjne, wskazane jest skojarzenie leczenia z chemioterapią miejscową; w przypadku grzybicy konieczne są miejscowe leki przeciwgrzybicze. Temetex nie jest wskazany do leczenia chorób oczu. Temetexu nie należy nakładać na oczy. W przypadku aplikacji produktu na twarz należy unikać kontaktu produktu z oczami. Skórne stosowanie kortykosteroidów w leczeniu rozległych dermatoz i/lub przez długi czas może determinować wtórne zjawisko wchłaniania ogólnoustrojowego, które występuje częściej u dzieci oraz w przypadku opatrunków okluzyjnych. pielucha może pełnić funkcję opatrunku okluzyjnego. Dlatego w leczeniu chorób przewlekłych, które wymagają przedłużonej terapii, w przypadku uzyskania korzystnego efektu terapeutycznego, wskazane będzie zmniejszenie dawki i częstotliwości aplikacji do minimum niezbędnego do opanowania objawów i uniknięcia nawrotów, wstrzymanie stosowania możliwie jak najszybciej.W trakcie terapii należy monitorować stan pacjenta, aby wykryć wczesne oznaki i objawy nadmiaru steroidów (astenia, nadciśnienie, zaburzenia elektrolitowe itp.) We wszystkich przypadkach wskazane jest ograniczenie stosowanie miejscowych sterydów przez krótkie okresy czasu.
Dzieci
Ten lek nie jest zalecany dla niemowląt i dzieci w wieku poniżej czterech lat (patrz „Ostrzeżenia i środki ostrożności”).
Ciąża i karmienie piersią
Jeśli pacjentka jest w ciąży lub karmi piersią, podejrzewa, że może być w ciąży lub planuje mieć dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem tego leku.
Miejscowe podawanie kortykosteroidów ciężarnym zwierzętom laboratoryjnym może powodować pojawienie się wad rozwojowych płodu.Nie wykazano możliwości przeniesienia tych danych na ludzi. Ogólnie rzecz biorąc, w przypadku preparatów miejscowych (tj. do stosowania miejscowego) zawierających kortykosteroidy, takich jak Temetex, nie zaleca się stosowania w pierwszym trymestrze ciąży.
W szczególności należy unikać nakładania produktu na duże obszary skóry lub przez dłuższy czas.
U kobiet w ciąży Temetex należy stosować tylko wtedy, gdy jest to bezwzględnie konieczne i pod bezpośrednim nadzorem lekarza.
Prowadzenie i używanie maszyn
Temetex nie wpływa na zdolność prowadzenia pojazdów i obsługiwania maszyn.
Ważne informacje o zaróbkach
Ten produkt leczniczy zawiera p-hydroksybenzoesan metylu i p-hydroksybenzoesan propylu, które mogą powodować reakcje alergiczne (w tym opóźnione).
Dawka, sposób i czas podawania Jak stosować Temetex: dawkowanie
Ten lek należy zawsze stosować zgodnie z zaleceniami lekarza lub farmaceuty. W razie wątpliwości skonsultuj się z lekarzem lub farmaceutą.O ile nie zalecono inaczej, kurację należy rozpocząć od rozprowadzania preparatu cienką warstwą 2-3 razy dziennie. Ta dawka powinna być obserwowana przez okres 1-2 tygodni, podczas których na ogół obserwuje się znaczące wyniki kliniczne. Gdy tylko obraz kliniczny ulegnie poprawie, wystarczy ograniczyć podawanie do jednej dziennej aplikacji lub przestawić się na analogiczny lek o niższym stężeniu (Temetex 0,1% krem hydrofobowy).
W szczególnie opornych przypadkach lekarz może przepisać leczenie pod bandażem okluzyjnym. Nie zaleca się jednak jego stosowania na dużej powierzchni ciała. Jeśli podczas zabiegu wystąpią procesy zakaźne skóry, przez pewien czas konieczne będzie nie nakładanie bandaża okluzyjnego. W przypadku rozległych zmian wskazane jest leczenie małych obszarów sukcesywnie, pojedynczo.
Dzięki swojemu szczególnemu składowi (niskotłuszczowa emulsja „olej w wodzie”) Temetex zapewnia odpowiednie natłuszczenie skóry, nie blokując transpiracji i wymiany ciepła. Dzięki temu znajduje zastosowanie zarówno w chorobach skóry, które nie są nadmiernie wydzielające, jak i tych, które nie są szczególnie suche.
Używaj u dzieci
U niemowląt i dzieci poniżej 4 roku życia nie zaleca się leczenia przez okres dłuższy niż trzy tygodnie, zwłaszcza w miejscach zakrytych pieluchami.
Pominięcie zastosowania leku Temetex
Nie należy stosować dawki podwójnej w celu uzupełnienia pominiętej dawki.
Przerwanie stosowania leku Temetex
W przypadku dalszych pytań dotyczących stosowania tego leku należy zwrócić się do lekarza lub farmaceuty.
Przedawkowanie Co zrobić w przypadku przyjęcia zbyt dużej dawki leku Temetex
W przypadku przypadkowego połknięcia/przyjmowania przedawkowania leku Temetex należy natychmiast powiadomić lekarza lub udać się do najbliższego szpitala. Nie są znane przypadki przedawkowania.
Skutki Uboczne Jakie są skutki uboczne Temetexu?
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią. Działania niepożądane, które mogą wystąpić podczas stosowania tego leku obejmują:
Miejscowe zaczerwienienie, obrzęk (obrzęk), łuszczenie (utrata górnej warstwy skóry), swędzenie jako objawy nadwrażliwości na lek. Inne skutki obejmują nadmierne owłosienie (wzrost owłosienia), wykwity trądzikopodobne (podobne do trądziku), atrofię skóry (zmniejszenie objętości skóry), hipopigmentację (zmniejszenie koloru skóry), teleangiektazje (poszerzenie drobnych naczyń krwionośnych widocznych pod skórą) , rozstępy, kruchość naczyń, plamica (czerwonawe zabarwienie skóry spowodowane małymi wylewami krwi z naczyń włosowatych).
Po długotrwałych kuracjach (zwłaszcza na twarzy) nawracające krostkowe zapalenie skóry (objawy skórne przypominające pęcherzyki, które pojawiają się po odstawieniu leku), które ze względu na wrażliwość na steroidy, takie jak Temetex, ujawniają się dopiero po odstawieniu terapii.
Podczas leczenia dużych obszarów skóry (około 10% i więcej powierzchni ciała) i/lub długotrwałego stosowania (ponad 4 tygodnie), zwłaszcza pod opatrunkiem okluzyjnym, jak w przypadku wszystkich innych miejscowych kortyzonów, towarzyszą następujące reakcje: zanik skóry ( utrata górnej warstwy skóry), teleangiektazje (rozszerzenie drobnych naczyń krwionośnych widocznych pod skórą), rozstępy, objawy trądzikopodobne (podobne do „trądziku”), okołoustne zapalenie skóry (stan zapalny skóry wokół ust), zwiększony wzrost owłosienia ciała (nadmierne owłosienie).
Objawy ogólnoustrojowe (tj. mogące objawiać się w całym organizmie, na przykład zaburzeniami hormonalnymi) wynikające z wchłaniania kortykosteroidów przez skórę. W zabiegach okluzyjnych należy pamiętać, że folie użyte do opatrunku same mogą powodować zjawiska uczuleniowe. Stosowanie, zwłaszcza długotrwałe, produktów do stosowania miejscowego może wywołać zjawisko uczulenia.W takim przypadku konieczne jest przerwanie leczenia i wdrożenie odpowiedniej terapii.
U osób predysponowanych mogą wystąpić reakcje nadwrażliwości.
Przestrzeganie instrukcji zawartych w ulotce dołączonej do opakowania zmniejsza ryzyko wystąpienia działań niepożądanych.
Zgłaszanie skutków ubocznych
Jeśli wystąpią jakiekolwiek działania niepożądane, należy porozmawiać z lekarzem, w tym wszelkie możliwe działania niepożądane niewymienione w tej ulotce. Działania niepożądane można również zgłaszać bezpośrednio za pośrednictwem krajowego systemu zgłaszania pod adresem: www.agenziafarmaco.it/it/responsabili Zgłaszanie działań niepożądanych może pomóc w uzyskaniu dodatkowych informacji na temat bezpieczeństwa stosowania tego leku.
Wygaśnięcie i przechowywanie
Temetex nie wymaga żadnych specjalnych środków ostrożności podczas przechowywania. Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na opakowaniu po EXP Termin ważności oznacza ostatni dzień podanego miesiąca Termin ważności oznacza nieotwarty, prawidłowo przechowywany produkt Nie stosować tego leku, jeśli jest znany. widoczne oznaki pogorszenia.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa, co pomoże chronić środowisko.
Inne informacje
Co zawiera lek Temetex
100 g kremu zawiera:
Składnik aktywny: walerianian diflukortolonu 0,3 g.
Pozostałe składniki: biały wosk pszczeli, parafina ciekła, biała wazelina, dehymuls® E, woda oczyszczona.
Opis wyglądu leku Temetex i co zawiera opakowanie
Temetex 3 mg/g hydrofobowy krem jest dostępny w 20 g tubie zawierającej biały lub lekko żółtawy krem.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO
TEMETEX
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY
Temetex 0,1% krem hydrofilowy. 100 g zawiera: walerianian diflukortolonu 0,1 g.
Temetex 0,1% krem hydrofobowy. 100 g zawiera: walerianian diflukortolonu 0,1 g.
Temetex 0,1% maść. 100 g zawiera: walerianian diflukortolonu 0,1 g.
Temetex 0,1% roztwór na skórę. 100 g zawiera: walerianian diflukortolonu 0,1 g.
Zaróbki, patrz 6.1.
03.0 POSTAĆ FARMACEUTYCZNA
Temetex 0,1% jest dostępny w postaci kremu hydrofilowego, kremu hydrofobowego, maści i roztworu do stosowania na skórę.
04.0 INFORMACJE KLINICZNE
04.1 Wskazania terapeutyczne
Temetex 0,1% krem hydrofilowy:
Wyprysk kontaktowy, kontaktowe zapalenie skóry (o etiologii alergicznej lub toksycznej, np. nadwrażliwość na detergenty lub inne środki chemiczne), wyprysk wulgarny (faza ostra i przewlekła), wyprysk mikrobiologiczny, dermoepidermitis, wyprysk łojotokowy, wyprysk żylaków (jednak nie bezpośrednio na wrzodzie), wyprysk dziecięcy, wyprysk odbytu, trądzik różowaty.
Temetex 0,1% krem hydrofobowy:
Zapalenie skóry i wyprysk kontaktowy, wyprysk zawodowy, wyprysk wulgarny, wyprysk pieniążkowaty (drobnoustrojowy), wyprysk żylaków (jednak nie bezpośrednio na wrzodzie), wyprysk niemowlęcy, wyprysk odbytu, neurodermit, oparzenia pierwszego stopnia, rumień słoneczny, ukąszenia owadów, rumień skórny, łuszczyca , liszaj ruber płaski i brodawkowaty.
Temetex 0,1% maść:
Neurodermatitis, egzema vulgaris (faza przewlekła), egzema mikrobiologiczna (sucha), wyprysk liszajowaty, łuszczyca, liszaj płaski płaski i brodawkowaty
Temetex 0,1% roztwór na skórę:
Miejscowe leczenie dermatoz wrażliwych na kortykosteroidy, szczególnie skóry głowy (łupież zwykły, potocznie zwany łupieżem, parakeratoza łojotokowa, łuszczyca, neurodermit, liszaj płaski, przewlekły rumieniowaty krążkowy) oraz ucha zewnętrznego (egzema, łuszczyca przewodu słuchowego) .
04.2 Dawkowanie i sposób podawania
O ile nie zalecono inaczej, kurację należy rozpocząć od rozprowadzania preparatu cienką warstwą 2-3 razy dziennie. Temetex 0,1% roztwór na skórę należy początkowo nakładać dwa razy dziennie na leczony obszar, lekko masując. Gdy tylko obraz kliniczny się poprawi, wystarczy jedna aplikacja dziennie.
Temetex 0,1% występuje w czterech różnych postaciach farmaceutycznych dobieranych w zależności od wyglądu i lokalizacji zmiany skórnej Temetex 0,1% roztwór na skórę jest szczególnie wskazany w dermatozach skóry głowy i ucha zewnętrznego. Temetex 0,1% hydrofilowy krem, ze względu na szczególnie niskotłuszczową zaróbkę (emulsję „olej w wodzie”), jest szczególnie wskazany w leczeniu zmian wydzielniczych i wilgotnych obszarów skóry, takich jak okolice odbytu i jamy pachowe, gdzie jest to wskazane. użyj bazy o dużej zawartości wody. Temetex 0,1% krem hydrofilowy umożliwia przepływ wydzieliny i powoduje szybkie wysięk i wysuszenie skóry. Preparat nie pozostawia śladów tłuszczu na skórze i dlatego nadaje się również do stosowania na twarz i nieosłonięte partie skóry.Temetex 0,1% krem hydrofobowy, ze względu na swoją szczególną substancję pomocniczą (baza tłuszczowa zawierająca niewielką ilość wody) ma bardzo szeroki możliwości stosowania od chorób skóry, które nie są nadmiernie wydzielające, po te, które nie są szczególnie suche.Preparat zapewnia odpowiednie natłuszczenie skóry, nie blokując potu i wymiany ciepła.Temetex 0,1% maść, ze względu na całkowicie tłustą bazę jest szczególnie wskazane w postaciach suchych oraz w stadiach przewlekłych, w których wymagane jest stosowanie preparatów bezwodnych. Temetex 0,1% maść utrzymuje wilgotność skóry i z tego powodu zmiękcza zgrubiałą warstwę rogową naskórka ułatwiając wnikanie składnika aktywnego Baza maści działa okluzywnie i dlatego generalnie nie wymaga opatrunku okluzyjnego. W szczególnych przypadkach opornych na terapię lekarz może przepisać leczenie pod opatrunkiem okluzyjnym. Chore miejsce na skórze poddane działaniu preparatu zostanie pokryte warstwą nieprzepuszczalnego materiału, który należy przykleić do otaczającej zdrowej skóry. Czas stosowania bandaża okluzyjnego ustala lekarz, ale nie może przekraczać dwóch dni, aby uniknąć ewentualnych zaburzeń homeostazy. W razie potrzeby opatrunek okluzyjny można powtórzyć kilka razy. Jeśli podczas leczenia wystąpią procesy zakaźne, przez pewien czas konieczne będzie nie stosowanie bandaży okluzyjnych. W przypadku rozległych zmian wskazane jest jednak, aby kolejno leczyć częściowe obszary pojedynczo.
Jeżeli po leczeniu Temetex 0,1% roztworem na skórę nastąpi znaczne wysuszenie skóry, wskazane jest przejście na „stosowanie” innej postaci farmaceutycznej (Temetex 0,1% krem hydrofilowy, hydrofobowy krem lub maść).
04.3 Przeciwwskazania
Znana nadwrażliwość na składniki. Infekcje gruźlicze i wirusowe leczonej skóry (opryszczka, ospa wietrzna itp.). Trądzik różowaty. Owrzodzenia skóry. Preparat nie jest przeznaczony do stosowania okulistycznego.
Opatrunek okluzyjny jest przeciwwskazany w przypadku zmian wysiękowych i infekcji skóry.
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania
W chorobach skóry, którym towarzyszą infekcje bakteryjne, wskazane jest skojarzenie leczenia z chemioterapią miejscową; w przypadku grzybicy konieczne są miejscowe leki przeciwgrzybicze.
Temetex 0,1% nie jest wskazany do leczenia chorób oczu.
Przezskórne stosowanie kortykosteroidów w leczeniu rozległych dermatoz i/lub przez długi czas może determinować wtórne zjawiska wchłaniania ogólnoustrojowego (zespół Cushinga, zahamowanie osi podwzgórzowo-przysadkowej). Zjawisko to występuje częściej u dzieci oraz w przypadku opatrunku okluzyjnego. W „stosowaniu pediatrycznym fałdy skórne i pielucha mogą działać jak bandaż okluzyjny. Dlatego w leczeniu chorób przewlekłych wymagających długotrwałej terapii, jeśli osiągnięto korzystny efekt terapeutyczny, wskazane będzie zmniejszenie dawki i częstotliwości aplikacji do niezbędnego minimum, w celu opanowania objawów i uniknięcia nawrotów, jak najszybciej zaprzestając stosowania preparatu.
W trakcie terapii konieczne jest monitorowanie stanu pacjenta w celu wykrycia wczesnych oznak i objawów nadmiaru steroidów (astenia, nadciśnienie, zaburzenia elektrolitowe itp.). We wszystkich przypadkach wskazane jest ograniczenie stosowania miejscowych sterydów do krótkich okresów czasu.
Niemowlęta i dzieci poniżej czwartego roku życia nie powinny być leczone dłużej niż trzy tygodnie, zwłaszcza w miejscach, w których są pieluszki.
Leków nie należy przechowywać w zasięgu dzieci.
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji
Nie są znane możliwe interakcje i niezgodności leków.
04.6 Ciąża i laktacja
Miejscowe stosowanie kortykosteroidów u ciężarnych zwierząt laboratoryjnych może powodować pojawienie się wad rozwojowych płodu.Nie wykazano możliwości przeniesienia tego objawu na ludzi.Jednak w pierwszych trzech miesiącach ciąży preparaty kortykosteroidów do stosowania miejscowego nie powinny być stosowane w dużych ilościach ani przez długo i ogólnie u kobiet w ciąży oraz w bardzo wczesnym dzieciństwie preparat należy stosować tylko w przypadku rzeczywistej potrzeby i pod bezpośrednim nadzorem lekarza.
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Temetex 0,1% nie wpływa na zdolność prowadzenia pojazdów i obsługi niektórych maszyn.
04.8 Działania niepożądane
Miejscowe zaczerwienienie, obrzęk, łuszczenie, swędzenie jako objawy nadwrażliwości na produkt. Inne objawy to nadmierne owłosienie, wykwity trądzikopodobne, atrofia skóry, hipopigmentacja, teleangiektazje, rozstępy, kruchość naczyń, plamica i po długotrwałym leczeniu (zwłaszcza na twarzy) nawracające krostkowe zapalenie skóry, które jako wrażliwe na steroidy ujawnia się dopiero po przerwaniu terapii. Długotrwałe i/lub stosowanie dużych dawek może wywołać zespół nadmiaru z nadciśnieniem tętniczym, osłabieniem, adynamią, zaburzeniami rytmu serca, hipokaliemią i zasadowicą metaboliczną.
W zabiegach okluzyjnych należy pamiętać, że folie użyte do opatrunku same mogą powodować zjawiska uczuleniowe.
Stosowanie, zwłaszcza długotrwałe, produktów do stosowania miejscowego może wywołać zjawisko uczulenia.W takim przypadku konieczne jest przerwanie leczenia i wdrożenie odpowiedniej terapii.
U osób predysponowanych mogą wystąpić reakcje nadwrażliwości.
04.9 Przedawkowanie
Nie są znane przypadki przedawkowania.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE
05.1 Właściwości farmakodynamiczne
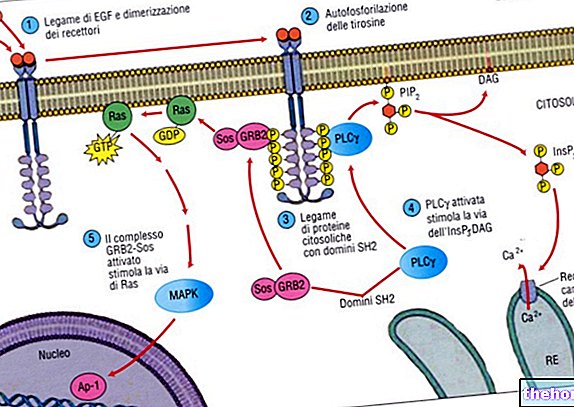
Walerianian diflukortolonu (DFV) jest kortykosteroidem do stosowania miejscowego o działaniu przeciwzapalnym, przeciwświądowym i zwężającym naczynia. Kortykosteroidy łagodzą stany zapalne za pomocą różnych mechanizmów, szczególnie poprzez promowanie syntezy czynnika (lipokortyny), który kontroluje enzym (fosfolipazę A2), który aktywuje kaskadę kwasu arachidonowego, prowadząc do powstawania czynników flogenicznych, takich jak prostaglandyny i nadtlenki lipolityczne.
DFV wykazuje 3 do 30 razy wyższą aktywność przeciwzapalną niż inne porównawcze kortykosteroidy do stosowania miejscowego i 10 razy wyższą aktywność antyproliferacyjną niż flukortolon.
05.2 Właściwości farmakokinetyczne
Po nałożeniu na skórę kortykosteroidy są w dużej mierze zatrzymywane przez warstwę rogową naskórka i tylko niewielka część dociera do skóry właściwej, gdzie mogą zostać wchłonięte. Wiele czynników może sprzyjać bardziej widocznej absorpcji: obszar i rozszerzenie skóry, która ma być leczona, rodzaj zmiany, czas trwania zabiegu, ewentualny bandaż okluzyjny. W związku z tym należy pamiętać, że niektóre obszary skóry (twarz, powieki, włosy, moszna) wchłaniają je łatwiej niż inne (skóra kolan, łokci, dłoni i podeszew stóp).
DFV szybko penetruje ludzki naskórek, osiągając maksymalne stężenie w ciągu 4 godzin od aplikacji. Stężenie to przeważa w bardziej powierzchownych warstwach skóry. Wchłanianie ogólnoustrojowe po 7 godzinach stosowania wynosi mniej niż 1% dawki początkowej. Niewielka ilość wchłonięta do krążenia jest szybko metabolizowana (okres półtrwania w osoczu około 4 godzin) do co najmniej trzech substancji rozkładających, które są szybko i całkowicie eliminowane przez nerki w postaci sprzężonej. W moczu zidentyfikowano 7 metabolitów DFV.
Metabolizm śródskórny DFV po podaniu na skórę człowieka polega na powolnej hydrolizie substancji do diflukortolonu i kwasu walerianowego (5-15% dawki podawanej przez 7 godzin).
05.3 Przedkliniczne dane o bezpieczeństwie
Toksykologia:
Toksyczność ostra DFV jest znikoma (LD50 per os u myszy > 4 g/kg). Testy przeprowadzone przy stosowaniu miejscowym w stężeniach równych 0,5% potwierdziły brak możliwej do określenia toksyczności ostrej.Tylko po długotrwałym stosowaniu u psów przez 14 tygodni preparatów w stężeniu 0,1% w dawce 100 mg/kg/dobę tak działa ogólnoustrojowe zamanifestowane.
06.0 INFORMACJE FARMACEUTYCZNE
06.1 Zaróbki
Temetex 0,1% krem hydrofilowy:
monostearynian glikolu polietylenowego, alkohol stearylowy, parafina ciekła, wazelina biała, wersenian sodu, karbomer, wodorotlenek sodu, parahydroksybenzoesan metylu, parahydroksybenzoesan propylu, woda oczyszczona.
Temetex 0,1% krem hydrofobowy:
wosk biały, parafina ciekła, wazelina biała, dehymuls E, woda oczyszczona.
Temetex 0,1% maść:
parafina ciekła, wazelina biała, lunacera M, uwodorniony olej rycynowy.
Temetex 0,1% roztwór na skórę:
alkohol, glicerol, poliwinylopirolidon, woda oczyszczona.
06.2 Niekompatybilność
Do tej pory nie są znane żadne konkretne niezgodności.
06.3 Okres ważności
Wygaśnięcie nieotwartego opakowania prawidłowo przechowywanego:
Krem hydrofilowy, krem hydrofobowy, maść: 5 lat.
Roztwór do skóry: 3 lata.
06.4 Specjalne środki ostrożności przy przechowywaniu
Brak specjalnych środków ostrożności przy przechowywaniu.
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania
Temetex 0,1% krem hydrofilowy, Temetex 0,1% krem hydrofobowy, Temetex 0,1% maść:
Elastyczna tuba aluminiowa wewnętrznie zabezpieczona lakierem i zamknięta plastikową zakrętką.
Temetex 0,1% roztwór na skórę:
Butelka szklana, zamykana nakrętką polietylenową; dozownik z zakrętką, umieszczony w torebce polietylenowej, do nałożenia na butelkę przy pierwszym użyciu.
Poszczególne pojemniki są zamknięte w odpowiednim kartonowym pudełku wraz z ilustracyjną ulotką.
06.6 Instrukcje użytkowania i obsługi
Brak specjalnych instrukcji.
07.0 PODMIOT POZWOLENIA NA DOPUSZCZENIE DO OBROTU
Teofarma S.r.l. - Via F.lli Cervi, 8 - 27010 Valle Salimbene (PV)
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
Tuba "0,1% krem hydrofilowy" 30g AIC nr 023682089
Tuba "0,1% krem hydrofobowy" 30g AIC nr 023682026
Tuba "0,1% maść" 30g AIC nr 023682053
Butelka „0.1% roztwór na skórę” 30 ml AIC nr 023682103
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA
Odnowienie: czerwiec 2005
10.0 DATA ZMIAN TEKSTU
01/03/2005