Struktura i funkcje
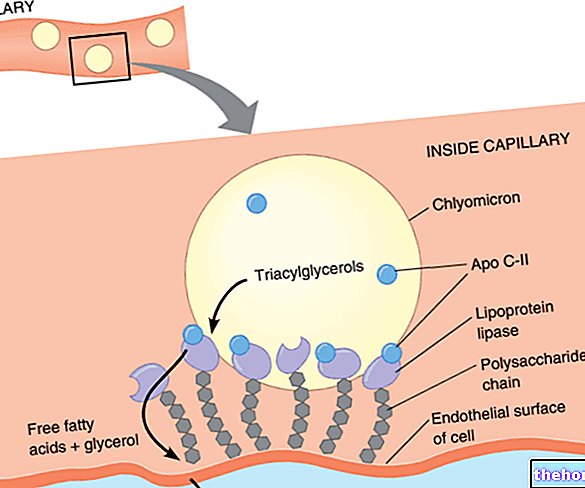
Hemoglobina jest metaloproteiną zawartą w czerwonych krwinkach, odpowiedzialną za transport tlenu w krwiobiegu.W rzeczywistości tlen jest tylko umiarkowanie rozpuszczalny w wodzie; dlatego ilości rozpuszczone we krwi (mniej niż 2% całości) nie są wystarczające do zaspokojenia metabolicznego zapotrzebowania tkanek. Potrzeba konkretnego przewoźnika jest więc oczywista.
W krwiobiegu tlen nie może wiązać się bezpośrednio i odwracalnie z białkami, tak jak ma to miejsce w przypadku metali takich jak miedź i żelazo. grupa EME, z metalicznym sercem reprezentowanym przez atom żelaza w stanie utlenienia Fe2+ (stan zredukowany), który wiąże tlen w sposób odwracalny.
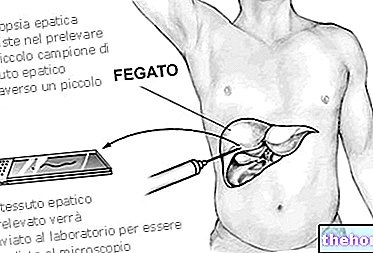
Analiza krwi
- Prawidłowe wartości hemoglobiny we krwi: 13-17 g/100 ml
U kobiet wartości są średnio o 5-10% niższe niż u mężczyzn.
Możliwe przyczyny wysokiego stężenia hemoglobiny
- Czerwienice
- Dłuższy pobyt na wzniesieniu
- Przewlekłe choroby płuc
- Choroba serca
- Doping krwi (stosowanie erytropoetyny i pochodnych lub substancji naśladujących ich działanie)
Możliwe przyczyny niskiego poziomu hemoglobiny
- Anemie
- Niedobór żelaza (niedobór żelaza)
- Obfite krwawienie
- Raki
- Ciąża
- Talasemie
- Oparzenia
Zawartość tlenu we krwi jest zatem podawana przez zsumowanie niewielkiej ilości rozpuszczonej w plazmie z frakcją związaną z żelazem hemoglobiny.
Ponad 98% tlenu obecnego we krwi wiąże się z hemoglobiną, która z kolei krąży w krwiobiegu rozlokowanym w czerwonych krwinkach.Dlatego bez hemoglobiny erytrocyty nie mogłyby spełniać swojego zadania jako transportery tlenu we krwi.
Biorąc pod uwagę centralną rolę tego metalu, synteza hemoglobiny wymaga odpowiedniego spożycia żelaza w diecie. Około 70% żelaza obecnego w organizmie jest w rzeczywistości zawarte w grupach hemowych hemoglobiny.
Hemoglobina składa się z 4 podjednostek strukturalnie bardzo podobnych do mioglobiny*.
* Podczas gdy hemoglobina transportuje tlen z płuc do tkanek, mioglobina przenosi tlen uwalniany przez hemoglobinę do różnych organelli komórkowych, które go używają (np. mitochondriów).

Hemoglobina jest dużą i złożoną metaloproteiną, charakteryzującą się czterema kulistymi łańcuchami białkowymi odpowiednio owiniętymi wokół grupy hemu zawierającej Fe2+.
Dla każdej cząsteczki hemoglobiny znajdujemy zatem cztery grupy hemowe owinięte we względny globularny łańcuch białkowy. Ponieważ w każdej cząsteczce hemoglobiny są cztery atomy żelaza, każda cząsteczka hemoglobiny może związać ze sobą cztery atomy tlenu, zgodnie z odwracalną reakcją:
Hb + 4O2 ← → Hb (O2) 4
Jak wiadomo, zadaniem hemoglobiny jest pobieranie tlenu z płuc, uwalnianie go do komórek, które go potrzebują, pobieranie z nich dwutlenku węgla i uwalnianie go do płuc, gdzie chilo zaczyna się ponownie.
Podczas przepływu krwi w naczyniach włosowatych pęcherzyków płucnych hemoglobina wiąże ze sobą tlen, który następnie uwalnia się do tkanek w krążeniu obwodowym. Wymiana ta zachodzi, ponieważ wiązania tlenu z żelazem grupy EME są nietrwałe i wrażliwe na wiele czynników, z których najważniejszym jest napięcie lub ciśnienie cząstkowe tlenu.
Wiązanie tlenu do hemoglobiny i efekt Bohra
W płucach ciśnienie tlenu w osoczu wzrasta z powodu dyfuzji gazu z pęcherzyków do krwi (↑ PO2); ten wzrost powoduje, że hemoglobina chciwie wiąże się z tlenem; odwrotnie występuje w tkankach obwodowych, gdzie stężenie rozpuszczonego tlenu we krwi spada (↓ PO2), a ciśnienie parcjalne dwutlenku węgla wzrasta (↑ CO2); powoduje to, że hemoglobina uwalnia tlen i zostaje naładowana CO2. im więcej dwutlenku węgla jest we krwi, tym mniej tlenu pozostaje w hemoglobinie.
Chociaż ilość tlenu fizycznie rozpuszczonego we krwi jest bardzo niska, odgrywa zatem fundamentalną rolę. W rzeczywistości ilość ta silnie wpływa na siłę wiązania między tlenem a hemoglobiną (jak również stanowi „ważną wartość referencyjną w regulacji wentylacji płuc”).
Podsumowując wszystko na wykresie, ilość tlenu związanego z hemoglobiną rośnie w stosunku do pO2 zgodnie z krzywą sigmoidalną:

Fakt, że obszar plateu jest tak duży, zapewnia istotny margines bezpieczeństwa przy maksymalnym wysyceniu hemoglobiny podczas przechodzenia do płuc.Chociaż pO2 na poziomie pęcherzykowym zwykle wynosi 100 mm Hg, obserwując liczbę, w rzeczywistości zauważamy, jak nawet przy ciśnieniu parcjalnym tlenu równym 70 mmHg (typowe występowanie niektórych chorób lub przebywanie na dużych wysokościach), procenty nasyconej hemoglobiny pozostają bliskie 100%.
W obszarze maksymalnego nachylenia, gdy ciśnienie cząstkowe tlenu spada poniżej 40 mmHg, zdolność hemoglobiny do wiązania tlenu nagle spada.
W warunkach spoczynkowych PO2 w płynach wewnątrzkomórkowych wynosi około 40 mmHg; w tym miejscu, dzięki prawom gazów, rozpuszczony w plazmie tlen dyfunduje w kierunku biedniejszych tkanek O2, przechodząc przez błonę kapilarną, co powoduje dalsze obniżenie napięcia plazmy O2, co sprzyja uwalnianiu tlenu z hemoglobiny. . Z drugiej strony podczas intensywnego wysiłku fizycznego ciśnienie tlenu w tkankach spada do 15 mmHg lub mniej, w wyniku czego krew jest mocno uszczuplona w tlen.
Z tego, co zostało powiedziane, w warunkach spoczynku znaczna ilość utlenowanej hemoglobiny opuszcza tkanki, pozostając dostępną w razie potrzeby (na przykład, aby poradzić sobie z nagłym wzrostem metabolizmu w niektórych komórkach).
Linia ciągła pokazana na powyższym obrazku nazywana jest krzywą dysocjacji hemoglobiny; typowo oznacza się ją in vitro przy pH 7,4 i w temperaturze 37 ° C.
Efekt Bohra ma wpływ zarówno na pobór O2 na poziomie płuc, jak i na jego uwalnianie na poziomie tkanek.
Tam, gdzie jest więcej rozpuszczonego dwutlenku węgla w postaci wodorowęglanu, hemoglobina łatwiej uwalnia tlen i zostaje naładowana dwutlenkiem węgla (w postaci wodorowęglanu).

Ten sam efekt uzyskuje się poprzez zakwaszenie krwi: im bardziej spada pH krwi i tym mniej tlenu pozostaje w hemoglobinie, nic dziwnego, że we krwi rozpuszcza się dwutlenek węgla głównie w postaci kwasu węglowego, który ulega dysocjacji.



Na cześć odkrywcy wpływ pH lub dwutlenku węgla na dysocjację tlenu jest znany jako efekt Bohra.
Zgodnie z przewidywaniami, w środowisku kwaśnym hemoglobina łatwiej uwalnia tlen, podczas gdy w środowisku podstawowym wiązanie z tlenem jest silniejsze.

Inne czynniki zdolne do modyfikowania powinowactwa hemoglobiny do tlenu obejmują temperaturę. W szczególności powinowactwo hemoglobiny do tlenu zmniejsza się wraz ze wzrostem temperatury ciała. Jest to szczególnie korzystne w miesiącach zimowych i wiosennych, ponieważ temperatura krwi płucnej (w kontakcie z powietrze środowiska zewnętrznego) jest niższe niż osiągane w tkankach, dzięki czemu uwalnianie tlenu jest ułatwione.

2,3 difosfoglicerynian jest półproduktem w glikolizie, który wpływa na powinowactwo hemoglobiny do tlenu.Jeśli jego stężenie w krwinkach czerwonych wzrasta, powinowactwo hemoglobiny do tlenu zmniejsza się, co ułatwia uwalnianie tlenu do tkanek. Nic dziwnego, że stężenie erytrocytów wzrostu 2,3 difosfoglicerynian np. w anemii, niewydolności krążeniowo-oddechowej oraz podczas pobytu na dużej wysokości.
Ogólnie rzecz biorąc, działanie 2,3 bisfosfoglicerynianu jest stosunkowo powolne, zwłaszcza w porównaniu z szybką reakcją na zmiany pH, temperatury i ciśnienia cząstkowego dwutlenku węgla.

Efekt Bohra jest bardzo ważny podczas intensywnej pracy mięśni, w takich warunkach faktycznie w tkankach najbardziej narażonych na stres dochodzi do lokalnego wzrostu temperatury i ciśnienia dwutlenku węgla, a więc i kwasowości krwi. Jak wyjaśniono powyżej, wszystko to sprzyja uwalnianiu tlenu do tkanek, przesuwając krzywą dysocjacji hemoglobiny w prawo.