Składniki aktywne: Atomoksetyna
Strattera 10, 18, 25, 40, 60, 80 i 100 mg kapsułki twarde
Ulotki informacyjne Strattera są dostępne dla wielkości opakowań:- Strattera 10, 18, 25, 40, 60, 80 i 100 mg kapsułki twarde
- Strattera 4 mg/ml roztwór doustny
Dlaczego stosuje się Strattera? Po co to jest?
Po co to jest
Strattera zawiera atomoksetynę i jest stosowany w leczeniu zespołu nadpobudliwości psychoruchowej z deficytem uwagi (ADHD).
- u dzieci powyżej 6 roku życia
- u młodych ludzi
- u dorosłych.
Jest stosowany tylko jako część ogólnego leczenia chorób, które wymaga również interwencji nielekowych, takich jak terapia wspomagająca psychologiczna i behawioralna.
Nie należy go stosować w leczeniu ADHD u dzieci poniżej 6 roku życia, ponieważ nie wiadomo, czy lek ten działa lub jest bezpieczny u tych osób.
U dorosłych Strattera stosuje się w leczeniu ADHD, gdy objawy są bardzo rozpraszające i wpływają na pracę lub życie towarzyskie oraz gdy objawy choroby występowały w dzieciństwie.
Jak to działa
Strattera zwiększa poziom noradrenaliny w mózgu. Norepinefryna jest naturalnie wytwarzaną substancją chemiczną, która zwiększa czujność i zmniejsza impulsywność i nadpobudliwość u pacjentów z ADHD.Lek ten został przepisany, aby pomóc kontrolować objawy ADHD. Ten lek nie jest środkiem pobudzającym i dlatego nie uzależnia. Całkowite złagodzenie objawów może potrwać kilka tygodni po rozpoczęciu leczenia tym lekiem.
O ADHD
Dzieci i młodzież z ADHD znajdują:
- trudno stać w miejscu e
- trudno się skoncentrować.
To nie ich wina, że nie mogą robić tych rzeczy. Wiele dzieci i młodych ludzi stara się to robić. Jednak z ADHD mogą mieć problemy z codziennym życiem, a dzieci i młodzież z ADHD mogą mieć trudności w nauce i odrabianiu lekcji. Walczą o dobre wyniki w domu, w szkole lub gdzie indziej. ADHD nie wpływa na inteligencję dziecka lub młodej osoby.
Dorośli z ADHD mają trudności z robieniem tych wszystkich rzeczy, które sprawiają trudności dzieciom; jednak może to prowadzić do problemów z:
- Praca
- Relacje interpersonalne
- niska samo ocena
- Edukacja
Przeciwwskazania Kiedy nie należy stosować produktu Strattera
NIE WOLNO przyjmować leku Strattera, jeśli:
- jeśli pacjent ma uczulenie (nadwrażliwość) na atomoksetynę lub którykolwiek z pozostałych składników leku Strattera;
- przyjmowali lek znany jako inhibitor monoaminooksydazy (IMAO), taki jak fenelzyna, w ciągu ostatnich dwóch tygodni. Lek MAOI jest czasami stosowany w leczeniu depresji i innych zaburzeń psychicznych; Jeśli pacjent przyjmuje Strattera razem z lekiem IMAO, mogą wystąpić poważne lub zagrażające życiu działania niepożądane. Należy również odczekać co najmniej 14 dni po zaprzestaniu leczenia lekiem Strattera przed rozpoczęciem przyjmowania leku IMAO.
- masz chorobę oczu zwaną jaskrą z wąskim kątem przesączania (podwyższone ciśnienie w oku)
- u pacjenta występują poważne problemy z sercem, na które może wpływać przyspieszenie akcji serca i (lub) ciśnienie krwi, ponieważ może to być skutkiem działania leku Strattera
- u pacjenta występują poważne problemy z naczyniami krwionośnymi w mózgu, takie jak udar, obrzęk lub osłabienie części naczynia krwionośnego (tętniak) lub zwężenie lub zablokowanie naczyń krwionośnych
- mieć guza nadnercza (guz chromochłonny).
Nie należy przyjmować leku Strattera, jeśli którykolwiek z powyższych stanów dotyczy pacjenta. W razie wątpliwości należy porozmawiać z lekarzem lub farmaceutą przed przyjęciem leku Strattera. Dzieje się tak, ponieważ Strattera może pogorszyć te problemy.
Środki ostrożności dotyczące stosowania Informacje ważne przed zastosowaniem leku Strattera
O poniższych ostrzeżeniach i środkach ostrożności należy poinformować zarówno dorosłych, jak i dzieci. Przed rozpoczęciem leczenia lekiem Strattera należy poinformować lekarza, jeśli u pacjenta występuje:
- myśli samobójcze lub próby samobójcze
- problemy z sercem (w tym wady serca) lub przyspieszenie akcji serca. Strattera może zwiększyć częstość bicia serca (pulsu). U pacjentów z wadami serca zgłaszano nagły zgon
- wysokie ciśnienie krwi. Strattera może zwiększać ciśnienie krwi
- niskie ciśnienie krwi. Strattera może powodować zawroty głowy lub omdlenia u osób z niskim ciśnieniem krwi
- problemy z nagłymi zmianami ciśnienia krwi lub częstości akcji serca
- choroba sercowo-naczyniowa lub przebyty udar mózgu
- problemy z wątrobą. Może być potrzebna mniejsza dawka
- objawy psychotyczne, w tym halucynacje (takie jak słyszenie głosów lub widzenie rzeczy, których nie ma), wiara w rzeczy, które nie są prawdziwe lub podejrzliwość
- mania (uczucie podekscytowania lub nadmiernego podekscytowania nietypowym zachowaniem) i pobudzenie
- agresja
- nieprzyjazne i gniewne uczucia (wrogość)
- historia padaczki lub napadów padaczkowych z jakiegokolwiek innego powodu. Strattera może wywoływać wzrost częstości napadów
- inne nastroje niż zwykle (wahania nastroju) lub uczucie bardzo nieszczęśliwego
- trudności w kontrolowaniu siebie, powtarzające się skurcze niektórych części ciała lub powtarzanie dźwięków i słów.
Przed rozpoczęciem leczenia należy skontaktować się z lekarzem lub farmaceutą, jeśli którakolwiek z powyższych sytuacji dotyczy pacjenta. Dzieje się tak, ponieważ Strattera może pogorszyć te problemy. Twój lekarz będzie chciał sprawdzić, jak lek działa na Ciebie.
Przed rozpoczęciem stosowania leku Strattera należy skonsultować się z lekarzem
Te kontrole służą do określenia, czy Strattera jest odpowiednim lekiem dla Ciebie.
Twój lekarz zmierzy je:
- ciśnienie krwi i tętno (tętno) przed i podczas przyjmowania leku Strattera;
- wzrost i wagę, jeśli pacjent jest dzieckiem lub nastolatkiem podczas przyjmowania leku Strattera.
Twój lekarz porozmawia z Tobą:
- wszelkie inne przyjmowane leki
- czy istnieje jakaś rodzinna historia niewyjaśnionej nagłej śmierci
- wszelkie inne problemy zdrowotne (takie jak problemy z sercem), które możesz mieć Ty lub Twoja rodzina.
Ważne jest, aby podać jak najwięcej informacji.Pomoże to lekarzowi zdecydować, czy Strattera jest odpowiednim lekiem dla pacjenta.Twój lekarz może zdecydować, że przed rozpoczęciem stosowania tego leku potrzebne są inne badania lekarskie.
Interakcje Jakie leki lub pokarmy mogą zmienić działanie leku Strattera?
Należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent przyjmuje lub ostatnio przyjmował lub planuje przyjmować jakiekolwiek inne leki, w tym leki wydawane bez recepty. Lekarz zadecyduje, czy można przyjmować Strattera z tymi innymi lekami, aw niektórych przypadkach może być konieczne dostosowanie dawki lub znacznie wolniejsze jej zwiększanie.
Nie należy przyjmować leku Strattera z lekami zwanymi MAO (inhibitory monoaminooksydazy) stosowanymi w depresji. Patrz punkt 2 „Kiedy nie stosować leku Strattera”.
Jeśli pacjent przyjmuje inne leki, Strattera może wpływać na ich działanie lub powodować działania niepożądane. Jeśli pacjent przyjmuje którykolwiek z poniższych leków, przed zastosowaniem leku Strattera należy skonsultować się z lekarzem lub farmaceutą:
- leki podnoszące ciśnienie krwi lub stosowane do kontrolowania ciśnienia krwi
- leki takie jak leki przeciwdepresyjne, np. imipramina, wenlafaksyna, mirtazapina, fluoksetyna i paroksetyna
- niektóre leki na kaszel i przeziębienie, które zawierają leki, które mogą wpływać na ciśnienie krwi. Przy zakupie któregokolwiek z tych produktów należy skonsultować się z farmaceutą
- niektóre leki stosowane w leczeniu zaburzeń psychicznych
- leki, o których wiadomo, że zwiększają ryzyko drgawek
- niektóre leki, w przypadku których Strattera pozostaje w organizmie dłużej niż zwykle (takie jak chinidyna i terbinafina)
- salbutamol (lek przeciwastmatyczny), który przyjmowany doustnie lub we wstrzyknięciach może powodować szybsze bicie serca, ale nie jest to związane z pogorszeniem astmy.
Leki wymienione poniżej mogą powodować zwiększone ryzyko nieprawidłowego rytmu serca, jeśli są przyjmowane z lekiem Strattera:
- leki stosowane do kontrolowania rytmu serca
- leki zmieniające stężenie soli we krwi
- leki do zapobiegania i leczenia malarii
- niektóre antybiotyki (takie jak erytromycyna i moksyfloksacyna).
W przypadku wątpliwości, czy którykolwiek z przyjmowanych leków znajduje się na powyższej liście, przed zastosowaniem leku Strattera należy zwrócić się do lekarza lub farmaceuty.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
Ciąża, karmienie piersią i płodność
Nie wiadomo, czy Strattera może wpływać na nienarodzone dziecko lub czy przenika do mleka matki.
- Strattera nie należy stosować w okresie ciąży, chyba że zaleci to lekarz.
- Należy również unikać przyjmowania leku Strattera podczas karmienia piersią lub zaprzestać karmienia piersią.
Samego siebie:
- jesteś w ciąży lub karmisz piersią
- podejrzewasz, że jesteś w ciąży lub planujesz zajść w ciążę
- planować karmienie piersią, przed zastosowaniem leku Strattera należy zasięgnąć porady lekarza lub farmaceuty.
Prowadzenie i używanie maszyn
Po przyjęciu leku Strattera możesz odczuwać zmęczenie, senność lub zawroty głowy. Należy zachować ostrożność podczas prowadzenia pojazdów i obsługi maszyn do momentu poznania wpływu leku Strattera na zdolności.W przypadku uczucia zmęczenia, senności lub zawrotów głowy nie należy prowadzić pojazdów ani obsługiwać żadnych niebezpiecznych maszyn.
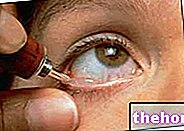
Ważne informacje o zawartości kapsułek
Nie otwierać kapsułek Strattera, ponieważ zawartość kapsułki może podrażniać oczy. W przypadku kontaktu zawartości kapsułek z oczami, chore oko należy natychmiast przemyć wodą i zasięgnąć porady lekarskiej Ręce i inne części ciała, które mogły mieć kontakt z zawartością kapsułek, należy umyć się tak szybko, jak to możliwe.
Dawka, sposób i czas podawania Jak stosować Strattera: dawkowanie
- Strattera należy zawsze przyjmować zgodnie z zaleceniami lekarza. Zazwyczaj przyjmuje się go raz lub dwa razy dziennie (pierwsza dawka rano, druga późnym popołudniem lub wczesnym wieczorem).
- Jeśli pacjent przyjmuje Strattera raz na dobę i odczuwa senność i nudności, lekarz może zmienić lek na dwa razy na dobę.
- Kapsułki należy połykać w całości, niezależnie od posiłków.
- Kapsułek nie wolno otwierać ani wyjmować wewnętrznej zawartości kapsułek i pobierać w inny sposób.
- Przyjmowanie leku o tej samej porze każdego dnia może pomóc pamiętać o jego zażywaniu.
Ile wziąć
Dzieci lub młodzież (w wieku 6 lat lub starsza): Lekarz zaleci dawkę leku Strattera i obliczy dawkę na podstawie masy ciała. Zwykle zacznie zmniejszać dawkę przed zwiększeniem dawki Strattera, którą należy przyjmować w zależności od masy ciała.
- Masa ciała do 70 kg: początkowa całkowita dawka dobowa 0,5 mg na kg masy ciała przez co najmniej 7 dni. Lekarz może wówczas zdecydować o zwiększeniu dawki do zwykłej dawki podtrzymującej wynoszącej 1,2 mg na kg masy ciała na dobę.
- Masa ciała powyżej 70 kg: początkowa całkowita dawka dobowa 40 mg przez co najmniej 7 dni. Lekarz może wówczas zdecydować o zwiększeniu dawki do zwykłej dawki podtrzymującej 80 mg na dobę. Maksymalna dawka dobowa przepisana przez lekarza wynosi 100 mg.
Dorośli ludzie
- Strattera należy rozpocząć od całkowitej dawki dobowej 40 mg przez co najmniej 7 dni. Lekarz może wówczas zdecydować o zwiększeniu dawki do zwykłej dawki podtrzymującej 80-100 mg na dobę. Maksymalna dawka dobowa przepisana przez lekarza wynosi 100 mg.
W przypadku problemów z wątrobą lekarz może przepisać mniejszą dawkę.
Leczenie długoterminowe
Strattera nie musi być zażywana w nieskończoność. Jeśli pacjent przyjmuje Strattera przez ponad rok, lekarz ponownie oceni leczenie, aby sprawdzić, czy lek jest nadal potrzebny.
W przypadku dalszych pytań dotyczących stosowania tego leku należy zwrócić się do lekarza lub farmaceuty.
Pominięcie przyjęcia leku Strattera
W przypadku pominięcia dawki leku Strattera, należy ją przyjąć tak szybko, jak to możliwe, ale nie należy przyjmować więcej niż całkowitą dawkę dobową w ciągu 24 godzin.Nie należy stosować dawki podwójnej w celu uzupełnienia pominiętych dawek.
Przerwanie stosowania Strattera
W przypadku przerwania stosowania leku Strattera zwykle nie wystąpią żadne działania niepożądane, ale objawy ADHD mogą powrócić.Przed przerwaniem leczenia należy porozmawiać z lekarzem.
Przedawkowanie Co zrobić w przypadku przyjęcia zbyt dużej dawki leku Strattera
W przypadku przyjęcia większej niż zalecana dawki leku Strattera, należy natychmiast skontaktować się z lekarzem lub oddziałem ratunkowym najbliższego szpitala i poinformować o liczbie przyjętych kapsułek Najczęściej zgłaszanymi objawami przedawkowania są objawy żołądkowo-jelitowe, senność, zawroty głowy, drżenie i nieprawidłowe zachowanie.
Skutki uboczne Jakie są skutki uboczne Strattera
Jak każdy lek, Strattera może powodować działania niepożądane, chociaż nie u każdego one wystąpią. Chociaż niektórzy ludzie mają skutki uboczne, większość uważa, że Strattera może pomóc. Lekarz omówi z pacjentem te działania niepożądane.
Możliwe efekty uboczne
- Skutki uboczne to niepożądane rzeczy, które mogą się zdarzyć po zażyciu leku. Jeśli wystąpi którykolwiek z poniższych skutków ubocznych, natychmiast porozmawiaj z zaufaną osobą dorosłą. Następnie omówi to z lekarzem. Główne rzeczy, które mogą się zdarzyć, to:
- Twoje serce bije szybciej niż normalnie
- Być bardzo przygnębionym i nieszczęśliwym lub chcąc zrobić sobie krzywdę
- Czuję się agresywny
- Poczucie nieszczęścia lub inny nastrój niż zwykle (wahania nastroju)
- Wykazywać objawy reakcji alergicznej, takie jak „wysypka, swędzenie lub pokrzywka, obrzęk twarzy, warg, języka lub innych części ciała, duszność, świszczący oddech lub trudności w oddychaniu
- Drgawki
- Widzenie, odczuwanie lub słyszenie rzeczy, których inni ludzie nie widzą, nie czują ani nie słyszą
- Uszkodzenie wątroby: ból brzucha, który boli przy uciskaniu (tkliwość) po prawej stronie tuż pod żebrami
Ponieważ lek może powodować senność, ważne jest, aby nie uprawiać sportów na świeżym powietrzu, takich jak jazda konna lub jazda na rowerze, pływanie lub wspinanie się na drzewa.
Niektóre skutki uboczne mogą być poważne. W przypadku wystąpienia któregokolwiek z wymienionych poniżej działań niepożądanych należy natychmiast skontaktować się z lekarzem.
Niezbyt często (dotyczy mniej niż 1 na 100 osób)
- uczucie lub przyspieszone bicie serca, zmiany rytmu serca
- myśli lub uczucia samobójcze
- agresja
- nieprzyjazne i gniewne uczucia (wrogość)
- wahania lub zmiany nastroju
- ciężka reakcja alergiczna z objawami:
- obrzęk twarzy i języka
- problemy z oddychaniem
- pokrzywka (małe, wypukłe, swędzące plamy na skórze)
- konwulsje
- objawy psychotyczne, w tym halucynacje (takie jak słyszenie głosów lub widzenie rzeczy, których nie ma), wiara w rzeczy, które nie są prawdziwe lub podejrzliwość.
Dzieci i młodzież w wieku poniżej 18 lat mają zwiększone ryzyko wystąpienia działań niepożądanych (dotyczących mniej niż 1 na 100 osób) działań niepożądanych, takich jak:
- myśli lub uczucia samobójcze (mogą dotyczyć do 1 na 100 osób)
- zmiany nastroju lub huśtawki (mogą dotyczyć do 1 na 10 osób)
Dorośli mają zmniejszone ryzyko wystąpienia działań niepożądanych (dotyczących mniej niż 1 na 10 000 osób), takich jak:
- konwulsje
- objawy psychotyczne, w tym halucynacje (takie jak słyszenie głosów lub widzenie rzeczy, których nie ma), wiara w rzeczy, które nie są prawdziwe lub podejrzliwość.
Rzadko (dotyczy mniej niż 1 na 1000 osób)
- uszkodzenie wątroby
Należy przerwać przyjmowanie leku Strattera i natychmiast skontaktować się z lekarzem, jeśli wystąpi którykolwiek z następujących objawów:
- ciemny mocz
- zażółcenie skóry lub oczu
- ból brzucha, który boli przy uciskaniu prawej strony brzucha tuż pod żebrami
- niewyjaśnione uczucie mdłości (nudności)
- zmęczenie
- swędzenie
- uczucie grypy.
Inne zgłoszone działania niepożądane wymieniono poniżej. Jeśli się pogorszą, skontaktuj się z lekarzem lub farmaceutą.
- bół głowy
- ból w żołądku (brzuch)
- zmniejszony apetyt (brak głodu)
- mdłości (nudności) lub
- być chorym (wymiotować)
- senność
- podwyższone ciśnienie krwi
- zwiększona częstość akcji serca (pulsacja).
- mdłości
- suchość w ustach
- bół głowy
- zmniejszony apetyt (brak głodu)
- problemy z zasypianiem, zasypianiem i wczesnym wstawaniem
- podwyższone ciśnienie krwi
- zwiększone tętno (puls)
- bycie drażliwym lub poruszonym
- zaburzenia snu, w tym wczesne przebudzenie
- depresja
- uczucie smutku lub beznadziejności
- czuć się niespokojnie
- tik
- rozszerzenie źrenic (czarny środek oka)
- zawroty głowy
- zaparcie
- utrata apetytu
- ból brzucha, niestrawność
- obrzęk, zaczerwienienie i swędzenie skóry – wysypka
- uczucie ospałości (ospałość)
- ból w klatce piersiowej
- zmęczenie
- utrata wagi.
- czuję się wzburzony
- zmniejszone pożądanie seksualne
- zaburzenia snu
- depresja
- uczucie smutku lub beznadziejności
- czuć się niespokojnie
- zawroty głowy
- „anomalia lub zmiana smaku, która nie zniknie”.
- drżenie
- mrowienie lub drętwienie dłoni lub stóp
- senność, sen, uczucie zmęczenia
- zaparcie
- ból brzucha
- niestrawność
- powietrze w jelicie (wzdęcia)
- On wymiotował
- uderzenia gorąca lub zaczerwienienia
- czuć lub mieć bardzo szybkie bicie serca
- obrzęk, zaczerwienienie i swędzenie skóry
- zwiększona potliwość
- wysypka
- problemy z oddawaniem moczu, takie jak niemożność oddania moczu, częste oddawanie moczu lub początkowe trudności z oddawaniem moczu, ból w oddawaniu moczu
- zapalenie gruczołu krokowego (zapalenie gruczołu krokowego)
- ból pachwiny u mężczyzn
- niemożność uzyskania „erekcji
- opóźnienie w orgazmie
- trudności w utrzymaniu erekcji
- skurcze menstruacyjne
- brak siły lub energii
- zmęczenie
- uczucie ospałości (ospałość)
- dreszcze
- wrażliwość, drażliwość, nerwowość
- uczucie pragnienia
- utrata wagi
- półomdlały
- drżenie
- migrena
- nieprawidłowe odczucia skórne, takie jak pieczenie, kłucie, swędzenie lub mrowienie
- mrowienie lub drętwienie dłoni lub stóp
- konwulsje
- uczucie przyspieszonego bicia serca (wydłużenie odstępu QT)
- świszczący oddech
- zwiększona potliwość
- swędząca skóra
- brak siły lub energii.
- niepokój
- tik
- półomdlały
- migrena
- zmieniony rytm serca (wydłużenie odstępu QT)
- uczucie zimna w palcach rąk i nóg
- ból w klatce piersiowej
- świszczący oddech
- swędząca czerwona wysypka (pokrzywka)
- skurcze mięśni
- Zachęcam do oddania moczu
- nieobecny lub nieprawidłowy orgazm
- nieregularne miesiączki
- niezdolność do wytrysku.
- słabe krążenie krwi, które powoduje drętwienie i bladość palców rąk i nóg (zespół Raynauda)
- problemy z oddawaniem moczu, takie jak częste oddawanie moczu lub trudności z rozpoczęciem oddawania moczu, ból podczas oddawania moczu;
- przedłużone i bolesne erekcje
- ból pachwiny u mężczyzn.
- słabe krążenie krwi, które powoduje drętwienie i bladość palców rąk i nóg (zespół Raynauda)
- przedłużone i bolesne erekcje.
Wpływ na wzrost
Niektóre dzieci zgłaszały zmniejszony wzrost (masy i wzrostu) po rozpoczęciu przyjmowania leku Strattera. Jednak w przypadku długotrwałego leczenia dzieci odzyskują wagę i wzrost przewidziany dla wieku.Lekarz będzie monitorował wagę i wzrost dziecka w okresie leczenia. Jeśli dziecko nie rośnie lub nie przybiera na wadze zgodnie z oczekiwaniami, lekarz może podjąć decyzję o zmianie dawki lub czasowym przerwaniu stosowania leku Strattera.
Zgłaszanie skutków ubocznych
Porozmawiaj z lekarzem lub farmaceutą, jeśli:
- wystąpi którykolwiek z tych skutków ubocznych i stanie się uciążliwy lub pogorszy się
- wystąpią jakiekolwiek działania niepożądane niewymienione w tej ulotce.
Działania niepożądane można również zgłaszać bezpośrednio za pośrednictwem strony internetowej Włoskiej Agencji Leków (www.agenziafarmaco.it/it/responsabili).Zgłaszając działania niepożądane, można uzyskać więcej informacji na temat bezpieczeństwa stosowania tego leku.
Wygaśnięcie i przechowywanie
Przechowuj Stratterę w miejscu niedostępnym i niewidocznym dla dzieci.
Nie stosować leku Strattera po upływie terminu ważności zamieszczonego na pudełku i blistrze po „EXP”. Termin ważności odnosi się do ostatniego dnia miesiąca.
Ten produkt leczniczy nie wymaga żadnych specjalnych warunków przechowywania.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa, co pomoże chronić środowisko.
Inne informacje
Czynności, które zrobi lekarz podczas leczenia lekiem
Lekarz wykona kilka badań:
- przed rozpoczęciem leczenia (aby Strattera była bezpieczna i korzystna)
- po rozpoczęciu leczenia (będą one wykonywane nie rzadziej niż co 6 miesięcy, ale być może częściej)
Testy zostaną przeprowadzone nawet w przypadku zmiany dawki. Testy te obejmą:
- pomiar wzrostu i wagi u dzieci i młodzieży
- pomiar ciśnienia krwi i tętna
- sprawdzić, czy nie występują problemy lub czy podczas stosowania leku Strattera nie nasiliły się działania niepożądane.
Co zawiera Strattera 10, 18, 25, 40, 60, 80 i 100 mg kapsułki twarde
- Substancją czynną jest chlorowodorek atomoksetyny. Każda kapsułka twarda zawiera atomoksetyny chlorowodorek w ilości odpowiadającej 10 mg, 18 mg, 25 mg, 40 mg, 60, 80 i 100 mg atomoksetyny.
- Pozostałe składniki to wstępnie żelowana skrobia i dimetikon.
- Otoczka kapsułki zawiera laurylosiarczan sodu i żelatynę Kolory otoczki kapsułki to: Żółty tlenek żelaza E172 (18 mg, 60 mg, 80 mg i 100 mg) Dwutlenek tytanu E171 (10 mg, 18 mg, 25 mg, 40 mg, 60 mg, 80 mg i 100 mg) FD&C Blue 2 (indygotyna) E132 (25 mg, 40 mg i 60 mg) Żelaza tlenek czerwony E172 (80 mg i 100 mg) Czarny jadalny tusz (zawierający szelak i czarny tlenek żelaza E172).
Jak wygląda lek Strattera i co zawiera opakowanie
- Kapsułki twarde 10 mg (białe z Lilly 3227/10 mg)
- Kapsułki twarde 18 mg (złote/białe, z nadrukiem Lilly 3238/18 mg)
- Kapsułki twarde 25 mg (niebieskie / białe, z Lilly 3228/25 mg)
- Kapsułki twarde 40 mg (niebieskie, oznaczone Lilly 3229/40 mg)
- Kapsułki twarde 60 mg (niebieskie / złote, z napisem Lilly 3239/60 mg)
- Kapsułki twarde 80 mg (brązowe / białe, z nadrukiem Lilly 3250/80 mg)
- Kapsułki twarde 100 mg (brązowe, oznaczone Lilly 3251/100 mg)
Kapsułki Strattera są dostępne w opakowaniach po 7, 14, 28 lub 56 kapsułek. Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
Informacje dla dzieci i młodzieży
Informacje te pomogą Ci poznać najważniejsze informacje o leku o nazwie Strattera.
Jeśli nie lubisz czytać, ktoś taki jak twoja mama, tata lub opiekun może ci to przeczytać i odpowiedzieć na wszelkie pytania. Pomocne może być przeczytanie go od czasu do czasu.
Dlaczego podano mi ten lek?
- Lek ten może pomóc dzieciom i młodzieży z ADHD.
- ADHD może:
- sprawiasz, że biegasz za dużo
- nie uważaj
- sprawiają, że działasz szybko, nie myśląc o tym, co będzie dalej (impulsywność)
- Koliduje z nauką, relacjami z przyjaciółmi i tym, co myślisz o sobie.To nie twoja wina.
Podczas przyjmowania tego leku
- Oprócz przyjmowania tego leku otrzymasz również inną pomoc w radzeniu sobie z ADHD, na przykład rozmowę ze specjalistami ADHD.
- Ten lek musi ci pomóc. Ale to nie leczy ADHD.
- Będziesz musiał chodzić do lekarza kilka razy w roku na kontrole. Ma to na celu upewnienie się, że lek działa i że dobrze się rozwijasz i rozwijasz.
- Dziewczęta powinny natychmiast powiadomić lekarza, jeśli podejrzewają, że mogą być w ciąży. Nie wiemy, jak ten lek wpływa na płód. Jeśli uprawiasz seks, porozmawiaj ze swoim lekarzem o antykoncepcji.
Niektórzy ludzie nie mogą przyjmować tego leku
Nie możesz przyjmować tego leku, jeśli:
- zażyłeś lek znany jako inhibitor monoaminooksydazy (IMAO), taki jak fenelzyna, w ciągu ostatnich dwóch tygodni
- masz chorobę oczu zwaną jaskrą z wąskim kątem przesączania (podwyższone ciśnienie w oku)
- masz poważne problemy z sercem
- masz poważne problemy z naczyniami krwionośnymi w mózgu;
- masz guza nadnerczy
Niektóre osoby muszą porozmawiać z lekarzem przed rozpoczęciem przyjmowania tego leku
Musisz porozmawiać z lekarzem, jeśli:
- jesteś w ciąży lub karmisz piersią
- przyjmujesz inne leki – lekarz musi zostać poinformowany o wszystkich przyjmowanych lekach
- masz myśli o skrzywdzeniu siebie lub innych
- masz problemy ze zbyt szybkim biciem serca lub pomijaniem uderzeń, mimo że nie ćwiczysz
- słyszysz głosy lub widzisz rzeczy, których inni ludzie nie widzą ani nie słyszą
- łatwo się denerwujesz
Jak zażywać ten lek (kapsułki)?
- Lek należy połknąć, popijając wodą, niezależnie od posiłków.
- Kapsułek nie wolno otwierać. Jeśli kapsułki pękną, a zawartość kapsułek wejdzie w kontakt ze skórą lub oczami, poproś o pomoc osobę dorosłą.
- Lekarz poinformuje Cię, ile razy dziennie należy przyjmować ten lek.
- Przyjmowanie tego leku o tej samej porze każdego dnia może pomóc pamiętać o jego przyjmowaniu.
- Nie należy przerywać przyjmowania leku bez wcześniejszej konsultacji z lekarzem.
Możliwe efekty uboczne
- Skutki uboczne to niepożądane rzeczy, które mogą się zdarzyć po zażyciu leku. Jeśli wystąpi którykolwiek z poniższych skutków ubocznych, natychmiast porozmawiaj z zaufaną osobą dorosłą. Następnie omówi to z lekarzem. Główne rzeczy, które mogą się zdarzyć, to:
- Twoje serce bije szybciej niż normalnie
- Być bardzo przygnębionym i nieszczęśliwym lub chcąc zrobić sobie krzywdę
- Czuję się agresywny
- Poczucie nieszczęścia lub inny nastrój niż zwykle (wahania nastroju)
- Wykazywać objawy reakcji alergicznej, takie jak „wysypka, swędzenie lub pokrzywka, obrzęk twarzy, warg, języka lub innych części ciała, duszność, świszczący oddech lub trudności w oddychaniu
- Drgawki
- Widzenie, odczuwanie lub słyszenie rzeczy, których inni ludzie nie widzą, nie czują ani nie słyszą
- Uszkodzenie wątroby: ból brzucha, który boli przy uciskaniu (tkliwość) po prawej stronie tuż pod żebrami
Ponieważ lek może powodować senność, ważne jest, aby nie uprawiać sportów na świeżym powietrzu, takich jak jazda konna lub jazda na rowerze, pływanie lub wspinanie się na drzewa.
Jeśli odczuwasz jakikolwiek dyskomfort podczas przyjmowania leku, natychmiast powiadom zaufaną osobę dorosłą.
Inne rzeczy do zapamiętania
- Upewnij się, że przechowujesz lek w bezpiecznym miejscu, aby nikt inny go nie wziął, zwłaszcza młodsi bracia lub siostry.
- Lek jest właśnie dla Ciebie – nie pozwól nikomu go wziąć. To może ci pomóc, ale może być złe dla innych.
- W przypadku pominięcia leku, nie należy następnym razem przyjmować dwóch tabletek. Po prostu weź jedną tabletkę o zwykłej porze.
- Jeśli zażyjesz za dużo leku, natychmiast powiadom mamę, tatę lub opiekuna.
- Ważne jest, aby nie zażywać zbyt dużo leków, bo zachorujesz.
- Nie należy przerywać przyjmowania leku, dopóki lekarz nie stwierdzi, że wszystko jest w porządku.
Kogo powinienem zapytać, jeśli jest coś, czego nie rozumiem?
Twoja mama, ojciec, opiekun, lekarz, pielęgniarka lub farmaceuta mogą Ci pomóc.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO
KAPSUŁKI TWARDE STRATTERS
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY
Każda kapsułka twarda zawiera atomoksetyny chlorowodorek w ilości odpowiadającej 10 mg, 18 mg, 25 mg, 40 mg, 60 mg, 80 mg i 100 mg atomoksetyny.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
03.0 POSTAĆ FARMACEUTYCZNA
Kapsułki twarde.
Kapsułki STRATTERA 10 mg: białe, nieprzezroczyste, twarde kapsułki z czarnym nadrukiem „Lilly 3227” i „10 mg”.
Kapsułki STRATTERA 18 mg: złote (wieczko) i nieprzezroczyste białe (korpus), twarde kapsułki z czarnym nadrukiem „Lilly 3238” i „18 mg”.
Kapsułki STRATTERA 25 mg: nieprzezroczyste niebieskie (wieczko) i nieprzezroczyste białe (korpus), twarde kapsułki z czarnym nadrukiem „Lilly 3228” i „25 mg”.
Kapsułki STRATTERA 40 mg: nieprzezroczyste, niebieskie, twarde kapsułki z czarnym nadrukiem „Lilly 3229” i „40 mg”.
Kapsułki STRATTERA 60 mg: nieprzezroczyste niebieskie (wieczko) i złote (korpus) kapsułki twarde z czarnym nadrukiem „Lilly 3239” i „60 mg”.
Kapsułki STRATTERA 80 mg: nieprzezroczyste brązowe (wieczko) i nieprzezroczyste białe (korpus), twarde kapsułki z czarnym nadrukiem „Lilly 3250” i „80 mg”.
Kapsułki STRATTERA 100 mg: nieprzezroczyste, brązowe, twarde kapsułki z czarnym nadrukiem „Lilly 3251” i „100 mg”.
4.
04.0 INFORMACJE KLINICZNE
04.1 Wskazania terapeutyczne
Strattera jest wskazana w leczeniu zespołu nadpobudliwości psychoruchowej z deficytem uwagi (ADHD) u dzieci w wieku 6 lat, młodzieży i dorosłych w ramach multimodalnego programu leczenia.Leczenie powinien rozpocząć lekarz specjalista w leczeniu ADHD, taki jak pediatra, neuropsychiatra lub psychiatra wieku dziecięcego i młodzieńczego. Diagnozę należy postawić zgodnie z kryteriami ustalonymi przez aktualne wytyczne DSM lub ICD.
U dorosłych należy potwierdzić obecność objawów ADHD, które występowały wcześniej w dzieciństwie.Potwierdzenie przez stronę trzecią jest pożądane i Strattera nie powinna być rozpoczynana, jeśli badanie objawów ADHD w dzieciństwie jest niepewne. Rozpoznania nie można postawić wyłącznie na podstawie obecności jednego lub więcej objawów ADHD.Na podstawie oceny klinicznej pacjenci muszą mieć ADHD o co najmniej umiarkowanym nasileniu, na co wskazuje co najmniej umiarkowane upośledzenie czynnościowe w 2 lub więcej obszarach (np. społeczne, edukacyjne i/lub zawodowe) mające wpływ na różne aspekty życia jednostki.
Dodatkowe informacje dotyczące bezpiecznego stosowania tego leku:
Program leczenia multimodalnego zwykle obejmuje interwencje psychologiczne, edukacyjne i społeczne mające na celu ustabilizowanie pacjentów z zaburzeniem zachowania charakteryzującym się objawami, które mogą obejmować: przewlekłą historię słabej koncentracji, nieuwagę, labilność emocjonalną, impulsywność, nadaktywność umiarkowaną do ciężkiej, niewielkie objawy neurologiczne i nieprawidłowe EEG. Nauka może być zaburzona lub nie.
Leczenie farmakologiczne nie jest wskazane dla wszystkich pacjentów z tym zaburzeniem i decyzja o zastosowaniu leku musi być oparta na bardzo wnikliwej ocenie nasilenia objawów oraz upośledzenia pacjenta w stosunku do jego wieku i utrzymywania się objawów.
04.2 Dawkowanie i sposób podawania
Do stosowania doustnego. Strattera można podawać w pojedynczej dawce dobowej rano, niezależnie od posiłków. Pacjenci, u których nie uzyskano zadowalającej odpowiedzi klinicznej (w zakresie tolerancji [na przykład nudności lub senność] lub skuteczności) przyjmujący Strattera w pojedynczej dawce dobowej, mogą odnieść korzyść, dzieląc dobową dawkę leku na dwie równe dawki, pierwszą w rano a drugi późnym popołudniem lub wczesnym wieczorem.
Dawkowanie u dzieci/młodzieży o masie ciała do 70 kg:
Strattera należy podawać początkowo w całkowitej dawce dobowej około 0,5 mg/kg.
Dawkę początkową należy utrzymywać przez co najmniej 7 dni przed jej stopniowym zwiększaniem w zależności od odpowiedzi klinicznej i tolerancji. Zalecana dawka podtrzymująca wynosi około 1,2 mg/kg/dobę (na podstawie masy ciała pacjenta i dostępnych dawek atomoksetyny). Dawki powyżej 1,2 mg/kg/dobę nie wykazały żadnych dodatkowych korzyści. Bezpieczeństwo pojedynczych dawek powyżej 1,8 mg/kg/dobę i całkowitych dawek dobowych powyżej 1,8 mg/kg nie było systematycznie oceniane. W niektórych przypadkach właściwe może być kontynuowanie leczenia w wieku dorosłym.
Dawkowanie u dzieci/młodzieży o masie ciała powyżej 70 kg:
Strattera należy podawać początkowo w łącznej dawce dobowej 40 mg. Dawkę początkową należy utrzymywać przez co najmniej 7 dni przed jej stopniowym zwiększaniem w zależności od odpowiedzi klinicznej i tolerancji. Zalecana dawka podtrzymująca to 80 mg. Dawki powyżej 80 mg nie wykazały dodatkowych korzyści. Maksymalna zalecana całkowita dawka dobowa wynosi 100 mg. Bezpieczeństwo pojedynczych dawek większych niż 120 mg i całkowitych dawek dobowych większych niż 150 mg nie było systematycznie oceniane.
Dawkowanie u dorosłych
Strattera należy podawać początkowo w łącznej dawce dobowej 40 mg. Dawkę początkową należy utrzymywać przez co najmniej 7 dni przed jej stopniowym zwiększaniem w zależności od odpowiedzi klinicznej i tolerancji. Zalecana dzienna dawka podtrzymująca wynosi 80 mg do 100 mg. Maksymalna zalecana całkowita dawka dobowa wynosi 100 mg. Bezpieczeństwo pojedynczych dawek większych niż 120 mg i całkowitych dawek dobowych większych niż 150 mg nie było systematycznie oceniane.
Dodatkowe informacje dotyczące bezpiecznego stosowania tego leku:
Badanie przesiewowe przed zabiegiem:
Przed przepisaniem należy przeprowadzić odpowiednią historię medyczną i wstępną ocenę stanu sercowo-naczyniowego pacjenta, w tym ciśnienia krwi i częstości akcji serca (patrz punkty 4.3 i 4.4).
Monitorowanie w trakcie leczenia:
Stan sercowo-naczyniowy należy regularnie monitorować, rejestrując ciśnienie krwi i częstość akcji serca po każdym dostosowaniu dawki, a następnie co najmniej co sześć miesięcy. W przypadku pacjentów pediatrycznych zaleca się stosowanie wykresu centylowego, natomiast w przypadku dorosłych należy przestrzegać aktualnych wytycznych dotyczących nadciśnienia tętniczego. (Patrz punkt 4.4).
Przerwanie leczenia
W programie rozwoju leku nie opisano wyraźnych objawów odstawiennych. W przypadku istotnych działań niepożądanych atomoksetyna może zostać nagle przerwana; w przeciwnym razie lek może być powoli odstawiany przez odpowiedni okres czasu.
Leczenie lekiem Strattera niekoniecznie musi trwać w nieskończoność. Należy ponownie ocenić potrzebę kontynuacji leczenia przez ponad 1 rok, zwłaszcza jeśli pacjent uzyskał stabilną i zadowalającą odpowiedź.
Populacje specjalne
Niewydolność wątroby: U pacjentów z umiarkowanymi zaburzeniami czynności wątroby (klasa B wg Childa-Pugha) dawki początkowe i podtrzymujące należy zmniejszyć do 50% zwykle stosowanej dawki. U pacjentów z ciężkimi zaburzeniami czynności wątroby (klasa C w skali Childa-Pugha) dawkę początkową i podtrzymującą należy zmniejszyć do 25% zwykle stosowanej dawki. (patrz punkt 5.2).
Niewydolność nerek: pacjenci ze schyłkową niewydolnością nerek mieli większą ogólnoustrojową ekspozycję na atomoksetynę niż osoby zdrowe (wzrost o około 65%), ale nie zaobserwowano różnicy po korekcie ekspozycji na dawkę mg/kg. Strattera można zatem podawać pacjentom z ADHD ze schyłkową niewydolnością nerek lub z niewydolnością nerek o mniejszym stopniu, stosując zwykłe dawkowanie. Atomoksetyna może nasilać nadciśnienie u pacjentów ze schyłkową niewydolnością nerek. (patrz punkt 5.2).
Około 7% populacji rasy kaukaskiej ma genotyp odpowiadający niefunkcjonującemu enzymowi CYP2D6 (nazywanemu słabym metabolizmem CYP2D6). Pacjenci z tym genotypem są kilkakrotnie bardziej narażeni na atomoksetynę niż pacjenci z czynnym enzymem. Osoby o słabym metabolizmie są zatem bardziej narażone na wystąpienie zdarzeń niepożądanych (patrz punkty 4.8 i 5.2). należy rozważyć wolniejsze dostosowywanie dawki.
Starsi ludzie: stosowanie atomoksetyny u pacjentów w wieku powyżej 65 lat nie było systematycznie oceniane.
Dzieci poniżej 6 roku życia: Nie ustalono bezpieczeństwa i skuteczności stosowania produktu Strattera u dzieci w wieku poniżej 6 lat, dlatego produktu Strattera nie należy stosować u dzieci w wieku poniżej 6 lat (patrz punkt 4.4).
04.3 Przeciwwskazania
Nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1.
Atomoksetyny nie wolno stosować w skojarzeniu z inhibitorami monoaminooksydazy (IMAO).
Atomoksetyny nie należy stosować przez co najmniej dwa tygodnie po zakończeniu leczenia IMAO.Leczenia IMAO nie należy rozpoczynać w ciągu dwóch tygodni po zakończeniu leczenia atomoksetyną.
Atomoksetyny nie należy stosować u pacjentów z jaskrą z wąskim kątem przesączania, ponieważ w badaniach klinicznych stosowanie atomoksetyny wiązało się ze zwiększoną częstością występowania rozszerzenia źrenic.
Atomoksetyny nie należy stosować u pacjentów z ciężką chorobą sercowo-naczyniową lub chorobą naczyń mózgowych (patrz punkt 4.4 Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania – Wpływ na układ sercowo-naczyniowy) Poważne choroby układu krążenia mogą obejmować ciężkie nadciśnienie tętnicze, niewydolność serca, zarostową chorobę tętnic, dusznicę bolesną, hemodynamicznie istotną wrodzoną wadę serca , kardiomiopatie, zawał mięśnia sercowego, potencjalnie zagrażające życiu arytmie i zaburzenia kanałów (choroby spowodowane dysfunkcją kanału jonowego) Poważne choroby naczyń mózgowych mogą obejmować tętniak mózgu lub udar mózgu.
Atomoksetyny nie należy stosować u pacjentów z guzem chromochłonnym nadnerczy lub guzem chromochłonnym nadnerczy w wywiadzie (patrz punkt 4.4 Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania – Wpływ na układ sercowo-naczyniowy).
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania
Zachowania samobójcze
Zachowania samobójcze (próby samobójcze i myśli samobójcze) zgłaszano u pacjentów leczonych atomoksetyną.W badaniach klinicznych z podwójnie ślepą próbą przypadki zachowań samobójczych były rzadkie, ale obserwowane częściej u dzieci i młodzieży leczonych atomoksetyną niż u dzieci otrzymujących placebo, w których nie było przypadków. W badaniach klinicznych z podwójnie ślepą próbą u dorosłych nie stwierdzono różnicy w częstości zachowań samobójczych pomiędzy atomoksetyną a placebo.Pacjenci leczeni z powodu ADHD powinni być uważnie obserwowani pod kątem wystąpienia lub nasilenia zachowań samobójczych.
Nagła śmierć i istniejące wcześniej nieprawidłowości serca
U pacjentów ze strukturalnymi zaburzeniami serca, którzy przyjmowali atomoksetynę w zwykłych dawkach, zgłaszano nagły zgon.Chociaż niektóre ciężkie strukturalne zaburzenia serca niosą ze sobą zwiększone ryzyko nagłego zgonu, atomoksetynę należy stosować ostrożnie u pacjentów ze znanymi strukturalnymi zaburzeniami serca. ciężki i po konsultacji z kardiologiem.
Wpływ na układ sercowo-naczyniowy
Atomoksetyna może wpływać na częstość akcji serca i ciśnienie krwi.
Niewielki wzrost częstości akcji serca (średnie ciśnienie krwi (średnie
Jednak połączone dane z kontrolowanych i niekontrolowanych badań klinicznych dotyczących ADHD pokazują, że około 8-12% dzieci i młodzieży oraz 6-10% dorosłych ma bardziej wyraźną zmianę częstości akcji serca (20 uderzeń na minutę lub więcej) i krwi. ciśnienie (15-20 mm Hg lub wyższe). Analiza danych z tych badań klinicznych wykazała, że około 15-26% dzieci i młodzieży oraz 27-32% dorosłych, u których wystąpiły takie zmiany ciśnienia krwi i częstości akcji serca podczas leczenia atomoksetyną, miało przedłużone lub postępujące zwiększenie przyczyniają się w dłuższej perspektywie do następstw klinicznych, takich jak przerost mięśnia sercowego.
W wyniku tych ustaleń „u pacjentów rozważanych do leczenia atomoksetyną należy przeprowadzić dokładny wywiad lekarski i badanie fizykalne w celu oceny chorób serca, a tacy pacjenci powinni zostać poddani dalszej specjalistycznej ocenie kardiologicznej, jeśli wyniki są wstępne, sugerując chorobę serca w wywiadzie. lub choroba serca.
Zaleca się mierzenie i rejestrowanie częstości akcji serca i ciśnienia krwi przed rozpoczęciem leczenia oraz w trakcie leczenia, po każdym dostosowaniu dawki, a następnie co najmniej co 6 miesięcy w celu zidentyfikowania możliwych klinicznie istotnych wzrostów. W przypadku pacjentów pediatrycznych zaleca się stosowanie wykresu centylowego, natomiast w przypadku dorosłych należy przestrzegać aktualnych wytycznych dotyczących nadciśnienia tętniczego.
Atomoksetyny nie wolno stosować u pacjentów z ciężką chorobą układu krążenia lub naczyń mózgowych (patrz punkt 4.3 Przeciwwskazania – Ciężkie choroby układu krążenia i naczyń mózgowych). Atomoksetynę należy stosować ostrożnie u pacjentów, których podstawowe schorzenia mogą się nasilać w wyniku wzrostu ciśnienia krwi i częstości akcji serca, takich jak pacjenci z nadciśnieniem tętniczym, tachykardią lub chorobą sercowo-naczyniową lub mózgowo-naczyniową.
Pacjenci, u których podczas leczenia atomoksetyną wystąpią objawy, takie jak kołatanie serca, ból w klatce piersiowej spowodowany wysiłkiem, omdlenia o niewyjaśnionej przyczynie, duszność lub inne objawy sugerujące chorobę serca, powinni zostać niezwłocznie poddani specjalistycznej ocenie kardiologicznej.
Ponadto atomoksetynę należy stosować ostrożnie u pacjentów z wrodzonym lub nabytym zespołem wydłużonego odstępu QT lub wydłużeniem odstępu QT w wywiadzie rodzinnym (patrz punkty 4.5 i 4.8).
Ponieważ zgłaszano również przypadki niedociśnienia ortostatycznego, atomoksetynę należy stosować ostrożnie w każdej sytuacji, która może predysponować pacjenta do niedociśnienia lub w sytuacjach związanych z nagłymi zmianami częstości akcji serca lub ciśnienia krwi.
Wpływ na naczynia mózgowe
Pacjenci z dodatkowymi czynnikami ryzyka zaburzeń naczyniowo-mózgowych (takimi jak choroba sercowo-naczyniowa w wywiadzie, jednoczesne stosowanie produktów leczniczych podnoszących ciśnienie krwi) powinni być oceniani na każdej wizycie pod kątem neurologicznych objawów przedmiotowych i podmiotowych po rozpoczęciu leczenia atomoksetyną.
Wpływ na wątrobę
Bardzo rzadko zgłaszano spontaniczne przypadki uszkodzenia wątroby, charakteryzujące się podwyższoną aktywnością enzymów wątrobowych i zwiększeniem stężenia bilirubiny w połączeniu z żółtaczką. Ponadto bardzo rzadko zgłaszano ciężkie uszkodzenie wątroby, w tym ostrą niewydolność wątroby. Leczenie produktem Strattera należy przerwać u pacjentów z żółtaczką lub u których badania laboratoryjne wskazują na uszkodzenie wątroby i nie wolno podawać ponownie.
Objawy psychotyczne lub maniakalne
Objawy maniakalne lub psychotyczne, które występują podczas leczenia atomoksetyną, na przykład omamy, urojenia, mania lub pobudzenie u pacjentów bez wcześniejszych zaburzeń psychotycznych lub manii, mogą być spowodowane przez atomoksetynę w zwykłych dawkach. W przypadku wystąpienia takich objawów należy rozważyć możliwość, że są one spowodowane przez atomoksetynę i należy rozważyć przerwanie leczenia. Nie można wykluczyć, że Strattera powoduje nasilenie wcześniej istniejących objawów psychotycznych lub maniakalnych.
Agresywne zachowanie, wrogość lub labilność emocjonalna
W badaniach klinicznych wrogość (głównie agresję, zachowania buntownicze i gniew) obserwowano częściej u dzieci, młodzieży i dorosłych leczonych produktem Strattera niż u osób otrzymujących placebo. W badaniach klinicznych chwiejność emocjonalną obserwowano częściej u dzieci leczonych produktem Strattera niż u dzieci otrzymujących placebo. Pacjenci powinni być ściśle monitorowani pod kątem pojawienia się lub pogorszenia zachowań agresywnych, wrogości lub labilności emocjonalnej.
Możliwe zdarzenia alergiczne
Chociaż niezbyt często, u pacjentów otrzymujących atomoksetynę zgłaszano reakcje alergiczne, w tym reakcje anafilaktyczne, wysypkę, obrzęk naczynioruchowy i pokrzywkę.
Drgawki
Napady padaczkowe są potencjalnym ryzykiem związanym z atomoksetyną. Leczenie atomoksetyną należy rozpoczynać ostrożnie u pacjentów z drgawkami w wywiadzie. Należy rozważyć przerwanie leczenia atomoksetyną u każdego pacjenta, u którego wystąpią drgawki lub w przypadku zwiększenia częstości napadów, gdy nie zidentyfikowano innej przyczyny.
Wzrost i rozwój
Podczas leczenia atomoksetyną należy monitorować wzrost i rozwój dzieci i młodzieży. Pacjenci wymagający długotrwałego leczenia powinni być okresowo monitorowani i należy rozważyć zmniejszenie dawki lub przerwanie leczenia u dzieci i młodzieży z niezadowalającym wzrostem lub przyrostem masy ciała.
Dane kliniczne nie wskazują na negatywny wpływ atomoksetyny na funkcje poznawcze lub dojrzewanie płciowe, jednak ilość dostępnych danych odległych jest ograniczona, dlatego pacjenci wymagający długotrwałego leczenia powinni być uważnie monitorowani.
Wystąpienie lub nasilenie współwystępującej depresji, lęku i tików
W kontrolowanym badaniu przeprowadzonym u dzieci z ADHD i równoczesnym występowaniem przewlekłych tików ruchowych lub zespołu Tourette'a, u pacjentów leczonych atomoksetyną nie wystąpiły nasilenie tików w porównaniu z pacjentami, którym podawano placebo. W kontrolowanym badaniu przeprowadzonym u nastoletnich pacjentów z ADHD i równoczesnym występowaniem dużego zaburzenia depresyjnego, u pacjentów leczonych atomoksetyną nie wystąpiło pogorszenie depresji w porównaniu z pacjentami otrzymującymi placebo. W dwóch kontrolowanych badaniach przeprowadzonych u pacjentów z ADHD (jedno z udziałem dzieci i dorosłych) i współistniejącymi zaburzeniami lękowymi, u pacjentów leczonych atomoksetyną nie występowało nasilenie lęku w porównaniu z pacjentami otrzymującymi placebo.
W okresie po wprowadzeniu do obrotu u pacjentów przyjmujących atomoksetynę zgłaszano rzadkie przypadki lęku i depresji lub obniżonego nastroju oraz bardzo rzadkie przypadki tików (patrz punkt 4.8).
Pacjenci leczeni atomoksetyną z powodu ADHD powinni być uważnie obserwowani pod kątem pojawienia się lub nasilenia objawów lęku, obniżonego nastroju, depresji lub tików.
Dzieci poniżej 6 roku życia
Produkt Strattera nie powinien być stosowany u pacjentów w wieku poniżej 6 lat, ponieważ skuteczność i bezpieczeństwo w tej grupie wiekowej nie zostały ustalone.
Inne zastosowanie terapeutyczne
Strattera nie jest wskazany w leczeniu epizodów dużej depresji i (lub) lęku, ponieważ wyniki badań klinicznych u osób dorosłych w tych stanach bez ADHD nie wykazały działania w porównaniu z placebo (patrz punkt 5.1).
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji
Wpływ innych produktów leczniczych na atomoksetynę:
IMAO: atomoksetyny nie należy stosować w skojarzeniu z IMAO (patrz punkt 4.3).
Inhibitory CYP2D6 (SSRI (takie jak fluoksetyna i paroksetyna), chinidyna, terbinafina): U pacjentów otrzymujących te leki ekspozycja na atomoksetynę może być zwiększona od 6 do 8 razy, a Css max 3-4 razy większe, ponieważ atomoksetyna jest metabolizowana przez CYP2D6. U pacjentów już przyjmujących produkty lecznicze będące inhibitorami CYP2D6 może być wymagane wolniejsze zwiększanie dawki i mniejsza końcowa dawka atomoksetyny. Jeśli inhibitor CYP2D6 zostanie przepisany lub odstawiony po dostosowaniu dawki atomoksetyny do odpowiedniej dawki, należy ponownie ocenić odpowiedź kliniczną i tolerancję u tego pacjenta w celu ustalenia, czy konieczne jest dostosowanie dawki.
Należy zachować ostrożność podczas podawania atomoksetyny jednocześnie z silnymi inhibitorami enzymów cytochromu P450 innymi niż CYP2D6 pacjentom słabo metabolizującym z udziałem CYP2D6, ponieważ ryzyko klinicznie istotnego zwiększenia ekspozycji na atomoksetynę in vivo jest nieznane.
Salbutamol (lub inni agoniści beta 2):
Atomoksetynę należy podawać ostrożnie pacjentom leczonym dużymi dawkami salbutamolu (lub innych beta 2 -mimetyków) przyjmowanych w nebulizacji lub podawanych ogólnoustrojowo, ze względu na możliwość nasilenia działania sercowo-naczyniowego.
Zgłoszono sprzeczne wyniki dotyczące tej interakcji. Ogólnoustrojowe podawanie salbutamolu (600 mcg dożylnie w ciągu 2 godzin) w połączeniu z atomoksetyną (60 mg dwa razy dziennie przez 5 dni) powodowało wzrost częstości akcji serca i ciśnienia krwi. Efekt ten był najbardziej widoczny po początkowym równoczesnym podaniu salbutamolu i atomoksetyny, ale powrócił do wartości wyjściowych po 8 godzinach. Jednak w innym badaniu przeprowadzonym u zdrowych dorosłych Azjatów, szybko metabolizujących atomoksetynę, wpływ standardowej dawki salbutamolu podawanej wziewnie (200 mikrogramów) na ciśnienie krwi i częstość akcji serca nie uległ wzmocnieniu po jednoczesnym krótkotrwałym stosowaniu atomoksetyny ( 80 mg raz na dobę przez 5 dni). Podobnie częstość akcji serca po wielokrotnych inhalacjach salbutamolu (800 mcg) była podobna w obecności lub nieobecności atomoksetyny.
Należy zachować ostrożność podczas monitorowania częstości akcji serca i ciśnienia krwi, a dostosowanie dawki atomoksetyny lub salbutamolu (lub innych agonistów receptora beta2) może być uzasadnione w przypadku znacznego zwiększenia częstości akcji serca i ciśnienia krwi podczas jednoczesnego podawania tych leków.
Istnieje ryzyko zwiększonego ryzyka wydłużenia odstępu QT, gdy atomoksetyna jest podawana z innymi lekami wydłużającymi odstęp QT (takimi jak neuroleptyki, leki przeciwarytmiczne klasy IA i III, moksyfloksacyna, erytromycyna, metadon, meflochina, trójpierścieniowe leki przeciwdepresyjne, lit lub cyzapryd), leki które powodują zaburzenia równowagi elektrolitowej (takie jak diuretyki tiazydowe) i leki hamujące CYP2D6.
Napady padaczkowe stanowią potencjalne ryzyko związane z atomoksetyną. Zaleca się ostrożność podczas jednoczesnego stosowania leków, o których wiadomo, że mogą obniżać próg drgawkowy (takich jak trójpierścieniowe leki przeciwdepresyjne lub SSRI, neuroleptyki, fenotiazyny lub butyrofenon, meflochina, chlorochina, bupropion lub tramadol) (patrz punkt 4.4). Ponadto należy zachować ostrożność w przypadku przerwania jednoczesnego leczenia benzodiazepinami ze względu na możliwość wystąpienia drgawek związanych z przerwaniem leczenia.
Leki przeciwnadciśnieniowe
Atomoksetynę należy stosować ostrożnie razem z przeciwnadciśnieniowymi produktami leczniczymi. Ze względu na możliwy wzrost ciśnienia tętniczego, atomoksetyna może zmniejszać skuteczność leków przeciwnadciśnieniowych/leków stosowanych w leczeniu nadciśnienia tętniczego.Należy zachować ostrożność w monitorowaniu ciśnienia krwi i w przypadku, gdy uzasadniona może być ponowna ocena leczenia atomoksetyną lub lekami przeciwnadciśnieniowymi. znaczących zmian ciśnienia krwi.
Środki zwiększające ciśnienie lub leki zwiększające ciśnienie krwi
Ze względu na możliwy zwiększony wpływ na ciśnienie krwi, atomoksetynę należy stosować ostrożnie razem z lekami presyjnymi lub lekami, które mogą podwyższać ciśnienie krwi (takimi jak salbutamol). Należy uważnie monitorować ciśnienie krwi, a w przypadku istotnej zmiany ciśnienia krwi może być uzasadniona ponowna ocena leczenia atomoksetyną lub środkami podwyższającymi ciśnienie krwi.
Leki, które zakłócają noradrenalinę:
Produkty lecznicze, które wpływają na noradrenalinę, należy stosować ostrożnie jednocześnie z atomoksetyną ze względu na możliwe addytywne lub synergistyczne działanie farmakologiczne. Przykładami takich leków są leki przeciwdepresyjne, takie jak imipramina, wenlafaksyna i mirtazapina, lub leki zmniejszające przekrwienie, takie jak pseudoefedryna lub fenylefryna.
Leki wpływające na pH żołądka:
Produkty lecznicze zwiększające pH żołądka (wodorotlenek magnezu/wodorotlenek glinu, omeprazol) nie mają wpływu na biodostępność atomoksetyny.
Produkty lecznicze o wysokim stopniu wiązania z białkami osocza:
Przeprowadzono badania wypierania leku in vitro z zastosowaniem terapeutycznych stężeń atomoksetyny i innych leków silnie wiążących białka osocza. Warfaryna, kwas acetylosalicylowy, fenytoina lub diazepam nie wpływają na wiązanie atomoksetyny z albuminą ludzką. Podobnie atomoksetyna nie wpływa na wiązanie tych związków z ludzką albuminą.
04.6 Ciąża i laktacja
Ciąża
Ogólnie badania na zwierzętach nie wykazują bezpośredniego szkodliwego wpływu na ciążę, rozwój zarodka/płodu, przebieg porodu lub rozwój pourodzeniowy (patrz punkt 5.3). Dane kliniczne dotyczące narażenia na atomoksetynę w czasie ciąży są ograniczone. Dane te są niewystarczające, aby wskazać, czy istnieje „związek między atomoksetyną a działaniami niepożądanymi podczas ciąży i laktacji”. Atomoksetyny nie należy stosować w okresie ciąży, chyba że potencjalne korzyści nie są uzasadnić potencjalne ryzyko dla płodu.
Czas karmienia
U szczurów atomoksetyna i (lub) jej metabolity przenikają do mleka ludzkiego.Nie wiadomo, czy atomoksetyna przenika do mleka ludzkiego. Ze względu na brak danych należy unikać stosowania atomoksetyny w okresie karmienia piersią.
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Dane dotyczące wpływu na zdolność prowadzenia pojazdów i obsługiwania maszyn są ograniczone. Stosowanie atomoksetyny wiąże się z „zwiększoną częstością zmęczenia, senności i zawrotów głowy w porównaniu z placebo u pacjentów pediatrycznych i dorosłych. .
04.8 Działania niepożądane
Dzieci i młodzież:
W badaniach kontrolowanych placebo u dzieci i młodzieży najczęstszymi zdarzeniami niepożądanymi związanymi ze stosowaniem atomoksetyny były ból głowy, ból brzucha1 i zmniejszenie apetytu, zgłaszane odpowiednio przez około 19%, 18% i 16% pacjentów, które jednak rzadko powodują przerwanie leczenia. (wskaźniki przerwania leczenia wynoszą 0,1% w przypadku bólu głowy, 0,2% w przypadku bólu brzucha i 0,0% w przypadku zmniejszonego apetytu). Ból brzucha i zmniejszony apetyt są zwykle przemijające.
W związku ze zmniejszonym apetytem, u niektórych pacjentów na początku leczenia wystąpiło opóźnienie wzrostu zarówno pod względem przyrostu masy ciała, jak i wzrostu. Średnio, po początkowym zmniejszeniu przyrostu masy ciała i wzrostu, pacjenci leczeni atomoksetyną powrócili do średniej masy ciała i wzrostu przewidywanej na podstawie danych z grupy wyjściowej pacjentów leczonych przez długi czas.
Nudności, wymioty i senność2 mogą wystąpić u około 10% - 11% pacjentów, zwłaszcza w pierwszym miesiącu terapii. Jednak epizody te miały na ogół nasilenie łagodne do umiarkowanego i były przemijające i nie prowadziły do znacznej liczby przerw w leczeniu (wskaźnik przerwania leczenia ≤ 0,5%).
Zarówno w badaniach z udziałem dzieci, jak i kontrolowanych placebo badaniach z udziałem osób dorosłych u pacjentów leczonych atomoksetyną wystąpiło zwiększenie częstości akcji serca oraz skurczowego i rozkurczowego ciśnienia krwi (patrz punkt 4.4).
Ze względu na wpływ na napięcie noradrenergiczne u pacjentów przyjmujących atomoksetynę zgłaszano niedociśnienie ortostatyczne (0,2%) i omdlenia (0,8%). Atomoksetynę należy stosować ostrożnie w każdym stanie predysponującym pacjenta do niedociśnienia.
Poniższa tabela działań niepożądanych została sporządzona na podstawie zgłoszeń zdarzeń niepożądanych i badań laboratoryjnych przeprowadzonych podczas badań klinicznych oraz zgłoszeń spontanicznych zgłaszanych u dzieci i młodzieży w okresie po wprowadzeniu produktu do obrotu.
Tabela: Działania niepożądane
Szacowana częstość: bardzo często (≥1/10), często (≥1/100,
1 Obejmuje również ból w górnej części brzucha, dyskomfort w nadbrzuszu, brzuch i brzuch.
2 Obejmuje również sedację.
3 Obejmuje bezsenność początkową, centralną i terminalną (przebudzenie wcześnie rano).
4Tętno i ciśnienie krwi opierają się na pomiarze parametrów życiowych.
* Patrz punkt 4.4.
** Patrz punkty 4.4 i 4.5.
Osoby słabo metabolizujące CYP2D6 (PM)
Następujące działania niepożądane występowały z częstością co najmniej 2% u pacjentów ze słabym metabolizmem przy użyciu CYP2D6 i były statystycznie istotnie częstsze u pacjentów ze słabym metabolizmem przy użyciu CYP2D6 (PM) niż u pacjentów ze intensywnym (EM) metabolizmem przy użyciu CYP2D6: apetyt (24,1% u pacjentów z PM, 17,0% u pacjentów z EM), bezsenność mieszana (w tym bezsenność, bezsenność ośrodkowa i bezsenność początkowa, 14,9% u pacjentów z PM, 9,7% u pacjentów z EM), depresja mieszana (w tym depresja, duża depresja, objawy depresyjne, obniżony nastrój i dysforia, 6,5 % u pacjentów z PM i 4,1% u pacjentów EM), zmniejszenie masy ciała (7,3% u pacjentów z PM, 4,4% u pacjentów EM EM), zaparcia (6,8% u pacjentów z PM, 4,3% u pacjentów EM), drżenie (4,5% u pacjentów z PM pacjentów, 0,9% u pacjentów z EM); sedacja (3,9% u pacjentów z PM, 2,1% u pacjentów z EM); przeczos (3,9% u pacjentów z PM, 1,7% u pacjentów z EM); moczenie (3,0% u pacjentów z PM, 1,2% u pacjentów z EM); pacjenci z EM); zapalenie spojówek (2,5% u pacjentów z PM, 1,2% u pacjentów z EM); omdlenie (2,5% u pacjentów z PM, 0,7% u pacjentów z EM); wczesne budzenie się rano (2,3% u pacjentów z PM, 0,8% u pacjentów z EM); rozszerzenie źrenic (2,0% u pacjentów z PM, 0,6% u pacjentów z EM). Na uwagę zasługuje następujące zdarzenie, które nie spełnia powyższych kryteriów: zaburzenie lękowe uogólnione (0,8% u pacjentów z PM, 0,1% u pacjentów z EM), ponadto w badaniach trwających do 10 tygodni ubytek masy ciała był wyraźniejszy u pacjentów z PM ( średnio 0,6 kg u pacjentów EM i 1,1 kg u pacjentów PM).
Dorośli ludzie:
W badaniach klinicznych ADHD u dorosłych podczas leczenia atomoksetyną najczęstszymi zdarzeniami niepożądanymi według klasyfikacji układów i narządów były zaburzenia żołądkowo-jelitowe, zaburzenia układu nerwowego i zaburzenia psychiczne.Najczęstszymi zgłaszanymi zdarzeniami niepożądanymi (≥5%) było zmniejszenie apetytu (14,9%), bezsenność (11,3%), ból głowy (16,3%), suchość w ustach (18,4%) i nudności (26,7%)). Większość z tych zdarzeń miała nasilenie łagodne do umiarkowanego, a najczęściej zgłaszanymi poważnymi zdarzeniami były nudności, bezsenność, zmęczenie i ból głowy.
Występowanie zatrzymania moczu lub wahania moczu u dorosłych pacjentów należy uznać za potencjalnie związane z atomoksetyną.
Poniższa tabela działań niepożądanych została sporządzona na podstawie zgłoszeń zdarzeń niepożądanych i badań laboratoryjnych przeprowadzonych podczas badań klinicznych oraz zgłoszeń spontanicznych u osób dorosłych w okresie po wprowadzeniu produktu do obrotu.
Tabela: Działania niepożądane
Szacowana częstość: bardzo często (≥1/10), często (≥1/100,
1 Obejmuje również ból w górnej części brzucha, dyskomfort w nadbrzuszu, brzuch i brzuch.
2 Obejmuje również bezsenność początkową, centralną i terminalną (przebudzenie wcześnie rano).
3 Tętno i ciśnienie krwi opierają się na pomiarze parametrów życiowych.
4 Obejmuje reakcje anafilaktyczne i obrzęk naczynioruchowy.
* Patrz punkt 4.4.
** Patrz punkty 4.4 i 4.5.
Osoby słabo metabolizujące CYP2D6 (PM)
Następujące działania niepożądane występowały z częstością co najmniej 2% u pacjentów ze słabym metabolizmem przy użyciu CYP2D6 i były statystycznie istotnie częstsze u pacjentów ze słabym metabolizmem przy użyciu CYP2D6 (PM) niż u pacjentów ze intensywnym (EM) metabolizmem przy użyciu CYP2D6: niewyraźne widzenie (3,9% u pacjentów z PM) , 1,3% u pacjentów EM), suchość w ustach (34,5% u pacjentów z PM, 17,4% u pacjentów EM), zaparcia (11,3% u pacjentów z PM, 6, 7% u pacjentów EM), nerwowość (4,9% u pacjentów z PM, 1,9 % u pacjentek EM), zmniejszony apetyt (23,2% u pacjentek z PM, 14,7% u pacjentek EM), mięśniak macicy (2,3% u pacjentek z PM, 0,1% u pacjentek EM), drżenie (5,4% u pacjentek z PM, 1,2% u pacjentek EM pacjentów), bezsenność (19,2% u pacjentów z PM, 11,3% u pacjentów EM), zaburzenia snu (6,9% u pacjentów z PM, 3,4% u pacjentów EM), bezsenność centralna (5,4% u pacjentów z PM, 2,7% u pacjentów EM), bezsenność końcowa (3% u pacjentów z PM, 0,9% u pacjentów z EM), zatrzymanie moczu (5,9% u pacjentów z PM, 1,2% u pacjentów EM), zaburzenia erekcji (20,9% u pacjentów z PM, 8,9% u pacjentów EM), zaburzenia wytrysku (6,1% u pacjentów z PM, 2,2% u pacjentów EM), nadmierna potliwość (14,8% u pacjentów z PM, 6,8% u pacjentów z EM), chłód obwodowy (3% u pacjentów z PM, 0,5% u pacjentów z EM).
Zgłaszanie podejrzewanych działań niepożądanych
Zgłaszanie podejrzewanych działań niepożądanych, które występują po dopuszczeniu produktu leczniczego do obrotu, jest ważne, ponieważ umożliwia ciągłe monitorowanie stosunku korzyści do ryzyka produktu leczniczego. Pracownicy służby zdrowia proszeni są o zgłaszanie wszelkich podejrzewanych działań niepożądanych za pośrednictwem Włoskiej Agencji Leków. , Strona internetowa: (http://www.agenziafarmaco.gov.it/it/responsabili).
04.9 Przedawkowanie
Symptomy i objawy:
W okresie po wprowadzeniu do obrotu zgłaszano przypadki ostrego i przewlekłego przedawkowania atomoksetyny stosowanej w monoterapii, które nie prowadziły do zgonu. Najczęściej zgłaszanymi ostrymi i przewlekłymi objawami przedawkowania były objawy żołądkowo-jelitowe, senność, zawroty głowy, drżenie i nieprawidłowe zachowanie. Zgłaszano również nadpobudliwość i pobudzenie. Obserwowano również objawy przedmiotowe i podmiotowe odpowiadające łagodnej do umiarkowanej aktywacji współczulnego układu nerwowego (np. tachykardia, podwyższone ciśnienie krwi, rozszerzenie źrenic, suchość w ustach) oraz zgłaszano przypadki świądu i wysypki. łagodne do umiarkowanego W niektórych przypadkach przedawkowania atomoksetyny zgłaszano drgawki i bardzo rzadko wydłużenie odstępu QT. Istnieją również doniesienia o śmiertelnych przypadkach ostrego przedawkowania związanego z przyjmowaniem atomoksetyny z co najmniej jednym innym lekiem.
Doświadczenie z przedawkowaniem atomoksetyny w badaniach klinicznych jest ograniczone.W badaniach klinicznych nie odnotowano przypadków śmiertelnego przedawkowania.
Leczenie przedawkowania:
Pacjentowi należy zapewnić sztuczną wentylację. W celu ograniczenia wchłaniania przydatny może być węgiel aktywowany, jeśli pacjent zgłosi się w ciągu 1 godziny od spożycia. Zaleca się monitorowanie parametrów życiowych i kardiologicznych wraz z odpowiednimi działaniami objawowymi i podtrzymującymi Pacjenta należy obserwować przez co najmniej 6 godzin Biorąc pod uwagę silne wiązanie atomoksetyny z białkami osocza, jest mało prawdopodobne, aby dializa była przydatna w leczeniu przedawkować.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE
05.1 Właściwości farmakodynamiczne
Grupa farmakoterapeutyczna: działające ośrodkowo sympatykomimetyki.
Kod ATC: N06BA09.
Mechanizm działania i efekty farmakodynamiczne
Atomoksetyna jest silnym i wysoce selektywnym inhibitorem presynaptycznego transportera norepinefryny, co stanowi jego rzekomy mechanizm działania, bez wywierania bezpośredniego wpływu na transportery serotoniny lub dopaminy Atomoksetyna ma minimalne powinowactwo do innych receptorów noradrenergicznych lub transporterów lub receptorów innych neuroprzekaźniki Dwa główne metabolity oksydacyjne atomoksetyny to 4-hydroksyatomoksetyna i N-desmetyloatomoksetyna.
4-hydroksyatomoksetyna ma taką samą siłę działania jak atomoksetyna jako inhibitor transportera norepinefryny, ale w przeciwieństwie do atomoksetyny, metabolit ten wywiera również działanie hamujące na transporter serotoniny.Jednak jakikolwiek wpływ na ten transporter jest prawdopodobnie minimalny, ponieważ większość 4-hydroksyatomoksetyny hydroksyatomoksetyna jest dalej metabolizowana, dlatego występuje w osoczu w bardzo małych stężeniach (1% stężenia atomoksetyny u pacjentów szybko metabolizujących i 0,1% stężenia atomoksetyny u osób słabo metabolizujących). N-desmetyloatomoksetyna ma znacznie niższą aktywność farmakologiczną niż atomoksetyna. -oznacza, że jest obecna w osoczu w stężeniach niższych niż atomoksetyna u osób intensywnie metabolizujących oraz w stężeniach porównywalnych do stężenia atomoksetyny u osób wolno metabolizujących.
Atomoksetyna nie jest środkiem psychostymulującym i nie jest pochodną amfetaminy.W randomizowanym, podwójnie zaślepionym badaniu z grupą kontrolną otrzymującą placebo u dorosłych, mającym na celu ocenę możliwości nadużywania poprzez porównanie działania atomoksetyny z działaniem placebo, atomoksetyna nie była powiązana z wzorcem reakcji, który sugeruje właściwości stymulujące lub euforyczne.
Skuteczność kliniczna i bezpieczeństwo
Populacja pediatryczna
W badaniach klinicznych Strattera wzięło udział ponad 5000 dzieci i młodzieży z ADHD. Ostrą skuteczność Strattery w leczeniu ADHD ustalono początkowo w sześciu randomizowanych, podwójnie zaślepionych, kontrolowanych placebo badaniach trwających od sześciu do dziewięciu tygodni.
Objawy przedmiotowe i podmiotowe ADHD oceniano porównując średnie zmiany od punktu początkowego do punktu końcowego u pacjentów leczonych produktem Strattera i pacjentów otrzymujących placebo. W każdym z sześciu badań atomoksetyna była statystycznie istotnie skuteczniejsza niż placebo pod względem zmniejszania objawów ADHD.
Ponadto skuteczność atomoksetyny w utrzymaniu odpowiedzi na objawy wykazano w rocznym badaniu kontrolowanym placebo, przeprowadzonym głównie w Europie z udziałem ponad 400 dzieci i młodzieży (ostre otwarte leczenie przez około 3 miesiące, a następnie 9 miesięcy podwójnie ślepej próby leczenie podtrzymujące w porównaniu z placebo). Odsetek pacjentów, u których doszło do nawrotu po 1 roku, wynosił odpowiednio 18,7% w grupie atomoksetyny i 31,4% w grupie placebo. Po roku leczenia atomoksetyną u pacjentów, którzy kontynuowali leczenie atomoksetyną przez dodatkowe 6 miesięcy, prawdopodobieństwo nawrotu lub częściowego nawrotu objawów było mniejsze niż u pacjentów, którzy przerwali aktywne leczenie i przeszli na placebo (odpowiednio 2% w porównaniu z 12%). Podczas długotrwałego leczenia należy okresowo oceniać odpowiedź na trwające leczenie u dzieci i młodzieży.
Strattera była skuteczna w pojedynczej dawce dobowej oraz w dwóch oddzielnych podaniach, jednej rano i drugiej późnym popołudniem/wczesnym wieczorem. Strattera podawana jako pojedyncza dawka dobowa wykazała statystycznie istotnie większe zmniejszenie nasilenia objawów ADHD w porównaniu z placebo, zgodnie z oceną nauczycieli i rodziców.
Europejska Agencja Leków odroczyła obowiązek przedstawienia wyników badań leku Strattera w podgrupie populacji pediatrycznej w wieku od 4 do 6 lat w leczeniu ADHD (informacje dotyczące stosowania u dzieci, patrz punkt 4.2).
Badania z aktywnym komparatorem
W 6-tygodniowym, randomizowanym, podwójnie zaślepionym badaniu pediatrycznym prowadzonym w grupach równoległych w celu oceny równoważności atomoksetyny ze standardowym lekiem porównawczym, takim jak metylofenidat o przedłużonym uwalnianiu, wykazano, że lek porównawczy wiązał się z wyższym wskaźnikiem odpowiedzi niż w przypadku atomoksetyna. Odsetek pacjentów sklasyfikowanych jako reagujący wyniósł 23,5% (placebo), 44,6% (atomoksetyna) i 56,4% (metylofenidat). Zarówno atomoksetyna, jak i lek porównawczy były statystycznie lepsze niż placebo, a metylofenidat był statystycznie lepszy od atomoksetyny (p = 0,016).Jednak z tego badania wykluczono pacjentów, którzy nie reagowali na stymulanty.
Populacja dorosłych
Strattera badano u ponad 4800 dorosłych, którzy spełniali kryteria diagnostyczne DSM-IV dla „ADHD. Ostrą skuteczność Strattera w leczeniu dorosłych ustalono w sześciu randomizowanych, podwójnie zaślepionych, kontrolowanych placebo badaniach, trwających od dziesięciu do szesnaście tygodni. Objawy przedmiotowe i podmiotowe ADHD oceniano porównując średnie zmiany od punktu początkowego do punktu końcowego u pacjentów leczonych atomoksetyną i pacjentów otrzymujących placebo. W każdym z sześciu badań atomoksetyna była statystycznie istotnie skuteczniejsza niż placebo w zmniejszaniu objawów ADHD (tabela X). U pacjentów leczonych atomoksetyną zaobserwowano statystycznie istotnie większą poprawę pod względem ogólnego klinicznego wrażenia ciężkości (skala CGI-S) po punkt końcowy w porównaniu z pacjentami otrzymującymi placebo we wszystkich 6 ostrych badaniach i miał statystycznie istotnie większą poprawę funkcjonowania związanego z ADHD we wszystkich 3 ostrych badaniach, w których to oceniano (tabela X). , badania kontrolowane placebo, ale nie wykazano ich w trzecim badaniu (Tabela X).
Tabela X Średnie zmiany wskaźników skuteczności w badaniach kontrolowanych placebo
Skróty: AAQoL = całkowity wynik skali jakości życia dorosłych z ADHD; AISRS = całkowity wynik w skali oceny objawów badacza dla dorosłych z ADHD; ATX = atomoksetyna; CAARS-Inv: SV = skala Connersa dla dorosłych z ADHD (badacz): wersja przesiewowa (Conners Adult ADHD Rating Scale, Investigator Rated, screening version Total ADHD Symptom Score); CGI-S = Ogólne kliniczne wrażenie ciężkości; LOCF = Ostatnia obserwacja zakończona; PBO = placebo.
a: Skale objawów ADHD; wyniki przedstawione w badaniu LYBY są zgodne ze skalą AISRS; wyniki wszystkich innych badań są zgodne ze skalą CAARS-Inv: SV.
W analizach wrażliwości, w których wykorzystano „zakończoną obserwację podstawową (metoda bazowa-obserwacja-przeniesienie-przeniesienie) dla pacjentów bez pomiaru po punkcie wyjściowym (tj. wszystkich leczonych pacjentów). Wyniki były zgodne z wynikami przedstawionymi w Tabeli X.
W klinicznie istotnych analizach odpowiedzi we wszystkich 6 ostrych badaniach oraz w obu zakończonych sukcesem badaniach długoterminowych, z zastosowaniem różnych definicji a priori i post hoc, pacjenci leczeni atomoksetyną konsekwentnie mieli wyższy wskaźnik odpowiedzi w statystycznie istotnie większym stopniu w porównaniu z pacjentami otrzymującymi placebo (Tabela Y).
Tabela Y Liczba (n) i odsetek pacjentów spełniających kryteria odpowiedzi w zbiorczych badaniach kontrolowanych placebo
a Obejmuje wszystkie badania w Tabeli X z wyjątkiem: Analiza ostrej odpowiedzi CGI-S wyklucza 2 badania u pacjentów ze współistniejącymi chorobami (LYBY, LYDQ); Analiza ostrej odpowiedzi CAARS wyklucza 1 badanie, w którym nie zastosowano skali CAARS (LYBY).
W dwóch ostrych badaniach u pacjentów ze współwystępującym alkoholizmem lub zaburzeniami lęku społecznego w obu badaniach nastąpiła poprawa objawów ADHD. W badaniu dotyczącym lęku współistniejącego stan lęku współistniejącego nie uległ pogorszeniu po leczeniu atomoksetyną.
Skuteczność atomoksetyny w utrzymaniu odpowiedzi objawowej wykazano w badaniu, w którym po początkowym 24-tygodniowym okresie aktywnego leczenia pacjenci spełniali kryteria klinicznie istotnej odpowiedzi (określanej jako poprawa wyniku zarówno w skali CAARS-Inv: SV, jak i CGI-S) zostali losowo przydzieleni do grupy otrzymującej atomoksetynę lub placebo przez dodatkowe 6 miesięcy leczenia metodą podwójnie ślepej próby. Pod koniec 6 miesięcy pacjenci spełniali kryteria utrzymania klinicznie istotnej odpowiedzi. wyższy odsetek pacjentów leczonych atomoksetyną niż placebo ( 64,3% vs 50,0%; p = 0,001) Pacjenci leczeni atomoksetyną wykazywali statystycznie istotnie lepsze utrzymanie funkcjonowania niż pacjenci leczeni placebo, na co wskazywała mniejsza średnia zmiana całkowitego wyniku w skali jakości życia ADHD ( YYQoL) w trzecim miesiącu (p = 0,003) iw szóstym miesiącu (p = 0,002).
Badanie QT/QTc
Dogłębne badanie QT/QTc przeprowadzone u zdrowych dorosłych pacjentów ze słabym metabolizmem (PM) CYP2D6 leczonych dawkami do 60 mg atomoksetyny dwa razy na dobę wykazało, że przy maksymalnych oczekiwanych stężeniach wpływ atomoksetyny na „odstęp QTc” nie różnił się istotnie w porównaniu z placebo. Wystąpił niewielki wzrost odstępu QTc wraz ze wzrostem stężenia atomoksetyny”.
05.2 Właściwości farmakokinetyczne
Farmakokinetyka atomoksetyny u dzieci i młodzieży jest podobna do farmakokinetyki u dorosłych. Nie oceniano farmakokinetyki atomoksetyny u dzieci w wieku poniżej sześciu lat.
Wchłanianie: Atomoksetyna jest szybko i prawie całkowicie wchłaniana po podaniu doustnym, osiągając średnie maksymalne obserwowane stężenie w osoczu (Cmax) po około 1-2 godzinach po podaniu. Całkowita biodostępność atomoksetyny po podaniu doustnym waha się od 63% do 94%, w zależności od różnic międzyosobniczych w umiarkowanym metabolizmie pierwszego przejścia. Atomoksetynę można przyjmować z jedzeniem lub bez jedzenia.
Dystrybucja: Atomoksetyna jest szeroko rozpowszechniona i silnie wiąże się (98%) z białkami osocza, głównie albuminami.
Biotransformacja: Atomoksetyna jest metabolizowana głównie przez układ enzymatyczny cytochromu P450 2D6 (CYP2D6). Osoby o zmniejszonej aktywności tego szlaku metabolicznego (osoby słabo metabolizujące) stanowią około 7% populacji rasy kaukaskiej i mają wyższe stężenia atomoksetyny w osoczu niż osoby o prawidłowej aktywności (osoby intensywnie metabolizujące).
U pacjentów ze słabym metabolizmem AUC atomoksetyny jest około 10 razy większe, a Cssmax około 5 razy większe niż u pacjentów z szybkim metabolizmem. Głównym metabolitem oksydacyjnym, który powstaje, jest 4-hydroksyatomoksetyna, która jest szybko glukuronidowana. ale jest obecny we krwi w znacznie niższych stężeniach. Chociaż 4-hydroksyatomoksetyna jest tworzona głównie przez CYP2D6, u osób pozbawionych aktywności CYP2D6 4-hydroksyatomoksetyna może być tworzona przez kilka innych enzymów cytochromu P450, ale w wolniejszym tempie. Atomoksetyna w dawkach terapeutycznych nie hamuje jej ani nie indukuje CYP2D6.
Enzymy cytochromu P450: Atomoksetyna nie powodowała klinicznie istotnego hamowania ani indukcji enzymów cytochromu P450, w tym CYP1A2, CYP3A, CYP2D6 i CYP2C9.
Eliminacja: Średni okres półtrwania w fazie eliminacji atomoksetyny po podaniu doustnym wynosi 3,6 godziny u osób intensywnie metabolizujących i 21 godzin u osób słabo metabolizujących. Atomoksetyna jest wydalana głównie w postaci 4-hydroksyatomoksetyny-LUB-glukuronid, głównie w moczu.
Liniowość / nieliniowość: profile farmakokinetyczne atomoksetyny są liniowe w zakresie dawek badanych zarówno u osób intensywnie, jak i wolno metabolizujących.
Populacje specjalne
Uszkodzenie wątroby prowadzi do zmniejszonego klirensu atomoksetyny, „zwiększonej ekspozycji na” atomoksetynę (2-krotny wzrost AUC w umiarkowanym uszkodzeniu wątroby i 4-krotny wzrost w ciężkim uszkodzeniu wątroby), „wydłużony okres półtrwania leku w porównaniu ze zdrowymi osobnikami kontrolnymi o tym samym genotypie co szybko metabolizujący CYP2D6. U pacjentów z umiarkowanymi lub ciężkimi zaburzeniami czynności wątroby (klasa B i C w skali Child-Pugh) należy dostosować dawkę początkową i podtrzymującą (patrz punkt 4.2).
Średnie stężenia atomoksetyny w osoczu u osób ze schyłkową niewydolnością nerek (ESRD) były na ogół wyższe niż średnie stężenia w osoczu u zdrowych osób z grupy kontrolnej, o czym świadczy wzrost Cmax (różnica 7%) i AUC0-? (różnica około 65%) Po dostosowaniu do masy ciała różnice między tymi dwiema grupami są zminimalizowane.Profile farmakokinetyczne atomoksetyny i jej metabolitów u osób z ESRD sugerują, że nie jest konieczne dostosowanie dawki (patrz punkt 4.2).
05.3 Przedkliniczne dane o bezpieczeństwie
Dane niekliniczne wynikające z konwencjonalnych badań dotyczących bezpieczeństwa, farmakologii, toksyczności po podaniu wielokrotnym, genotoksyczności, rakotwórczości lub toksyczności reprodukcyjnej i rozwojowej nie wykazały szczególnego zagrożenia dla człowieka. u zwierząt, wraz z obserwowanymi różnicami metabolicznymi między gatunkami, maksymalne tolerowane dawki u zwierząt stosowanych w badaniach nieklinicznych powodowały ekspozycję na atomoksetynę podobną lub nieco wyższą niż uzyskiwana u pacjentów ze słabym metabolizmem CYP2D6 przy maksymalnej zalecanej dawce dobowej.
Przeprowadzono badanie na młodych szczurach w celu oceny wpływu atomoksetyny na wzrost oraz rozwój neurobehawioralny i płciowy Łagodne opóźnienia w dojrzewaniu drożności pochwy (wszystkie dawki) i oddzieleniu napletka (obserwowano ≥ 10 mg/kg mc./dobę), niewielkie zmniejszenie masy najądrza i liczby plemników (≥ 10 mg / kg / dzień); nie stwierdzono jednak wpływu na płodność ani zdolność reprodukcyjną. Znaczenie tych odkryć dla ludzi nie jest znane.
Ciężarne króliki leczono atomoksetyną w dawkach do 100 mg/kg mc./dobę podawaną przez ssać w okresie organogenezy. Przy tej dawce w 1 z 3 badań zaobserwowano zmniejszenie liczby urodzeń żywych płodów, zwiększenie wczesnej resorpcji, niewielki wzrost częstości występowania nietypowego pochodzenia tętnicy szyjnej oraz przy braku tętnicy podobojczykowej. Efekty te były obserwowane przy dawkach, które powodowały łagodną toksyczność matczyną. Częstość występowania tych efektów mieści się w historycznych wartościach kontrolnych. Dawka bez efektu dla tych wyników wynosiła 30 mg / kg / dzień. Ekspozycja na niezwiązaną atomoksetynę w osoczu (AUC) u królików w dawkach 100 mg/kg/dobę była około 3,3-krotna (u osób intensywnie metabolizujących CYP2D6) i 0,4-krotnie (osoby słabo metabolizujące CYP2D6) w porównaniu z ekspozycją u mężczyzn przy maksymalnej dawce dobowej 1,4 mg / kg / dzień. Wyniki jednego z trzech badań na królikach były niejednoznaczne, a ich znaczenie dla ludzi nie jest znane.
06.0 INFORMACJE FARMACEUTYCZNE
06.1 Zaróbki
Skrobia żelowana (kukurydziana)
Dimetikon
Powłoka kapsułki:
Laurylosiarczan sodu
Galaretka
Barwniki do osłonek kapsułek
10 mg: dwutlenek tytanu E171
18 mg: żółty tlenek żelaza E172
25 mg, 40 mg, 60 mg: FD&C Blue 2 (Indygotyna) E132 i Dwutlenek tytanu E171
80 mg i 100 mg: żółty tlenek żelaza E172, czerwony tlenek żelaza E172 i dwutlenek tytanu E171
Barwniki powłoki ciała kapsułek
10 mg, 18 mg i 25 mg i 80 mg: Dwutlenek tytanu E171
40 mg: FD&C Blue 2 (Indygotyna) E132 i Dwutlenek tytanu E171
60 mg: żółty tlenek żelaza E172
100 mg: żółty tlenek żelaza E172, czerwony tlenek żelaza E172 i dwutlenek tytanu E171
Jadalny czarny tusz SW-9008 (zawierający szelak i czarny tlenek żelaza E172) lub jadalny czarny tusz SW-9010 (zawierający szelak i czarny tlenek żelaza E172).
06.2 Niekompatybilność
Nieistotne.
06.3 Okres ważności
3 lata
06.4 Specjalne środki ostrożności przy przechowywaniu
Ten produkt leczniczy nie wymaga żadnych specjalnych warunków przechowywania.
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania
Blistry z polichlorku winylu (PVC) / polietylenu (PE) / polichlorotrifluoroetylenu (PCTFE) zamknięte folią aluminiową.
Dostępny w opakowaniach po 7, 14, 28 i 56 kapsułek. Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
06.6 Instrukcje użytkowania i obsługi
Kapsułek nie wolno otwierać. Atomoksetyna działa drażniąco na oczy.W przypadku kontaktu zawartości kapsułek z oczami, chore oko należy natychmiast przemyć wodą i zasięgnąć porady lekarskiej. Ręce i wszelkie potencjalnie skażone powierzchnie należy jak najszybciej umyć.
07.0 PODMIOT POZWOLENIA NA DOPUSZCZENIE DO OBROTU
Eli Lilly Italia S.p.A.
Via Gramsci 731/733
Sesto Fiorentino (FI)
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
STRATTERA 10 mg kapsułki twarde, 7 kapsułek twardych: AIC N. 037063056
STRATTERA 10 mg kapsułki twarde, 14 kapsułek twardych: AIC N. 037063068
STRATTERA 10 mg kapsułki twarde, 28 kapsułek twardych: AIC N. 037063070
STRATTERA 10 mg kapsułki twarde, 56 kapsułek twardych: AIC N. 037063082
STRATTERA 18 mg kapsułki twarde, 7 kapsułek twardych: AIC N. 037063094
STRATTERA 18 mg kapsułki twarde, 14 kapsułek twardych: AIC N. 037063106
STRATTERA 18 mg kapsułki twarde, 28 kapsułek twardych: AIC N. 037063118
STRATTERA 18 mg kapsułki twarde, 56 kapsułek twardych: AIC N. 037063120
STRATTERA 25 mg kapsułki twarde, 7 kapsułek twardych: AIC N. 037063132
STRATTERA 25 mg kapsułki twarde, 14 kapsułek twardych: AIC N. 037063144
STRATTERA 25 mg kapsułki twarde, 28 kapsułek twardych: AIC N. 037063157
STRATTERA 25 mg kapsułki twarde, 56 kapsułek twardych: AIC N. 037063169
STRATTERA 40 mg kapsułki twarde, 7 kapsułek twardych: AIC N. 037063171
STRATTERA 40 mg kapsułki twarde, 14 kapsułek twardych: AIC N. 037063183
STRATTERA 40 mg kapsułki twarde, 28 kapsułek twardych: AIC N. 037063195
STRATTERA 40 mg kapsułki twarde, 56 kapsułek twardych: AIC N. 037063207
STRATTERA 60 mg kapsułki twarde, 7 kapsułek twardych: AIC N. 037063219
STRATTERA 60 mg kapsułki twarde, 14 kapsułek twardych: AIC N. 037063221
STRATTERA 60 mg kapsułki twarde, 28 kapsułek twardych: AIC N. 037063233
STRATTERA 60 mg kapsułki twarde, 56 kapsułek twardych: AIC N. 037063245
STRATTERA 80 mg kapsułki twarde, 7 kapsułek twardych: AIC N. 037063258
STRATTERA 80 mg kapsułki twarde, 14 kapsułek twardych: AIC N. 037063260
STRATTERA 80 mg kapsułki twarde, 28 kapsułek twardych: AIC N. 037063272
STRATTERA 80 mg kapsułki twarde, 56 kapsułek twardych: AIC N. 037063284
STRATTERA 100 mg kapsułki twarde, 7 kapsułek twardych: AIC N. 037063296
STRATTERA 100 mg kapsułki twarde, 14 kapsułek twardych: AIC N. 037063308
STRATTERA 100 mg kapsułki twarde, 28 kapsułek twardych: AIC N. 037063310
STRATTERA 100 mg kapsułki twarde, 56 kapsułek twardych: AIC N. 037063322
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA
19 kwietnia 2007
10.0 DATA ZMIAN TEKSTU
Rezolucja AIFA z dnia 3 listopada 2014 r.