Co to jest Targretin?
Targretin to lek zawierający substancję czynną beksaroten. Preparat jest dostępny w postaci białych miękkich kapsułek (75 mg).
W jakim celu stosuje się Targretin?
Targretin stosuje się w leczeniu objawów skórnych widocznych u pacjentów ze skórnym chłoniakiem T-komórkowym (CTCL). Chłoniak skórny z komórek T jest rzadkim typem chłoniaka (nowotworu tkanki limfatycznej), który pojawia się, gdy w skórze rośnie określony rodzaj białych krwinek (komórek T). Targretin stosuje się u pacjentów z zaawansowaną chorobą, u których nie wystąpiła odpowiedź na co najmniej jedno wcześniejsze leczenie.
Lek jest dostępny wyłącznie na receptę.
Jak stosuje się Targretin?
Terapię Targretin powinni rozpoczynać i kontynuować wyłącznie lekarze mający doświadczenie w leczeniu pacjentów z chłoniakiem skóry z limfocytów T. Dawka preparatu Targretin zależy od powierzchni ciała pacjenta mierzonej w metrach kwadratowych (m2). Zalecana dawka początkowa to 300 mg/m2/dobę. Dawkę można dostosować w zależności od reakcji pacjenta na leczenie lub skutków ubocznych. Terapię należy kontynuować tak długo, jak długo pacjent z niej korzysta. Więcej informacji można znaleźć w Charakterystyce Produktu Leczniczego zawartej w EPAR.
Kapsułki Targretin należy przyjmować w pojedynczej dawce dobowej, podczas posiłku.
Jak działa Targretin?
Substancja czynna preparatu Targretin, beksaroten, jest środkiem przeciwnowotworowym należącym do grupy retinoidów, substancji pochodzących z witaminy A. Dokładny mechanizm działania beksarotenu w CTCL nie jest znany.
Jak badano Targretin?
Skuteczność preparatu Targretin zbadano w dwóch badaniach z udziałem łącznie 193 pacjentów z CTCL, u których nie wystąpiła odpowiedź na co najmniej dwa poprzednie terapie.Badania te nie obejmowały grupy kontrolnej (tj. Targretin nie był porównywany z innym lekiem lub placebo). 93 z tych pacjentów było w zaawansowanym stadium choroby i było opornych na inne leczenie 61 pacjentów było leczonych dawką początkową 300 mg/m2/dobę Główną miarą skuteczności była odpowiedź na leczenie po 16 tygodniach, mierzona ocena przez lekarza poprawy EMEA 2007 oraz wynik uzyskany na podstawie 5 objawów klinicznych (obszar dotknięty chorobą, zaczerwienienie, wypukłości, łuszcząca się skóra i przebarwienia).
Jakie korzyści wykazał Targretin podczas badań?
W obu badaniach około połowa pacjentów leczonych dawką 300 mg/m2 odpowiedziała na leczenie, zgodnie z oceną lekarza, odpowiednio następujące wartości procentowe: 36% i 27%.
Jakie jest ryzyko związane z Targretinem?
Najczęściej obserwowanymi działaniami niepożądanymi związanymi ze stosowaniem Targretin (u więcej niż 1 na 10 pacjentów) są leukopenia (spadek liczby białych krwinek we krwi), niedoczynność tarczycy (niedostateczna aktywność tarczycy), hiperlipemia (wysoki poziom tłuszczu we krwi). ), hipercholesterolemia (wysoki poziom cholesterolu we krwi), złuszczające zapalenie skóry (łuszczenie się skóry), świąd, rumień, ból, ból głowy i osłabienie (osłabienie).
Preparatu Targretin nie należy stosować u pacjentów, u których może występować nadwrażliwość (uczulenie) na beksaroten lub którąkolwiek z pozostałych substancji. Preparatu Targretin nie należy również podawać:
- kobiety w ciąży lub karmiące piersią;
- kobiety, które mogą zajść w ciążę;
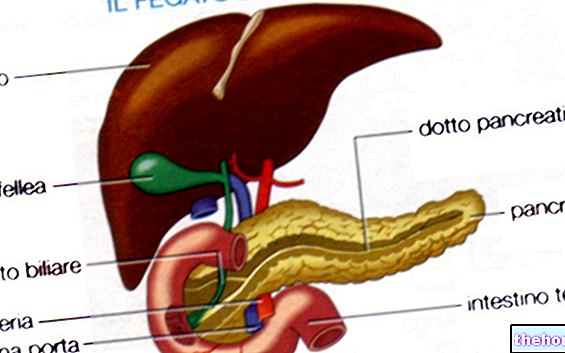
- osoby, które w przeszłości cierpiały na zapalenie trzustki (zapalenie trzustki);
- osoby z niekontrolowaną hipercholesterolemią (wysoki poziom cholesterolu we krwi);
- osoby z niekontrolowaną hipertriglicerydemią (wysoki poziom trójglicerydów [tłuszczów] we krwi);
- osoby z hiperwitaminozą A (wysoki poziom witaminy A w organizmie);
- osoby z niekontrolowaną chorobą tarczycy;
- osoby z chorobą wątroby;
osoby z trwającą infekcją.
Dlaczego Targretin został zatwierdzony?
Komitet ds. Produktów Leczniczych Stosowanych u Ludzi (CHMP) uznał, że korzyści płynące ze stosowania preparatu Targretin przewyższają ryzyko w leczeniu objawów skórnych u pacjentów z zaawansowanym chłoniakiem skórnym T-komórkowym opornym na co najmniej jedno leczenie ogólnoustrojowe, i w związku z tym zalecił wydanie „zezwolenie na wprowadzenie produktu do obrotu”.
Inne informacje o Targretin:
W dniu 29 marca 2001 r. Komisja Europejska wydała „Pozwolenie na dopuszczenie do obrotu" dla Targretin, ważne na terenie całej Unii Europejskiej. „Pozwolenie na dopuszczenie do obrotu" zostało odnowione w dniu 29 marca 2006 r. Podmiotem odpowiedzialnym „wprowadzającym do obrotu jest firma Eisai Ltd.
Aby zobaczyć pełną wersję EPAR firmy Targretin, kliknij tutaj.
Ostatnia aktualizacja niniejszego podsumowania: 03-2007.
Informacje na temat Targretin - beksaroten opublikowane na tej stronie mogą być nieaktualne lub niekompletne. Aby prawidłowo wykorzystać te informacje, zobacz stronę Wyłączenie odpowiedzialności i przydatne informacje.






-cos-cause-e-come-superarla.jpg)