Składniki aktywne: Brywudyna
Brivirac 125 mg tabletki
Dlaczego stosuje się Brivirac? Po co to jest?
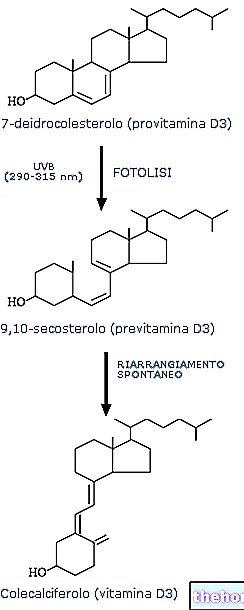
Brivirac zawiera substancję czynną brywudynę. Brivirac ma działanie przeciwwirusowe i zapobiega namnażaniu się wirusa wywołującego Ogień Św. Antoniego (wirus ospy wietrznej i półpaśca).
Brivirac stosuje się we wczesnym leczeniu Ognia Św.
Przeciwwskazania Kiedy nie należy stosować leku Brivirac
Nie przyjmować leku Brivirac
- jeśli pacjent ma uczulenie (nadwrażliwość) na substancję czynną brywudynę
- jeśli u pacjenta stwierdzono uczulenie (nadwrażliwość) na którykolwiek z pozostałych składników leku Brivirac (patrz punkt 6)
- jeśli jesteś w ciąży lub karmisz piersią
- jeśli masz mniej niż 18 lat.
W szczególności NIE NALEŻY przyjmować leku Brivirac:
- jeśli pacjent przyjmuje leki przeciwnowotworowe (chemioterapia), w szczególności jeśli jest leczony:
- 5-fluorouracyl (zwany również 5-FU, substancja czynna należąca do grupy zwanej 5-fluoropirymidynami)
- kremy, maści, krople do oczu lub jakakolwiek inna postać leku do użytku zewnętrznego zawierająca 5-fluorouracyl
- składniki aktywne przekształcane przez organizm w 5-fluorouracyl, takie jak:
- kapecytabina
- floksurydyna
- tegafur
- jakikolwiek inny składnik aktywny z grupy 5-fluoropirymidyn
- skojarzenia wyżej wymienionych składników aktywnych
- jeśli twój układ odpornościowy (tj. obrona twojego organizmu przed infekcjami) jest poważnie osłabiony; np. jeśli pacjent jest leczony:
- leki przeciwnowotworowe (chemioterapia) lub
- leki immunosupresyjne (tj. leki hamujące lub osłabiające czynność układu odpornościowego)
- jeśli pacjent przyjmuje lek zawierający flucytozynę w leczeniu zakażenia grzybiczego.
- jeśli pacjent przyjmuje lek na brodawki zawierający substancję czynną z grupy 5-fluoropirymidyn.
Środki ostrożności dotyczące stosowania Informacje ważne przed przyjęciem leku Brivirac
Przed rozpoczęciem przyjmowania leku Brivirac należy omówić to z lekarzem lub farmaceutą.
Nie należy przyjmować leku Brivirac razem z lekami zawierającymi 5-FU lub inne 5-fluoropirymidyny (patrz punkty „Kiedy nie stosować leku Brivirac” i „Inne leki i Brivirac”).
Nie należy stosować leku Brivirac, jeśli wysypka już w pełni rozwinęła się (początek strupów).W razie wątpliwości należy zwrócić się do lekarza.
Przed zastosowaniem leku Brivirac należy poradzić się lekarza, jeśli u pacjenta występuje przewlekła choroba wątroby (np. przewlekłe zapalenie wątroby).
Nie należy przyjmować leku Brivirac dłużej niż 7 dni, ponieważ wydłużenie czasu leczenia poza zalecany czas 7 dni zwiększa ryzyko wystąpienia zapalenia wątroby (patrz także punkt 4).
Dzieci i młodzież
Nie należy podawać leku Brivirac dzieciom i młodzieży w wieku od 0 do 18 lat, ponieważ nie badano bezpieczeństwa i skuteczności w tej grupie wiekowej.
Interakcje Jakie leki lub pokarmy mogą zmienić działanie leku Brivirac
Należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent przyjmuje, ostatnio przyjmował lub może przyjmować inne leki, w tym leki wydawane bez recepty.
PROSZĘ ZANOTOWAĆ:
Specjalne ostrzeżenie dla pacjentów leczonych produktami zawierającymi 5-fluorouracyl lub inne 5-fluoropirymidyny (patrz również czerwone pole powyżej):
Leku Brivirac nie należy stosować jednocześnie z jakimkolwiek lekiem chemioterapeutycznym zawierającym którąkolwiek z następujących substancji czynnych, ponieważ szkodliwe działanie tych leków może być znacznie nasilone i prowadzić do zgonu:
- 5-fluorouracyl, w tym formy do stosowania miejscowego
- kapecytabina
- floksurydyna
- tegafur
- inne 5-fluoropirymidyny
- kombinacje dowolnej z powyższych substancji z innymi składnikami aktywnymi.
Nie należy przyjmować leku Brivirac z lekami zawierającymi substancję czynną flucytozynę stosowaną w leczeniu zakażeń grzybiczych. Nie należy przyjmować leku Brivirac i natychmiast skontaktować się z lekarzem, jeśli:
- jest w trakcie terapii opartej na którymkolwiek z powyższych leków
- pacjent będzie leczony którymkolwiek z powyższych leków w ciągu 4 tygodni po zakończeniu leczenia lekiem Brivirac.
Jeśli pacjent przypadkowo przyjął lek Brivirac jednocześnie z którymkolwiek z leków wymienionych powyżej:
- przestań brać oba leki
- natychmiast skonsultować się z lekarzem. Może być konieczne udanie się do szpitala na leczenie.
Objawy i oznaki toksyczności 5-fluorouracylu spowodowane powyższymi interakcjami obejmują:
- złe samopoczucie; biegunka; zapalenie jamy ustnej i/lub wewnętrznej błony śluzowej jamy ustnej; zmniejszona liczba białych krwinek i zahamowanie czynności szpiku kostnego; wysypka i zaczerwienienie na całym ciele, z bolesną w dotyku skórą, a następnie duże pęcherze prowadzące do złuszczania dużych obszarów skóry (toksyczna nekroliza naskórka) (patrz także punkt 4).
- Doświadczenia po wprowadzeniu do obrotu wskazują na możliwą interakcję brywudyny z lekami dopaminergicznymi przeciwko chorobie Parkinsona, która może sprzyjać wystąpieniu napadu pląsawicy (nieprawidłowe, mimowolne ruchy przypominające taniec, w szczególności rąk, nóg i twarzy). Brivirac z jedzeniem i piciem Lek Brivirac można przyjmować z jedzeniem lub bez jedzenia.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
Ciąża i karmienie piersią
Przed zastosowaniem jakiegokolwiek leku należy zasięgnąć porady lekarza lub farmaceuty.
Nie stosować leku Brivirac w okresie ciąży.
Nie należy stosować leku Brivirac w okresie karmienia piersią. Substancja czynna leku Brivirac może przenikać do dziecka z mlekiem matki.
Prowadzenie i używanie maszyn
U niektórych pacjentów przyjmujących lek Brivirac obserwowano zawroty głowy i senność, chociaż niezbyt często. W przypadku zauważenia tych działań niepożądanych nie należy prowadzić pojazdów, obsługiwać maszyn ani wykonywać żadnych prac bez bezpiecznego podparcia. Zapytaj swojego lekarza o poradę.
Brivirac zawiera laktozę
Ten produkt leczniczy zawiera laktozę. Jeśli pacjent został poinformowany przez lekarza, że nie toleruje niektórych cukrów, powinien skontaktować się z lekarzem przed przyjęciem tego produktu leczniczego.
Dawka, sposób i czas podawania Jak stosować Brivirac: Dawkowanie
Lek należy zawsze stosować zgodnie z zaleceniami lekarza. Jeśli nie masz pewności, skonsultuj się z lekarzem lub farmaceutą.
Zalecana dawka to:
1 tabletka Brivirac 125 mg raz na dobę przez 7 dni.
Tabletkę Brivirac należy przyjmować mniej więcej o tej samej porze każdego dnia.
Brivirac można przyjmować z jedzeniem lub bez jedzenia.
Tabletkę należy połknąć w całości popijając odpowiednią ilością płynu, np. szklanka wody.
Leczenie należy rozpocząć jak najszybciej, co oznacza, że jeśli to możliwe, należy rozpocząć przyjmowanie leku Brivirac:
- w ciągu 3 dni od pojawienia się pierwszych skórnych oznak Ognia Św. Antoniego (wysypka) lub
- w ciągu 2 dni od pojawienia się pierwszych pęcherzy.
Zakończ 7-dniową kurację, nawet jeśli wcześniej poczujesz się lepiej.
Jeśli objawy utrzymują się lub nasilają w ciągu tygodnia leczenia, należy skontaktować się z lekarzem.
Przyjmowanie zwykłej dawki leku Brivirac zmniejsza ryzyko wystąpienia neuralgii popółpaścowej u pacjentów w wieku powyżej 50 lat. Neuralgia popółpaścowa to uporczywy ból, który po ustąpieniu wysypki rozwija się w obszarze wcześniej dotkniętym półpaścem.
Czas trwania leczenia
Ten lek jest przeznaczony do krótkotrwałego stosowania. Należy go przyjmować tylko przez 7 dni. Nie należy przyjmować tego leku w drugim cyklu leczenia.
Stosowanie u dzieci i młodzieży
Nie należy stosować leku Brivirac w wieku poniżej 18 lat.
Pominięcie przyjęcia leku Brivirac
W przypadku pominięcia tabletki o zwykłej porze, należy ją przyjąć tak szybko, jak sobie o tym przypomni.Następną tabletkę należy przyjąć następnego dnia mniej więcej o tej samej porze co dzień wcześniej.Kontynuować stosowanie nowej dawki do końca 7-dniowego cyklu cykl leczenia dni.
Nie należy stosować dawki podwójnej w celu uzupełnienia pominiętej tabletki.
W przypadku wielokrotnego zapominania o przyjęciu dawki dobowej należy poinformować o tym lekarza.
Przerwanie stosowania leku Brivirac
Nie należy przerywać stosowania leku Brivirac bez uprzedniej konsultacji z lekarzem.Aby leczenie było w pełni skuteczne, lek należy przyjmować przez 7 dni.W razie jakichkolwiek dalszych pytań dotyczących stosowania tego leku należy zwrócić się do lekarza lub farmaceuty.
Przedawkowanie Co zrobić w przypadku przyjęcia zbyt dużej dawki leku Brivirac
W przypadku zażycia większej liczby tabletek niż zalecana, należy skontaktować się z lekarzem. Zdecyduje, czy potrzebne są dalsze środki.
Skutki uboczne Jakie są skutki uboczne leku Brivirac
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Należy przerwać przyjmowanie leku Brivirac i natychmiast poinformować lekarza, jeśli u pacjenta wystąpi reakcja alergiczna z objawami przedmiotowymi i podmiotowymi, w tym swędzącą lub zaczerwienioną skórą (wysypką), wzmożoną potliwością, obrzękiem (rąk, stóp, twarzy, języka, warg, powiek lub krtani), trudnościami w oddychaniu (patrz także punkt 4) Objawy te mogą być ciężkie i wymagać natychmiastowej pomocy lekarskiej.
Następujące działania niepożądane były często obserwowane (mogą wystąpić nie częściej niż u 1 na 10 pacjentów):
- nudności (złe samopoczucie).
Następujące działania niepożądane obserwowano niezbyt często (mogą wystąpić nie częściej niż u 1 na 100 pacjentów):
- zmniejszenie liczby rodzaju białych krwinek (granulocytów)
- wzrost liczby niektórych rodzajów białych krwinek (eozynofile, limfocyty, monocyty)
- zmniejszenie liczby czerwonych krwinek (niedokrwistość)
- reakcje alergiczne, w tym:
- swędząca skóra (swędzenie)
- zaczerwienienie skóry (rumieniowa wysypka)
- zwiększona potliwość
- obrzęk: dłoni, stóp, twarzy, języka, ust, powiek, krtani (obrzęk krtani)
- kaszel, trudności w oddychaniu i (lub) duszność
- brak apetytu
- lęk
- bezsenność, senność
- bół głowy
- zawroty głowy
- zawroty głowy
- nieprawidłowe odczucia, takie jak pieczenie, drętwienie, mrowienie, najczęściej w rękach i nogach (parestezje)
- podwyższone ciśnienie krwi
- niestrawność (niestrawność), wymioty, ból brzucha
- biegunka
- nadmiar gazu w żołądku lub jelitach (wzdęcia)
- zaparcie
- przewlekła choroba wątroby z nagromadzeniem tłuszczu (stłuszczenie wątroby)
- zwiększenie stężenia we krwi niektórych substancji wytwarzanych przez wątrobę (wzrost enzymów wątrobowych)
- osłabienie, zmęczenie (zmęczenie)
- objawy grypopodobne (złe samopoczucie, gorączka, bóle i dreszcze)
Następujące działania niepożądane były rzadko obserwowane (mogą dotyczyć do 1 na 1000 pacjentów):
- niskie ciśnienie krwi
- zmniejszenie liczby płytek krwi
- halucynacje, majaczenie
- stan splątania
- drżenie
- zmienione poczucie smaku
- ból ucha
- zapalenie wątroby (zapalenie wątroby), zwiększenie stężenia bilirubiny we krwi
- ból kości
Zgłaszano również następujące działania niepożądane, chociaż ich częstość nie jest znana (częstość nie może być określona na podstawie dostępnych danych):
- utrata równowagi
- zapalenie naczyń krwionośnych (vasculitis)
- niewydolność wątroby o szybkim początku
- miejscowe zapalenie skóry występujące przez pewien czas w tym samym miejscu (wysypka utrwalona), zapalenie skóry z łuszczeniem się skóry (złuszczające zapalenie skóry), ciężka wysypka na całej powierzchni ciała i wewnątrz jamy ustnej z powodu reakcji alergicznej (rumień wielopostaciowy) owrzodzenie skóry, ust, oczu i narządów płciowych (zespół Stevensa Johnsona).
Zgłaszanie skutków ubocznych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe działania niepożądane niewymienione w tej ulotce, należy porozmawiać z lekarzem lub farmaceutą. Działania niepożądane można również zgłaszać bezpośrednio za pośrednictwem krajowego systemu zgłaszania pod adresem: http://www.agenziafarmaco.gov.it/it/responsabili Zgłaszanie działań niepożądanych może również pomóc w uzyskaniu dodatkowych informacji na temat bezpieczeństwa tego leku.
Wygaśnięcie i przechowywanie
Przechowywać w miejscu niedostępnym i niewidocznym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na pudełku i blistrze. Termin ważności odnosi się do ostatniego dnia tego miesiąca.
Blister przechowywać w opakowaniu zewnętrznym w celu ochrony leku przed światłem.
Nie należy wyrzucać żadnych leków do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa.Pomoże to chronić środowisko.
Termin ">Inne informacje
Co zawiera lek Brivirac
Substancją czynną jest brywudyna.
1 tabletka leku Brivirac zawiera 125 mg brywudyny.
Pozostałe składniki to:
- celuloza mikrokrystaliczna
- monohydrat laktozy
- powidon K 24-27
- stearynian magnezu
Jak wygląda lek Brivirac i co zawiera opakowanie
Tabletki Brivirac 125 mg są okrągłe, płaskie, białe lub prawie białe ze ściętymi krawędziami.
Tabletki znajdują się w blistrze w pudełku.
Brivirac jest dostępny w opakowaniach zawierających 1 i 7 tabletek oraz w opakowaniach zbiorczych zawierających 5 pudełek kartonowych, z których każde zawiera 7 tabletek.
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO -
BRIVIRAC 125 MG TABLETKI
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY -
1 tabletka zawiera 125 mg brywudyny.
Substancja pomocnicza o znanym działaniu: laktoza jednowodna. Każda tabletka zawiera 37 mg laktozy jednowodnej.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1
03.0 POSTAĆ FARMACEUTYCZNA -
Tablet
Białe lub prawie białe płaskie tabletki ze ściętymi krawędziami.
04.0 INFORMACJE KLINICZNE -
04.1 Wskazania terapeutyczne -
Wczesne leczenie ostrych infekcji półpaśca u dorosłych z prawidłową odpornością.
04.2 Dawkowanie i sposób podawania -
Dawkowanie
Dorośli: jedna tabletka Brivirac raz dziennie przez siedem dni.
Leczenie należy rozpocząć tak szybko, jak to możliwe, najlepiej w ciągu 72 godzin od wystąpienia pierwszych objawów skórnych (zwykle „wysypki”) lub 48 godzin od wystąpienia pierwszego pęcherza. Tabletki należy przyjmować codziennie mniej więcej o tej samej porze. Jeśli objawy utrzymują się lub nasilają w ciągu 7 dni leczenia, należy zalecić pacjentowi zwrócenie się o pomoc lekarską. Produkt przeznaczony do krótkotrwałego stosowania.
To leczenie zmniejsza również ryzyko wystąpienia neuralgii popółpaścowej u pacjentów w wieku powyżej 50 lat przy normalnej dawce wskazanej powyżej (1 tabletka leku Brivirac raz na dobę przez 7 dni).
Po pierwszym cyklu leczenia (7 dni) nie należy przeprowadzać drugiego kursu.
Populacje specjalne
Starsi pacjenci
Nie ma konieczności dostosowania dawkowania u pacjentów w wieku powyżej 65 lat.
Pacjenci z zaburzeniami czynności nerek lub wątroby
W konsekwencji zaburzenia czynności nerek lub wątroby nie obserwuje się znaczących zmian w ekspozycji ogólnoustrojowej na brywudynę, dlatego nie jest konieczne dostosowanie dawki u pacjentów z umiarkowaną lub ciężką niewydolnością nerek oraz u pacjentów z umiarkowaną lub ciężką niewydolnością wątroby (patrz także punkt 5.2).
Populacja pediatryczna
Brivirac jest przeciwwskazany u dzieci w wieku od 0 do 18 lat, ponieważ nie ustalono bezpieczeństwa i skuteczności w tej grupie wiekowej (patrz punkt 4.3).
Sposób podawania
Stosowanie doustne.
Spożycie pokarmu nie wpływa znacząco na wchłanianie brywudyny (patrz punkt 5.2).
04.3 Przeciwwskazania -
Produktu Brivirac nie wolno podawać w przypadku nadwrażliwości na substancję czynną lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1.
Pacjenci poddawani chemioterapii przeciwnowotworowej
Stosowanie produktu Brivirac jest przeciwwskazane u pacjentów poddawanych chemioterapii nowotworów, zwłaszcza leczonych 5-fluorouracylem (5 FU), w tym jego preparatami do stosowania miejscowego, jego prolekami (np. kapecytabina, floksurydyna, tegafur) oraz połączeniami zawierającymi te substancje czynne, lub inne 5-fluoropirymidyny (patrz również punkty 4.4 i 4.5).
Pacjenci poddawani terapii przeciwgrzybiczej flucytozyną
Stosowanie produktu Brivirac jest przeciwwskazane u pacjentów poddawanych terapii przeciwgrzybiczej flucytozyną, ponieważ jest to prolek 5-fluorouracylu (5 FU).
Pacjenci z obniżoną odpornością
Stosowanie produktu Brivirac jest przeciwwskazane u pacjentów z obniżoną odpornością, takich jak pacjenci poddawani chemioterapii przeciwnowotworowej, terapii immunosupresyjnej.
Dzieci
Nie ustalono bezpieczeństwa i skuteczności produktu Brivirac u dzieci, dlatego jego stosowanie nie jest wskazane.
Ciąża i karmienie piersią
Brivirac jest przeciwwskazany w okresie ciąży lub laktacji (patrz również punkt 4.6).
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania -
Brivirac i 5-fluorouracyl, w tym jego preparaty do stosowania miejscowego lub proleki (np. kapecytabina, floksurydyna, tegafur) lub połączenia zawierające te substancje czynne, oraz inne 5-fluoropirymidyny (np. flucytozyna) nie powinny być podawane jednocześnie i co najmniej 4 razy należy obserwować tygodnie przed rozpoczęciem leczenia lekami 5-fluoropirymidynowymi. Jako dodatkowy środek ostrożności należy monitorować aktywność enzymu DPD przed rozpoczęciem jakiegokolwiek leczenia 5-fluoropirymidyną u pacjentów, którym niedawno podawano Brivirac (patrz również punkty 4.5 i 4.8).
Brivirac nie powinien być stosowany, jeśli objawy skórne są już w pełni rozwinięte.
Brivirac należy stosować ostrożnie u pacjentów z przewlekłą chorobą wątroby, taką jak zapalenie wątroby. Dane uzyskane po wprowadzeniu produktu do obrotu wskazują, że przedłużanie leczenia poza zalecany okres 7 dni zwiększa ryzyko wystąpienia zapalenia wątroby (patrz także punkt 4.8).
Ponieważ laktoza jest obecna wśród substancji pomocniczych, pacjenci z rzadką dziedziczną nietolerancją galaktozy, niedoborem laktazy typu Lapp lub zespołem złego wchłaniania glukozy-galaktozy nie powinni przyjmować leku.
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji -
Przeciwwskazania do jednoczesnego stosowania 5-fluorouracylu (w tym jego preparatów do stosowania miejscowego i proleków, np. kapecytabiny, floksurydyny, tegafuru) lub innych 5-fluoropirymidyn, takich jak flucytozyna (patrz również punkt 4.3).
Ta interakcja, prowadząca do zwiększonej toksyczności fluoropirymidyny, jest potencjalnie śmiertelna.
Brywudyna, poprzez swój główny metabolit bromowinyluracyl (BVU), wywiera „nieodwracalne hamowanie dehydrogenazy dihydroksypirymidynowej (DPD), enzymu regulującego metabolizm zarówno naturalnych nukleozydów (np. tymidyny), jak i leków na bazie pirymidyny, takich jak 5-fluorouracyl (5 -FU): Konsekwencją hamowania enzymu jest nadmierna ekspozycja i zwiększona toksyczność 5-FU.
Badania kliniczne wykazały, że u zdrowych osób dorosłych poddawanych terapii opartej na produkcie Brivirac (125 mg raz na dobę przez 7 dni) całkowity powrót czynnościowy aktywności enzymu DPD następuje 18 dni po ostatnim podaniu.
Brivirac i 5-fluorouracyl lub inne 5-fluoropirymidyny, takie jak kapecytabina, floksurydyna i tegafur (lub połączenia zawierające te substancje czynne) lub flucytozyna nie powinny być podawane jednocześnie, a przed rozpoczęciem leczenia należy zachować minimalny odstęp 4 tygodni. 5-fluoropirymidyna. Jako dodatkowy środek ostrożności należy monitorować aktywność enzymu DPD przed rozpoczęciem jakiegokolwiek leczenia 5-fluoropirymidyną u pacjentów, którym niedawno podawano Brivirac.
W przypadku przypadkowego podania 5-FU lub leków pokrewnych pacjentom leczonym produktem Brivirac, należy odstawić oba leki i wdrożyć drastyczne środki w celu zmniejszenia toksyczności 5-FU. Zalecana jest natychmiastowa hospitalizacja i należy podjąć wszelkie środki, aby zapobiec zakażeniom ogólnoustrojowym i odwodnieniu. Do objawów toksyczności 5-FU należą nudności, wymioty, biegunka, aw ciężkich przypadkach zapalenie jamy ustnej, zapalenie błon śluzowych, toksyczna nekroliza naskórka, neutropenia i zahamowanie czynności szpiku kostnego.
Leki dopaminergiczne i/lub choroba Parkinsona
Doświadczenie po wprowadzeniu leku do obrotu wskazuje na możliwą interakcję brywudyny z lekami dopaminergicznymi przeciwko chorobie Parkinsona, prowadzącą do wywołania pląsawicy.
Inne informacje
Nie wykazano potencjału indukującego lub hamującego wątrobowego układu enzymatycznego P450.
Spożywanie pokarmu nie zmienia znacząco wchłaniania brywudyny.
04.6 Ciąża i karmienie piersią -
Brivirac jest przeciwwskazany podczas ciąży lub u kobiet karmiących piersią.
Badania na zwierzętach nie wykazały działania embriotoksycznego ani teratogennego. Toksyczny wpływ na płód zaobserwowano tylko przy dużych dawkach. Nie ustalono jednak bezpieczeństwa stosowania leku Brivirac u kobiet w ciąży.
Badania na zwierzętach wykazały, że brywudyna i jej główny metabolit bromowinyluracyl (BVU) przenikają do mleka.
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn -
Nie przeprowadzono badań dotyczących wpływu leku Brivirac na zdolność prowadzenia pojazdów i obsługiwania maszyn.Podczas prowadzenia pojazdów, obsługiwania maszyn lub pracy bez bezpiecznego podparcia należy wziąć pod uwagę, że w niektórych przypadkach zgłaszano zawroty głowy i senność (patrz punkt 4.8).
04.8 Działania niepożądane -
Podsumowanie profilu bezpieczeństwa
W badaniach klinicznych brywudynę podawano ponad 3900 pacjentom. Najpoważniejszą, ale rzadką reakcją było zapalenie wątroby.Reakcję tę obserwowano również podczas nadzoru po wprowadzeniu do obrotu.
Jedynym częstym działaniem niepożądanym były nudności (2,1%).Innymi najczęstszymi (niezbyt często i rzadko) działaniami niepożądanymi były te związane z zaburzeniami układu nerwowego i zaburzeniami psychicznymi SOC. Wpływ brywudyny na OUN wykazano również w danych z obserwacji po wprowadzeniu do obrotu .
Podczas klinicznego stosowania produktu obserwowano zaburzenia skóry i tkanki podskórnej, co również zostało podkreślone w danych z obserwacji po wprowadzeniu do obrotu.
Częstość występowania i rodzaj działań niepożądanych były porównywalne z tymi, o których wiadomo, że występują w przypadku innych nukleozydowych środków przeciwwirusowych należących do tej samej klasy.
Tabela podsumowująca działania niepożądane
W poniższej tabeli wymieniono działania niepożądane brywudyny pogrupowane według systemu według malejącego nasilenia.
Opis wybranych działań niepożądanych
Brywudyna może wchodzić w interakcje z chemioterapeutykami z klasy 5-fluoropirymidyn. Ta interakcja, która wywołuje zwiększoną toksyczność fluoropirymidyny, jest potencjalnie śmiertelna (patrz także 4.4 i 4.5).
Do objawów toksyczności 5-FU należą nudności, wymioty, biegunka oraz, w ciężkich przypadkach, zapalenie jamy ustnej, zapalenie błon śluzowych, toksyczna nekroliza naskórka, neutropenia i zahamowanie czynności szpiku kostnego (patrz również punkt 4.5).
Działania hepatotoksyczne występowały zarówno w badaniach klinicznych, jak i po wprowadzeniu produktu do obrotu.Obejmowały one cholestatyczne lub cytolityczne zapalenie wątroby, żółtaczkę cholestatyczną lub zwiększenie aktywności enzymów wątrobowych.Większość przypadków zapalenia wątroby rozpoczęła się w wieku od 3 do 28 dni po zakończeniu 7-dniowego dnia Dane po wprowadzeniu do obrotu wskazują, że przedłużanie leczenia poza zalecany okres 7 dni zwiększa ryzyko zapalenia wątroby.
Populacja pediatryczna
Nie badano brywudyny w populacji pediatrycznej i jej stosowanie u dzieci nie jest wskazane. Dlatego profil bezpieczeństwa w populacji pediatrycznej jest nieznany.
Zgłaszanie podejrzewanych działań niepożądanych
Zgłaszanie podejrzewanych działań niepożądanych występujących po dopuszczeniu produktu leczniczego do obrotu jest ważne, ponieważ umożliwia ciągłe monitorowanie stosunku korzyści do ryzyka produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem krajowego systemu zgłaszania. „adres www. agenziafarmaco.gov.it/it/responsabili.
04.9 Przedawkowanie -
Jak dotąd nie zgłoszono ostrego przedawkowania produktu Brivirac. Po zamierzonym lub przypadkowym przedawkowaniu należy zastosować odpowiednie leczenie objawowe i podtrzymujące.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE -
05.1 "Właściwości farmakodynamiczne -
Środek przeciwwirusowy
Kod ATC J05AB15
Brywudyna, substancja czynna leku Brivirac, jest jednym z najsilniejszych analogów nukleozydów hamujących replikację wirusa Varicella Zoster (VZV). Szczególnie wrażliwe są kliniczne szczepy VZV. W komórkach zakażonych wirusem brywudyna przechodzi szereg kolejnych fosforylacji, w wyniku których powstaje trifosforan brywudyny, który jest odpowiedzialny za hamowanie replikacji wirusa.Wewnątrzkomórkowa konwersja brywudyny do jej fosforylowanych pochodnych jest katalizowana przez enzymy kodowane przez wirusy, głównie kinazę tymidynową. w zakażonych komórkach, co wyjaśnia wysoką selektywność brywudyny wobec celów wirusowych. Trójfosforan brywudyny, raz utworzony w komórkach zakażonych wirusem, pozostaje wewnątrz komórek przez ponad 10 godzin i wchodzi w interakcję z wirusową polimerazą DNA.Ta interakcja powoduje silne zahamowanie replikacji wirusa.Mechanizm oporności opiera się na wirusowej kinazie tymidynowej (TK) Jednak w praktyce klinicznej wymogiem oporności jest przewlekłe leczenie przeciwwirusowe i niedobór odporności pacjenta, które są mało prawdopodobne we wskazanych wskazaniach i dawkowaniu.
Stężenie brywudyny zdolne do hamowania replikacji wirusa in vitro (IC50) odpowiada 0,001 μg/ml (zakres 0,0003 - 0,003 μg/ml). Tak więc brywudyna jest około 200 do 1000 razy silniejsza niż acyklowir i pencyklowir w hamowaniu replikacji VZV in vitro.Maksymalne stężenie brywudyny w osoczu (Cssmax) osób, które otrzymały proponowaną dawkę (125 mg raz na dobę) wynosi 1,7 mcg/ml (tj. 1000-krotność IC50 „in vitro”), a minimalne stężenie (Cssmin) wynosi 0,06 mcg/ml (tj. co najmniej 60-krotność IC50).Brywudyna miała bardzo szybki początek działania w warunkach wysokiego wzrostu wirusa, osiągając 50 % zahamowania replikacji wirusa w ciągu 1 godziny od ekspozycji na lek. Brywudyna wykazuje również działanie przeciwwirusowe u zwierząt doświadczalnych zakażonych wirusem małpim (małpy) lub wirusem opryszczki pospolitej typu I (myszy i świnki morskie).Brywudyna jest aktywna przeciwko wirusowi opryszczki pospolitej typu I, natomiast nie wykazuje znaczącej aktywności przeciwwirusowej przeciwko opryszczce pospolitej typu II .
Hamowanie replikacji wirusa podkreśla skuteczność produktu Brivirac w przyspieszaniu ustępowania objawów skórnych u pacjentów z początkowym stadium półpaśca.Wysokie działanie przeciwwirusowe brywudyny in vitro znajduje odzwierciedlenie w lepszej skuteczności klinicznej obserwowanej w porównawczych badaniach klinicznych z acyklowirem, dotyczących okres od rozpoczęcia leczenia do ostatniego wykwitu pęcherzykowego: średni czas został skrócony o 25% w przypadku brywudyny (13,5 godziny) w porównaniu z acyklowirem (18 godzin).
Ponadto względne ryzyko rozwoju neuralgii popółpaścowej (PHN) u pacjentów w wieku powyżej 50 lat z prawidłową odpornością, leczonych brywudyną na półpasiec, było o 25% mniejsze (33% pacjentów zgłosiło PHN) w porównaniu z acyklowirem (43% zgłoszonych pacjentów). PHN).
05.2 "Właściwości farmakokinetyczne -
Wchłanianie
Brywudyna jest szybko wchłaniana po podaniu doustnym produktu Brivirac. Biodostępność brywudyny wynosi około 30% doustnej dawki produktu Brivirac z powodu zwiększonego metabolizmu pierwszego przejścia. Średnie maksymalne stężenie brywudyny w osoczu w stanie stacjonarnym po podaniu doustnym dawki 125 mg produktu Brivirac wynosi 1,7 μg/ml i jest osiągane 1 godzinę po podaniu. Spożycie pokarmu nieznacznie opóźnia wchłanianie brywudyny, ale nie wpływa na całkowitą ilość wchłoniętego leku.
Dystrybucja
Brywudyna ulega znacznej dystrybucji do tkanek, na co wskazuje duża objętość dystrybucji (75 l). Brywudyna silnie wiąże się z białkami osocza (> 95%).
Biotransformacja
Brywudyna jest intensywnie i szybko metabolizowana przez enzym fosforylazy pirymidynowej, który rozszczepia węglowodany z wytworzeniem bromowinyluracylu (BVU), metabolitu bez aktywności wirustatycznej. wyższy niż związek macierzysty.
BVU jest dalej metabolizowany do kwasu uracyloctowego, głównego metabolitu polarnego wykrywanego w ludzkim moczu, ale niewykrywalnego w osoczu.
Eliminacja
Brywudyna jest skutecznie eliminowana przy całkowitym klirensie ciała 240 ml/min. Końcowy okres półtrwania brywudyny w osoczu wynosi około 16 h. Brywudyna jest wydalana z moczem (65% podanej dawki) głównie w postaci kwasu uracyloctowego i wielu polarnych związków mocznikopodobnych.Niezmieniona brywudyna stanowi mniej niż 1% dawki Brivirac wydalany z moczem. Parametry kinetyczne BVU pod względem końcowego okresu półtrwania i klirensu są tego samego rzędu wielkości co związek macierzysty.
Liniowość / nieliniowość
Kinetykę liniową obserwowano w zakresie dawek od 31,25 do 125 mg.
Stan stacjonarny dla brywudyny osiągany jest po 5 dniach codziennego podawania produktu Brivirac, bez oznak dalszej dalszej kumulacji.
Pacjenci w podeszłym wieku i pacjenci z zaburzeniami czynności nerek lub wątroby
Główne parametry kinetyczne (AUC, Cmax i końcowy okres półtrwania w osoczu) brywudyny mierzone u pacjentów w podeszłym wieku oraz u pacjentów z umiarkowanymi do ciężkich zaburzeniami czynności nerek (klirens kreatyniny między 26 a 50 ml/min/1,73 m² powierzchni ciała i klirens kreatyniny
05.3 Przedkliniczne dane o bezpieczeństwie -
Dane niekliniczne wynikające z konwencjonalnych badań farmakologicznych dotyczących bezpieczeństwa, genotoksyczności, potencjalnego działania rakotwórczego, toksycznego wpływu na reprodukcję nie ujawniają żadnego szczególnego zagrożenia dla ludzi w przypadku krótkotrwałego stosowania.
Przedkliniczne skutki ostrej i przewlekłej toksyczności obserwowano w badaniach krótkoterminowych przy narażeniu uznawanym za wystarczająco przewyższające maksymalne narażenie człowieka. krótkotrwałe leczenie ludzi. Docelowym narządem toksyczności u wszystkich gatunków wykorzystywanych w badaniach przedklinicznych była wątroba.
06.0 INFORMACJE FARMACEUTYCZNE -
06.1 Substancje pomocnicze -
Celuloza mikrokrystaliczna Laktoza jednowodna Powidon K 24-27 Magnezu stearynian
06.2 Niezgodność "-
Nieistotne.
06.3 Okres ważności "-
3 lata.
06.4 Specjalne środki ostrożności przy przechowywaniu -
Przechowywać blister w opakowaniu zewnętrznym w celu ochrony przed światłem.
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania -
a) Rodzaj pojemnika
Sztywny, nieprzezroczysty blister z folii PVC i folia aluminiowa.
b) Zawartość pojemnika
Oryginalne opakowanie zawierające 7 tabletek.
Opakowanie szpitalne zawierające 35 (5 x 7) tabletek.
Opakowanie próbek zawierające 1 tabletkę.
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
06.6 Instrukcje użytkowania i obsługi -
Niewykorzystany lek i odpady pochodzące z tego leku należy usunąć zgodnie z lokalnymi przepisami.
07.0 POSIADACZ „POZWOLENIA NA DOPUSZCZENIE DO OBROTU” -
Laboratori Guidotti S.p.A. - Via Livornese 897, Piza - La Vettola
Sprzedaż dealera: A. Menarini Industrie Farmaceutiche Riunite s.r.l. - Via Sette Santi 3, Florencja
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU -
AIC nr. 03572010 - „tabletki 125 mg” 7 tabletek w blistrze PVC/AL
AIC nr. 035700222 - "tabletki 125 mg" 35 (5x7) tabletek w blistrze PVC/AL
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA -
Data pierwszego zezwolenia: 06/07/2000
Data ostatniego przedłużenia: 06.07.2015
10.0 DATA ZMIAN TEKSTU -
Luty 2016