Co to jest Xgeva - denosumab?
Xgeva to roztwór do wstrzykiwań zawierający substancję czynną denosumab. Jest dostępny w fiolkach jednorazowego użytku zawierających 120 mg denosumabu.
W jakim celu stosuje się Xgeva - denosumab?
Preparat Xgeva stosuje się w zapobieganiu powikłaniom kostnym u osób dorosłych z guzami litymi, które rozprzestrzeniły się do kości.Powikłania te obejmują złamania, ucisk rdzenia kręgowego (gdy kość ściska rdzeń kręgowy) lub powikłania wymagające radioterapii lub zabiegu chirurgicznego.
Lek jest dostępny wyłącznie na receptę.
Jak stosuje się Xgeva - denosumab?
Produkt Xgeva podaje się raz na cztery tygodnie w postaci pojedynczego wstrzyknięcia podskórnego (120 mg) w udo, brzuch lub ramię.W trakcie leczenia produktem Xgeva pacjenci powinni otrzymywać dodatkowo wapń i witaminę D.
Jak działa Xgeva - denosumab?
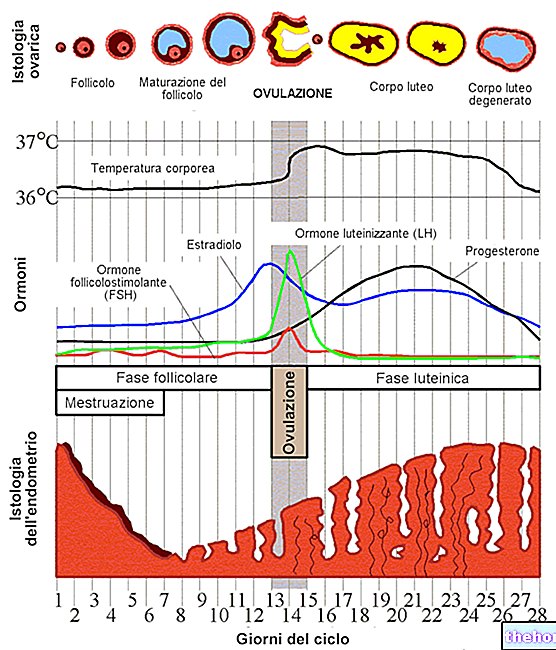
Substancja czynna leku Xgeva, denosumab, jest przeciwciałem monoklonalnym. Przeciwciało monoklonalne to przeciwciało (rodzaj białka) opracowane w celu rozpoznawania i przyłączania się do określonej struktury (antygenu) w organizmie. Denosumab został zaprojektowany tak, aby łączyć się z antygenem zwanym RANKL, który bierze udział w aktywacji osteoklastów, komórek organizmu odpowiedzialnych za rozkład tkanki kostnej. Wiążąc się z antygenem i hamując jego działanie, denosumab zmniejsza tworzenie i aktywność osteoklastów, co z kolei ogranicza utratę masy kostnej, zmniejszając prawdopodobieństwo złamań i innych poważnych powikłań kostnych.
Jak badano Xgeva - denosumab?
Efekty Xgeva zostały najpierw przetestowane na modelach eksperymentalnych, zanim zostały przebadane na ludziach.
Produkt Xgeva porównywano z kwasem zoledronowym (innym lekiem stosowanym w celu zapobiegania powikłaniom układu kostnego) w trzech dużych badaniach z udziałem pacjentów z przerzutami do kości z różnych rodzajów raka.W pierwszym badaniu wzięło udział 2046 pacjentów z rakiem piersi.W drugim badaniu wzięło udział 1901 mężczyzn z rak gruczołu krokowego, u których nie udało się zareagować na terapię hormonalną.W trzecim badaniu wzięło udział 1776 pacjentów z zaawansowanymi guzami litymi w różnych częściach ciała, z wyjątkiem piersi i prostaty, lub ze szpiczakiem mnogim (nowotwór szpiku kostnego).
We wszystkich badaniach oceniano ryzyko wystąpienia pierwszego „zdarzenia szkieletowego” (takiego jak złamanie, ucisk rdzenia kręgowego lub epizod wymagający radioterapii lub operacji) w okresie badania, mierząc odstęp czasu, jaki upłynął do wystąpienia tego zdarzenia.
Jaką korzyść wykazuje Xgeva – denosumab podczas badań?
Wykazano, że lek Xgeva skutecznie opóźnia pierwsze zdarzenie kostne u osób biorących udział w badaniach.W pierwszym i drugim badaniu lek Xgeva zmniejszał ryzyko wystąpienia pierwszego zdarzenia tego rodzaju o 18% w porównaniu z kwasem zoledronowym. W trzecim badaniu zmniejszenie tego ryzyka wyniosło 16% w porównaniu z kwasem zoledronowym.
Jakie jest ryzyko związane z lekiem Xgeva - denosumabem?
Najczęstsze działania niepożądane związane ze stosowaniem leku Xgeva (obserwowane u więcej niż 1 na 10 pacjentów) to duszność (trudności w oddychaniu) i biegunka. Pełny wykaz działań niepożądanych zgłaszanych podczas stosowania leku Xgeva znajduje się w ulotce dla pacjenta.
Leku Xgeva nie wolno stosować u osób, u których może występować nadwrażliwość (alergia) na denosumab lub którąkolwiek z pozostałych substancji.Nie należy go również stosować u osób z ciężką, nieleczoną hipokalcemią (poziom wapnia we krwi poniżej normy).
Dlaczego zatwierdzono Xgeva - denosumab?
CHMP zauważył, że istnieje potrzeba skutecznego nowego leczenia chorób układu kostnego związanych z zaawansowanymi nowotworami, zwłaszcza u pacjentów z chorobami nerek, ponieważ obecnie dostępne terapie mogą być toksyczne dla nerek. w przypadku szpiczaka mnogiego i progresji choroby (czas do pogorszenia się choroby) u pacjentów leczonych produktem Xgeva w porównaniu z pacjentami leczonymi kwasem zoledronowym; dlatego Komitet uznał, że ryzyko stosowania leku przewyższa korzyści w tej grupie pacjentów CHMP uznał, że korzyści ze stosowania leku Xgeva przewyższają ryzyko u pacjentów podmiotom z guzami litymi i zalecił przyznanie pozwolenia na dopuszczenie do obrotu tego produktu leczniczego.
Inne informacje dotyczące leku Xgeva - denosumab
W dniu 13 lipca 2011 r. Komisja Europejska wydała „Zezwolenie na dopuszczenie do obrotu” produktu Xgeva, ważne na terenie całej Unii Europejskiej.
W celu uzyskania dodatkowych informacji na temat leczenia produktem Xgeva należy zapoznać się z ulotką dla pacjenta (dołączoną do EPAR) bądź skontaktować się z lekarzem lub farmaceutą.
Ostatnia aktualizacja niniejszego podsumowania: 06-2011.
Informacje dotyczące leku Xgeva - denosumab opublikowane na tej stronie mogą być nieaktualne lub niekompletne. Aby prawidłowo wykorzystać te informacje, zobacz stronę Wyłączenie odpowiedzialności i przydatne informacje.














.jpg)