Co to jest Evista?
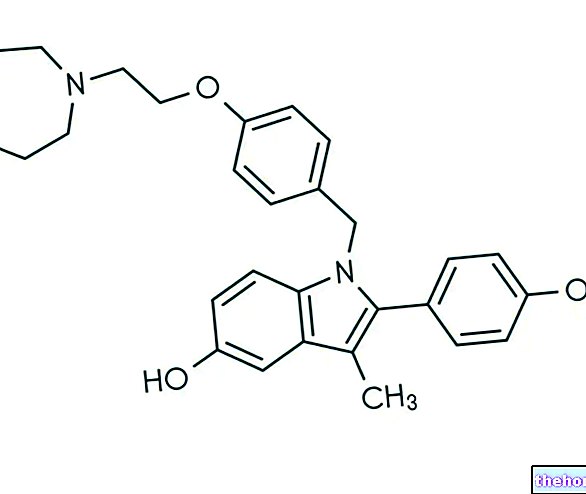
Evista to lek zawierający substancję czynną chlorowodorek raloksyfenu. Jest dostępny w postaci białych owalnych tabletek (60 mg).
Do czego służy Evista?
Evista jest stosowana w leczeniu i profilaktyce osteoporozy (choroby powodującej łamliwość kości) u kobiet po menopauzie.Wykazano, że Evista znacząco zmniejsza złamania kręgów (kręgosłupa), ale nie złamań biodra (biodra).
Lek jest dostępny wyłącznie na receptę.
Jak jest używany Evista?
Zalecana dawka dla dorosłych kobiet i kobiet w podeszłym wieku to jedna tabletka dziennie z posiłkami lub bez posiłków. Suplementy wapnia i witaminy D są ogólnie zalecane kobietom ze zmniejszonym spożyciem wapnia w diecie. Evista jest przeznaczona do długotrwałego użytkowania.
Jak działa Evista?
Osteoporoza występuje, gdy nie jest wytwarzana wystarczająca ilość nowej kości, aby zastąpić to, co jest naturalnie spożywane.Kości stają się coraz cieńsze i kruche i bardziej podatne na złamania.Osteoporoza występuje częściej u kobiet po menopauzie.Kiedy poziom żeńskiego hormonu estrogenu spada: estrogen spowalnia zmniejsza rozpad kości i czyni je mniej podatnymi na złamania.
Substancja czynna leku Evista, raloksyfen, jest selektywnym modulatorem receptora estrogenowego (SERM) i działa jako agonista receptora estrogenowego (substancja stymulująca receptor estrogenowy) w niektórych tkankach organizmu. Raloksyfen ma taki sam wpływ na kości jak estrogen, ale nie ma wpływu na pierś ani macicę.
Jak badano Evistę?
Preparat Evista badano w czterech badaniach głównych dotyczących leczenia i zapobiegania osteoporozie.
Trzy badania dotyczące zapobiegania osteoporozie obejmowały 1764 kobiety, które przyjmowały Evista lub placebo (leczenie pozorowane) przez dwa lata. W tych badaniach mierzono gęstość kości. W czwartym badaniu działanie preparatu Evista porównywano z działaniem preparatu Evista po placebo. w leczeniu osteoporozy u 7705 kobiet przez cztery lata. Główną miarą skuteczności była liczba kobiet, u których w trakcie badania wystąpiły złamania kręgów (kręgosłupa).
Jakie korzyści wykazał Evista podczas studiów?
Evista była skuteczniejsza niż placebo w zapobieganiu i leczeniu osteoporozy.
W zapobieganiu osteoporozie kobiety, które otrzymywały preparat Evista, odnotowały wzrost gęstości kości biodrowej i kręgosłupa o 1,6% w ciągu dwóch lat, podczas gdy te, które otrzymywały placebo, odnotowały spadek o 0,8%.
W leczeniu osteoporozy Evista był skuteczniejszy niż placebo w zmniejszaniu liczby złamań kręgów.W ciągu czterech lat, w porównaniu do placebo, Evista zmniejszył liczbę złamań kręgów o 46% u kobiet z osteoporozą i o 32% u kobiet z osteoporozą związaną z osteoporozą. z obecnością złamania. Evista nie wykazał wpływu na złamania biodra.
Jakie jest ryzyko związane z Evistą?
Najczęstsze działania niepożądane związane ze stosowaniem leku Evista (obserwowane u więcej niż 1 na 10 pacjentów) to rozszerzenie naczyń krwionośnych (uderzenia gorąca) i objawy grypopodobne. Pełna lista działań niepożądanych zgłoszonych podczas stosowania produktu Evista znajduje się w ulotce dla pacjenta.
Leku Evista nie wolno stosować u kobiet, które:
- mogę mieć dzieci;
- masz lub miałeś problemy z zakrzepami krwi, w tym zakrzepicą żył głębokich i zatorowością płucną (zakrzepy krwi w płucach);
- jeśli u pacjenta występuje choroba wątroby, ciężkie zaburzenia czynności nerek, niewyjaśnione krwawienie z macicy lub rak endometrium (rak wyściółki macicy).
Leku Evista nie wolno podawać osobom, u których występuje nadwrażliwość (alergia) na raloksyfen lub którykolwiek składnik preparatu.
Dlaczego Evista została zatwierdzona?
Komitet ds. Produktów Leczniczych Stosowanych u Ludzi (CHMP) uznał, że wykazano skuteczność preparatu Evista w zapobieganiu i leczeniu osteoporozy, bez wpływu na piersi i macicę. Komitet uznał, że korzyści płynące ze stosowania preparatu Evista przewyższają ryzyko w leczeniu i zapobieganiu osteoporozie u kobiet po menopauzie.Komitet zalecił przyznanie pozwolenia na dopuszczenie preparatu Evista do obrotu.
Inne informacje o Eviscie:
W dniu 5 sierpnia 1998 r. Komisja Europejska wydała „Pozwolenie na dopuszczenie do obrotu" dla preparatu Evista, ważne w całej Unii Europejskiej. „Pozwolenie na dopuszczenie do obrotu" zostało przedłużone w dniach 5 sierpnia 2003 r. i 5 sierpnia 2008 r. Posiadaczem pozwolenia na dopuszczenie do obrotu jest Daiichi Sankyo Europe GmbH .
Aby uzyskać pełną wersję EPAR Evista, kliknij tutaj.
Ostatnia aktualizacja niniejszego podsumowania: 01-2009.
Informacje dotyczące produktu Evista – chlorowodorku raloksyfenu opublikowane na tej stronie mogą być nieaktualne lub niekompletne. Aby prawidłowo wykorzystać te informacje, zobacz stronę Wyłączenie odpowiedzialności i przydatne informacje.