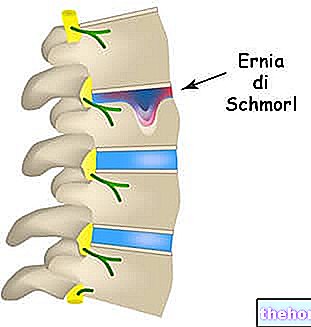
Składniki aktywne: Izotretynoina
ISOTRETINOIN STIEFEL Izotretinoina 0,05% krem
Dlaczego stosuje się krem izotretynoinowy - lek generyczny? Po co to jest?
Nazwa jego leku to krem Isotretinoin Stiefel 0,05%. Isotretinoin Stiefel zawiera substancję czynną zwaną izotretynoiną.
Izotretynoina Stiefel jest stosowana w leczeniu trądziku (czyraków) u młodych osób, które są w okresie dojrzewania lub weszły w okres dojrzewania oraz u dorosłych.Nie jest przeznaczony do stosowania u dzieci, które nie weszły w okres dojrzewania. Izotretynoina Stiefel pomaga:
- zmiękczają zaskórniki i zaskórniki, aby łatwiej wychodziły
- zapobiegają powstawaniu nowych zaskórników, zaskórników i czyraków
- zmniejszyć liczbę czerwonych i zapalnych czyraków trądzikowych.
Jest szczególnie odpowiedni, jeśli masz suchą skórę.
Przeciwwskazania, kiedy nie należy stosować kremu izotretynoinowego – leku generycznego
Nie stosować izotretynoiny Stiefel:
- jeśli pacjent ma uczulenie (nadwrażliwość) na izotretynoinę lub którykolwiek z pozostałych składników leku Isotretinoin Stiefel (wymienionych w punkcie 6).
- jeśli jesteś w ciąży, myślisz, że jesteś w ciąży lub planujesz zajść w ciążę
- jeśli karmisz piersią.
→ należy poinformować lekarza, jeśli którekolwiek z powyższych dotyczy Ciebie. Nie stosować izotretynoiny Stiefel.
Środki ostrożności dotyczące stosowania Informacje ważne przed zastosowaniem kremu izotretynoinowego – lek generyczny
Przed zastosowaniem leku Isotretinoin Stiefel lekarz powinien wiedzieć:
- jeśli Ty lub ktoś z Twoich bliskich miał raka skóry
- jeśli u pacjenta występowały problemy z tolerowaniem tego lub podobnych leków w przeszłości (uznano je za zbyt drażniące dla skóry)
- jeśli masz: o wyprysk o zaczerwienienie skóry, popękane naczynia włosowate i małe pryszcze, które zwykle znajdują się w środkowej części twarzy (trądzik różowaty) o zaczerwienienie i suchość wokół ust (okołowargowe zapalenie skóry
Izotretynoina Stiefel może dodatkowo zaakcentować te schorzenia.
- jeśli masz reakcje skórne na światło słoneczne
→ Skontaktuj się z lekarzem, jeśli uważasz, że którekolwiek z powyższych dotyczy Ciebie.
Uważaj, aby nie używać zbyt dużej ilości kremu, zwłaszcza tam, gdzie może spływać do oczu lub gromadzić się w kącikach nosa, fałdach skóry lub innych obszarach skóry, które nie wymagają leczenia.
Stosuj Isotretinoin Stiefel tylko na skórę.
Trzymaj go z dala od obszarów takich jak usta, usta i oczy.
Nie należy stosować Isotretinoin Stiefel na podrażnioną powierzchnię skóry. Na przykład, jeśli masz skaleczenia, otarcia lub oparzenia słoneczne.
Nie używaj zbyt dużej ilości Isotretinoin Stiefel na wrażliwych obszarach skóry, takich jak szyja.
Światło słoneczne
Stosowanie Izotretynoiny Stiefel może sprawić, że Twoja skóra stanie się bardziej wrażliwa na światło słoneczne.
Stosując Isotretinoin Stiefel należy:
- chronić skórę przed słońcem. Możesz to zrobić, używając kremu z filtrem i nosząc odzież, która chroni przed poparzeniem słonecznym.
- unikaj korzystania z leżaków (lamp słonecznych) lub spędzania długiego czasu na słońcu.
→ Jeśli doznasz oparzeń słonecznych, przestań stosować Isotretinoin Stiefel, aż stan skóry się poprawi.
Interakcje Jakie leki lub pokarmy mogą modyfikować działanie kremu izotretynoinowego – lek generyczny
Należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent przyjmuje, ostatnio przyjmował lub może przyjmować jakiekolwiek inne leki. Dotyczy to również leków zakupionych bez recepty.
W szczególności należy powiedzieć lekarzowi lub farmaceucie:
- jeśli pacjent stosuje nadtlenek benzoilu (inne leczenie trądziku) stosowany w tym samym czasie może zmniejszyć skuteczność leku Isotretinoin Stiefel. inne rano).
- jeśli stosujesz jakiekolwiek inne leczenie trądziku.Jeśli jest stosowany w tym samym czasie, może pogorszyć podrażnienie skóry. Jeśli Twoja skóra staje się bardzo podrażniona, może być konieczne rzadsze stosowanie Isotretinoin Stiefel lub zaprzestanie jej stosowania na krótki czas, aby skóra mogła się zregenerować, a następnie wznowić leczenie. Przerwij leczenie i skonsultuj się z lekarzem, jeśli podrażnienie skóry nie ulegnie poprawie.
→ Skontaktuj się z lekarzem, jeśli uważasz, że którekolwiek z powyższych dotyczy Ciebie.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
Ciąża i karmienie piersią
Nie należy stosować leku Isotretinoin Stiefel, jeśli jesteś w ciąży.
- Należy poinformować lekarza, jeśli jesteś w ciąży lub planujesz zajść w ciążę.
- Stosuj niezawodną metodę antykoncepcji, aby zapobiec ciąży podczas stosowania leku Isotretinoin Stiefel.
- Jeśli pacjentka zajdzie w ciążę podczas przyjmowania leku Isotretinoin Stiefel, powinna poinformować o tym lekarza.
Nie karmić piersią w przypadku stosowania leku Isotretinoin Stiefel. Należy zapytać lekarza, czy karmić piersią, czy stosować Isotretinoin Stiefel.
Przed zażyciem jakiegokolwiek leku należy poradzić się lekarza lub farmaceuty, jeśli pacjentka jest w ciąży lub karmi piersią.
Ważne informacje o niektórych składnikach Izotretynoiny Stiefel
- Izotretynoina Stiefel zawiera butylohydroksytoluen (BHT). Może powodować miejscowe reakcje skórne. Ponadto może powodować podrażnienia oczu i błon śluzowych, takich jak wnętrze nosa.
- Isotretinoin Stiefel zawiera alkohol cetostearylowy. Może powodować miejscowe reakcje skórne (np. kontaktowe zapalenie skóry).
- Izotretynoina Stiefel zawiera krezol chlorowy. Może powodować reakcje alergiczne.
- Izotretynoina Stiefel zawiera glikol propylenowy. Może powodować podrażnienie skóry.
Dawka, sposób i czas podawania Jak stosować krem izotretynoinowy – lek generyczny: dawkowanie
Izotretynoinę Stiefel należy zawsze stosować zgodnie z zaleceniami lekarza. W razie wątpliwości skonsultuj się z lekarzem lub farmaceutą.
- Stosuj Isotretinoin Stiefel raz lub dwa razy dziennie. Lekarz poinformuje Cię, jak stosować lek.
- Może upłynąć 6-8 tygodni, zanim pojawią się zauważalne efekty stosowania leku Isotretinoin Stiefel.
- Należy kontynuować stosowanie leku, dopóki lekarz nie zaleci inaczej.
Jak stosować Izotretynoinę Stiefel
- Myć dłonie.
- Całkowicie usuń makijaż
- Umyj obszar łagodnym mydłem i ciepłą wodą i delikatnie osusz.
- Cienką warstwę kremu Isotretinoin Stiefel nanieść na dotkniętą skórę opuszkami palców i masować.
- Nakładaj na cały obszar skóry skłonnej do trądziku, a nie tylko na pojedyncze pryszcze.
- Po użyciu kremu umyj ręce.
Przedawkowanie Co zrobić, jeśli pacjent przyjął zbyt dużą ilość kremu izotretynoinowego – lek generyczny
Zastosowanie większej niż zalecana dawki izotretynoiny Stiefel
Jeśli zastosujesz zbyt dużo Isotretinoin Stiefel lub częściej niż powinieneś, może to spowodować zaczerwienienie, łuszczenie lub podrażnienie skóry. Jeśli tak się stanie, używaj kremu rzadziej lub przestań go używać na kilka dni, a następnie zacznij od nowa. Stosowanie większej ilości Isotretinoin Stiefel niż powinna nie pomoże szybciej goić się wrzodów.
Jeśli przypadkowo połkniesz izotretynoinę Stiefel
Nie przewiduje się, aby składniki preparatu Isotretinoin Stiefel były szkodliwe w przypadku spożycia w niewielkich ilościach.
- Jeśli przypadkowo dostaniesz się do ust Isotretinoin Stiefel, natychmiast przemyj je dużą ilością wody.
- Skonsultuj się z lekarzem, jeśli spożyjesz dużą ilość izotretynoiny Stiefel.
Pominięcie zastosowania Isotretinoin Stiefel
Nie należy stosować podwójnej dawki kremu w celu uzupełnienia pominiętej dawki. Następną dawkę należy zastosować o zwykłej porze.
Skutki uboczne Jakie są skutki uboczne kremu izotretynoinowego - lek generyczny
Jak każdy lek, Isotretinoin Stiefel może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Ciężkie reakcje alergiczne:
- silne pieczenie, łuszczenie lub swędzenie skóry
→ Należy zaprzestać stosowania leku Isotretinoin Stiefel i natychmiast skontaktować się z lekarzem, jeśli zauważy się którekolwiek z powyższych działań niepożądanych – może być konieczna pilna pomoc medyczna.
Bardzo częste działania niepożądane (mogą wystąpić u co najmniej 1 na 10 osób):
Efekty te mogą wystąpić w obszarze skóry, na którym zastosowano krem. Jeśli sprawiają Ci problemy, spróbuj rzadziej stosować krem Isotretinoin Stiefel lub przestań go używać na kilka dni, aż podrażnienie ustąpi, a następnie zacznij go używać ponownie.
Przestań używać kremu Isotretinoin Stiefel, jeśli podrażnienie nie ustąpi:
- zaczerwienienie lub łuszczenie się skóry, szczególnie w pierwszych tygodniach stosowania
- łagodny świąd lub ból skóry
- podrażnienie lub bolesność skóry
- pieczenie skóry
- sucha skóra
- swędzenie
Inne skutki uboczne
Te działania niepożądane wystąpiły u niewielkiej liczby osób, ale ich dokładna częstość nie jest znana:
- skóra, która staje się ciemniejsza lub jaśniejsza
- zwiększona wrażliwość na światło słoneczne.
Zgłaszanie skutków ubocznych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe działania niepożądane niewymienione w tej ulotce, należy porozmawiać z lekarzem lub farmaceutą. Działania niepożądane można również zgłaszać bezpośrednio za pośrednictwem krajowego systemu zgłaszania pod adresem https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse
Zgłaszając działania niepożądane, możesz dostarczyć więcej informacji na temat bezpieczeństwa tego leku.
Wygaśnięcie i przechowywanie
Trzymaj Isotretinoin Stiefel w miejscu niewidocznym i niedostępnym dla dzieci
- Nie przechowywać izotretynoiny Stiefel w temperaturze powyżej 25°C.
- Nie stosować leku Isotretinoin Stiefel po upływie terminu ważności zamieszczonego na tubie i kartoniku
- Nie należy wyrzucać żadnych leków do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa.Pomoże to chronić środowisko.
Co zawiera lek Izotretynoina Stiefel
- Substancja czynna to 0,05% wag./wag. izotretynoiny
- Pozostałe składniki to: parafina ciekła lekka, adypinian di-n-butylu, eter stearylowy makrogolu, glikol propylenowy, alkohol cetostearylowy, alkohol benzylowy, PEG-5 stearynian gliceryny, karbomer, chlorokrezol, sodu wodorotlenek, butylohydroksytoluen (BHT), woda oczyszczona.
Jak wygląda lek Isotretinoin Stiefel i co zawiera opakowanie
- Izotretynoina Stiefel to jasnożółty krem
- Izotretynoina Stiefel jest sprzedawana w tubach po 15 gramów, 25 gramów, 30 gramów, 40 gramów lub 50 gramów śmietany.
- Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO
IZOTRETINOINA DIFA COOPER MIĘKKIE KAPSUŁKI
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY
Izotretynoina Difa Cooper 10 mg kapsułka miękka
Każda kapsułka miękka zawiera 10 mg izotretynoiny
Izotretynoina Difa Cooper 20 mg kapsułka miękka
Każda kapsułka miękka zawiera 20 mg izotretynoiny
Substancje pomocnicze:
Olej sojowy, Ponceau 4R (E 124), sorbitol
Pełny wykaz substancji pomocniczych, patrz punkt 6.1
03.0 POSTAĆ FARMACEUTYCZNA
Kapsułki miękkie
Isotretinoin Difa Cooper 10 mg kapsułki miękkie: jasnofioletowe podłużne kapsułki miękkie zawierające nieprzezroczysty żółty/pomarańczowy lepki płyn.
Isotretinoin Difa Cooper 20 mg kapsułki miękkie: Podłużne, miękkie, czerwonawo-brązowe kapsułki zawierające nieprzezroczysty żółty/pomarańczowy lepki płyn.
04.0 INFORMACJE KLINICZNE
04.1 Wskazania terapeutyczne
Ciężkie postacie trądziku (takie jak trądzik guzkowy lub trądzik skupiony lub trądzik z ryzykiem trwałego bliznowacenia) oporne na odpowiednie cykle standardowej terapii z ogólnoustrojowymi lekami przeciwbakteryjnymi i terapię miejscową.
04.2 Dawkowanie i sposób podawania
Izotretynoina powinna być przepisywana wyłącznie przez lub pod nadzorem lekarzy, którzy mają doświadczenie w stosowaniu ogólnoustrojowych retinoidów w leczeniu ciężkiego trądziku i którzy w pełni rozumieją ryzyko związane z leczeniem izotretynoiną oraz potrzebę monitorowania.
Kapsułki należy przyjmować z jedzeniem raz lub dwa razy dziennie.
Dorośli, w tym młodzież i osoby starsze
Leczenie izotretynoiną należy rozpocząć od dawki 0,5 mg/kg na dobę. Odpowiedź terapeutyczna na izotretynoinę i niektóre działania niepożądane izotretynoiny są zależne od dawki i różnią się w zależności od pacjenta.Dlatego podczas terapii konieczne jest indywidualne dostosowanie dawki.U większości pacjentów dawka wynosi od 0,5 do 1,0 mg/kg na dobę.
Długotrwała remisja i częstość nawrotów są ściślej związane z całkowitą podaną dawką niż z czasem trwania leczenia lub dawką dobową. Wykazano, że nie należy oczekiwać znaczących dodatkowych korzyści poza skumulowaną dawką leczniczą 120-150 mg/kg.Czas trwania leczenia będzie zależał od indywidualnej dawki dobowej.Czas leczenia trwający 16-24 tygodnie jest zwykle wystarczający do osiągnąć remisję.
U większości pacjentów całkowite ustąpienie trądziku uzyskuje się po jednym cyklu leczenia. W przypadku pewnego nawrotu można rozważyć kolejny cykl leczenia izotretynoiną w tej samej dawce dobowej i w tej samej skumulowanej dawce leczniczej. poprawę trądziku można zaobserwować do 8 tygodni po zakończeniu leczenia, nie należy rozważać dalszego leczenia przed upływem tego okresu.
Pacjenci z ciężką niewydolnością nerek
U pacjentów z ciężką niewydolnością nerek leczenie należy rozpocząć od mniejszej dawki (np. 10 mg/dobę). Następnie dawkę należy zwiększyć do 1 mg/kg/dobę lub do maksymalnej dawki tolerowanej przez pacjenta (patrz punkt 4.4 „Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania”).
Dzieci
Izotretynoina nie jest wskazana w leczeniu trądziku przedpokwitaniowego i nie jest zalecana u pacjentów w wieku poniżej 12 lat.
Pacjenci z nietolerancją
U pacjentów z ciężką nietolerancją zalecanej dawki leczenie można kontynuować w mniejszej dawce, czego konsekwencją jest dłuższy czas leczenia i większe ryzyko nawrotu. Aby osiągnąć maksymalną możliwą skuteczność u tych pacjentów, dawkę należy normalnie kontynuować przy maksymalnej tolerowanej dawce.
04.3 Przeciwwskazania
Izotretynoina jest przeciwwskazana u kobiet w ciąży lub karmiących piersią (patrz punkt 4.6 „Ciąża i laktacja”)
Izotretynoina jest przeciwwskazana u kobiet w wieku rozrodczym, chyba że spełnione są wszystkie warunki Programu Zapobiegania Ciąży (patrz punkt 4.4 „Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania”).
Ponadto izotretynoina jest przeciwwskazana u pacjentów
• Z niewydolnością wątroby
• Z nadmiernie wysokimi wartościami lipidów w osoczu
• Z hiperwitaminozą A
• Z nadwrażliwością na izotretynoinę, soję, orzeszki ziemne, Ponceau 4R (E 124) lub na którąkolwiek substancję pomocniczą
• Jednoczesne leczenie tetracyklinami (patrz punkt 4.5 „Interakcje z innymi produktami leczniczymi i inne rodzaje„ interakcji ”)
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania
Program Zapobiegania Ciąży
Ten lek jest TERATOGENNY
Izotretynoina jest przeciwwskazana u kobiet w wieku rozrodczym, chyba że pacjentka spełnia wszystkie poniższe warunki Programu Zapobiegania Ciąży:
- Pacjent musi mieć ciężki trądzik (trądzik guzkowy lub skupiony lub trądzik z ryzykiem trwałego bliznowacenia) oporny na odpowiednie cykle standardowego leczenia ogólnoustrojowymi lekami przeciwbakteryjnymi i leczenie miejscowe (patrz punkt 4.1 „Wskazania do stosowania”).
- Rozumie ryzyko teratogenne.
- Rozumie potrzebę rygorystycznych comiesięcznych obserwacji.
- Rozumie i akceptuje potrzebę skutecznej antykoncepcji, bez przerwy, od 1 miesiąca przed rozpoczęciem leczenia, przez cały czas trwania leczenia do 1 miesiąca po zakończeniu leczenia.Należy stosować co najmniej jedną, a najlepiej dwie uzupełniające się formy antykoncepcji, w tym metodę barierową.
- Nawet w przypadku braku miesiączki pacjentka musi przestrzegać wszystkich instrukcji dotyczących „skutecznej antykoncepcji”.
- Musi być w stanie przestrzegać skutecznych środków antykoncepcyjnych.
- Jest poinformowana i rozumie potencjalne konsekwencje ciąży oraz potrzebę szybkiej konsultacji z lekarzem w przypadku ryzyka ciąży.
- Rozumie potrzebę i wyraża zgodę na wykonanie testu ciążowego bezpośrednio przed rozpoczęciem leczenia, w trakcie leczenia oraz 5 tygodni po zakończeniu leczenia.
- Przyznał, że rozumie zagrożenia i niezbędne środki ostrożności związane ze stosowaniem izotretynoiny.
Te stany dotykają również kobiety, które nie są obecnie aktywne seksualnie, chyba że lekarz prowadzący uzna, że istnieją przekonujące powody, które wskazują, że nie ma ryzyka zajścia w ciążę.
Lekarz przepisujący lek musi zapewnić, że:
- Pacjentka przestrzega wcześniej zgłoszonych warunków zapobiegania ciąży, w tym potwierdzenie odpowiedniego poziomu zrozumienia.
- Pacjent rozpoznał wyżej wymienione wymagania.
- Pacjentka stosowała co najmniej jedną, a najlepiej dwie metody skutecznej antykoncepcji, w tym metodę mechaniczną przez co najmniej 1 miesiąc przed rozpoczęciem leczenia i kontynuuje stosowanie skutecznej antykoncepcji przez cały okres leczenia i przez co najmniej 1 miesiąc. miesiąc po zakończeniu kuracji.
- Ujemne wyniki testu ciążowego uzyskano przed, w trakcie i 5 tygodni po zakończeniu leczenia. Daty i wyniki badań muszą być udokumentowane.
Zapobieganie ciąży
Pacjentki powinny otrzymać wyczerpujące informacje na temat zapobiegania ciąży oraz porady dotyczące antykoncepcji, jeśli nie stosują skutecznej antykoncepcji.
Jako wymóg minimalny, pacjentki z potencjalnym ryzykiem zajścia w ciążę muszą stosować co najmniej jedną skuteczną metodę antykoncepcji. Pacjentki powinny najlepiej stosować dwie uzupełniające się formy antykoncepcji, w tym metodę barierową. Antykoncepcję należy kontynuować przez co najmniej 1 miesiąc po zakończeniu leczenia izotretynoiną, nawet u pacjentek z brakiem miesiączki.
Test ciążowy
Zgodnie z praktyką medyczną zaleca się wykonanie testu ciążowego z minimalną czułością 25 mIU/ml w pierwszych trzech dniach cyklu miesiączkowego pod nadzorem lekarza w następujący sposób.
Przed rozpoczęciem terapii
Przed rozpoczęciem antykoncepcji, w celu wykluczenia możliwości zajścia w ciążę, zaleca się wykonanie pod nadzorem lekarza wstępnego testu ciążowego, którego data wykonania i wynik są odnotowywane. czas wykonania Test ciążowy powinien odzwierciedlać aktywność seksualną pacjentki i powinien być wykonany około 3 tygodnie po ostatnim stosunku płciowym bez zabezpieczenia Lekarz przepisujący powinien poinformować pacjentkę o antykoncepcji.
Test ciążowy nadzorowany przez lekarza powinien być również wykonany w ciągu 3 dni od pierwszej recepty i powinien być wykonany po tym, jak pacjentka stosowała skuteczną antykoncepcję przez co najmniej 1 miesiąc. Ten test ciążowy powinien zapewnić, że pacjentka nie jest w ciąży w momencie rozpoczynania leczenia izotretynoiną.
Wizyty kontrolne
Wizyty kontrolne powinny być zaplanowane w odstępach 28-dniowych. Konieczność powtarzania comiesięcznych testów ciążowych pod nadzorem lekarza należy określić na podstawie lokalnej praktyki, biorąc pod uwagę aktywność seksualną pacjentki i niedawny wywiad menstruacyjny (nieregularne miesiączki, brak miesiączki lub brak miesiączki). Jeśli jest to wskazane, kontrolne testy ciążowe należy wykonać w ciągu 3 dni od przepisania recepty.
Koniec leczenia
Pięć tygodni po zakończeniu leczenia pacjentki muszą przejść końcowy test ciążowy, aby wykluczyć ciążę.
Ograniczenia dotyczące przepisywania i wydawania
Przepisywanie izotretynoiny kobietom w wieku rozrodczym należy ograniczyć do 30 dni leczenia, a dalsze leczenie wymaga wystawienia nowej recepty. Najlepiej byłoby, gdyby test ciążowy, wystawienie recepty i wydanie izotretynoiny nastąpiło tego samego dnia. Wydanie izotretynoiny musi nastąpić w ciągu maksymalnie 7 dni od wypisania recepty.
Pacjenci płci męskiej
Dostępne dane sugerują, że poziom narażenia matki na nasienie pacjentek otrzymujących izotretynoinę nie jest wystarczająco duży, aby można było wiązać teratogenne działanie izotretynoiny.Mężczyźni powinni pamiętać, aby nigdy nie udostępniać tego leku innym osobom, zwłaszcza kobietom.
Dodatkowe środki ostrożności
Pacjentów należy pouczyć, aby nigdy nie podawali tego leku innym osobom i zwracali niewykorzystane kapsułki do apteki po zakończeniu leczenia.
Pacjenci nie powinni być dawcami krwi w trakcie leczenia i przez miesiąc po odstawieniu leku ze względu na potencjalne ryzyko dla płodu kobiety w ciąży otrzymującej taką krew.
Materiał edukacyjny
Aby pomóc lekarzom przepisującym lek, farmaceutom i pacjentom uniknąć narażenia płodu na izotretynoinę, podmiot odpowiedzialny dostarczy materiały edukacyjne mające na celu wzmocnienie ostrzeżeń dotyczących teratogenności izotretynoiny, doradzając w zakresie antykoncepcji przed rozpoczęciem leczenia oraz informując o konieczności wykonania testu ciążowego.
Wszystkim pacjentkom płci męskiej i żeńskiej lekarz powinien udzielić pełnej informacji o ryzyku działania teratogennego i ścisłych środkach zapobiegania ciąży, określonych w Programie Zapobiegania Ciąży.
Zaburzenia psychiczne
U pacjentów leczonych izotretynoiną zgłaszano depresję, nasilenie depresji, lęk, agresję, zmiany nastroju, objawy psychotyczne i bardzo rzadko myśli samobójcze, próby samobójcze i samobójstwa (patrz punkt 4.8 „Działania niepożądane”).
Szczególną uwagę należy zwrócić na pacjentów z depresją w wywiadzie. Wszystkich pacjentów należy monitorować pod kątem objawów depresji i w razie potrzeby skierować na odpowiednie leczenie. Przerwanie leczenia może jednak nie wystarczyć. może być wymagana ocena psychologiczna."
Zaburzenia skóry i tkanki podskórnej
W początkowym okresie leczenia czasami obserwuje się pogorszenie trądziku, które ustępuje wraz z kontynuacją leczenia, zwykle w ciągu 7-10 dni i zwykle nie wymaga dostosowania dawki.
W okresie po wprowadzeniu do obrotu zgłaszano przypadki ciężkich reakcji skórnych (np. rumień wielopostaciowy (EM), zespół Stevena Johnsona (SJS) i toksyczne martwicze oddzielanie się naskórka (TEN) związane ze stosowaniem izotretynoiny. Ponieważ zdarzenia te mogą być trudne do rozróżnienia W przypadku podejrzenia ciężkiej reakcji skórnej należy przerwać leczenie izotretynoiną.
Unikaj intensywnej ekspozycji na światło słoneczne lub promieniowanie UV.W razie potrzeby należy stosować produkt przeciwsłoneczny o wysokim współczynniku ochrony (co najmniej 15).
Należy unikać agresywnej dermabrazji chemicznej i laseroterapii skóry u pacjentów leczonych izotretynoiną przez okres 5-6 miesięcy po zakończeniu leczenia ze względu na ryzyko powstania blizn przerostowych w obszarach atypowych oraz, rzadziej, pozapalnych hipo lub hiperpigmentacji w leczone obszary. Unikaj stosowania wosku do depilacji u pacjentów leczonych izotretynoiną przez okres co najmniej 6 miesięcy po zabiegu ze względu na ryzyko skaleczenia skóry.
Należy unikać jednoczesnego podawania izotretynoiny i miejscowych produktów przeciwtrądzikowych o działaniu keratolitycznym lub złuszczającym, ponieważ może wystąpić nasilenie miejscowego podrażnienia (patrz punkt 4.5 „Interakcje z innymi produktami leczniczymi i inne rodzaje„ interakcji ”).
Od początku leczenia zaleca się pacjentom stosowanie kremu nawilżającego lub kremu i balsamu do ust, ponieważ izotretynoina może powodować suchość skóry i ust.
Zaburzenia oka
Suchość oczu, zmętnienie rogówki, pogorszenie widzenia nocnego i zapalenie rogówki zwykle ustępują po przerwaniu leczenia. Suche oczy można złagodzić, stosując nawilżającą maść do oczu lub sztuczne łzy. Może wystąpić nietolerancja soczewek kontaktowych i pacjent może być zmuszony do noszenia okularów podczas leczenia.
Zgłaszano również pogorszenie widzenia w nocy, które u niektórych pacjentów było nagłe (patrz punkt 4.7 „Wpływ na zdolność prowadzenia pojazdów i „obsługiwania maszyn”). Pacjentów, u których występują problemy ze wzrokiem, należy skierować na badanie oczu. leczenie izotretynoiną.
Zaburzenia mięśniowo-szkieletowe i tkanki łącznej
U pacjentów otrzymujących izotretynoinę, szczególnie wśród tych, którzy podejmują wzmożoną aktywność fizyczną, zgłaszano bóle mięśni, bóle stawów i zwiększoną aktywność fosfokinazy kreatyninowej w surowicy (patrz punkt 4.8 „Działania niepożądane”).
Po kilku latach podawania bardzo wysokich dawek w leczeniu zaburzeń keratynizacji wystąpiły zmiany kostne, w tym przedwczesne zrosty nasad, hiperostoza i zwapnienie ścięgien i więzadeł. Dawki, czas trwania leczenia i całkowita dawka skumulowana u tych pacjentów na ogół znacznie przekraczały dawki zalecane w leczeniu trądziku.
Łagodne nadciśnienie śródczaszkowe
Zgłaszano przypadki łagodnego nadciśnienia śródczaszkowego, z których niektóre dotyczyły jednoczesnego stosowania tetracyklin (patrz punkty 4.3 „Przeciwwskazania” i 4.5 „Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji”). ból głowy, nudności i wymioty, zaburzenia widzenia i obrzęk tarczy nerwu wzrokowego.
Pacjenci, u których rozwinie się łagodne nadciśnienie śródczaszkowe, powinni natychmiast przerwać leczenie izotretynoiną.
Zaburzenia wątroby i dróg żółciowych
Enzymy wątrobowe należy sprawdzać przed leczeniem, 1 miesiąc po rozpoczęciu leczenia, a następnie co 3 miesiące, chyba że klinicznie jest wskazana częstsza kontrola.Zgłaszano przemijające i odwracalne zwiększenie aktywności aminotransferaz wątrobowych. normalny zakres i wartości powróciły do poziomu wyjściowego w trakcie leczenia. Jednak w przypadku utrzymującego się, klinicznie istotnego wzrostu aktywności aminotransferaz, należy rozważyć zmniejszenie dawki lub przerwanie leczenia.
Niewydolność nerek
Niewydolność nerek i niewydolność nerek nie wpływają na farmakokinetykę izotretynoiny. Dlatego izotretynoina może być podawana pacjentom z niewydolnością nerek. Zaleca się jednak, aby leczenie pacjentów rozpoczynać od zmniejszonej dawki, a następnie zwiększać do maksymalnej tolerowanej dawki (patrz punkt 4.2 „Dawkowanie i sposób podawania”).
Metabolizm lipidów
Stężenie lipidów w surowicy (wartości na czczo) należy sprawdzać przed leczeniem, 1 miesiąc po rozpoczęciu leczenia, a następnie co 3 miesiące, chyba że częstsze monitorowanie nie jest wskazane klinicznie. może również reagować na środki dietetyczne.
Izotretynoina jest związana ze zwiększonymi poziomami triglicerydów w osoczu.
Izotretynoinę należy przerwać, jeśli nie można kontrolować triglicerydemii do akceptowalnego poziomu lub jeśli wystąpią objawy zapalenia trzustki (patrz punkt 4.8 „Działania niepożądane”). Stężenia powyżej 800 mg/dl lub 9 mmol/l są czasami związane z ostrym zapaleniem trzustki, które może być śmiertelnym.
Zaburzenia żołądkowo-jelitowe
Izotretynoina jest związana z zapaleniem jelit (w tym miejscowym zapaleniem jelita krętego) u pacjentów bez wcześniejszej choroby jelit.Pacjenci, u których wystąpi ciężka (krwotoczna) biegunka, powinni natychmiast przerwać leczenie izotretynoiną.
Reakcje alergiczne
Rzadko zgłaszano reakcje anafilaktyczne, w niektórych przypadkach po wcześniejszej miejscowej ekspozycji na retinoidy. Rzadko zgłaszane są reakcje alergiczne skóry. Zgłaszano ciężkie przypadki alergicznego zapalenia naczyń, często z plamicą (wybroczyny i czerwone plamy) na kończynach i zajęciem pozaskórnym. Ciężkie reakcje alergiczne wymagają przerwania leczenia i uważnego monitorowania pacjenta.
Pacjenci wysokiego ryzyka
U pacjentów z cukrzycą, otyłością, alkoholizmem lub zaburzeniami metabolizmu lipidów leczonych izotretynoiną może być konieczne częstsze sprawdzanie stężenia lipidów i/lub glukozy we krwi. Zgłaszano podwyższony poziom glukozy we krwi na czczo i zdiagnozowano nowe przypadki cukrzycy podczas leczenia izotretynoiną.
Zaburzenia metabolizmu i odżywiania
Kapsułka miękka izotretynoiny Difa Cooper 10 mg / 20 mg zawiera sorbitol. Pacjenci z rzadką dziedziczną nietolerancją fruktozy nie powinni przyjmować tego leku.
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji
Pacjenci nie powinni przyjmować witaminy A jako leku towarzyszącego ze względu na ryzyko wystąpienia hiperwitaminozy A.
Zgłaszano przypadki łagodnego nadciśnienia śródczaszkowego (guz rzekomy mózgu) podczas jednoczesnego stosowania izotretynoiny i tetracyklin, dlatego należy unikać jednoczesnego leczenia tetracyklinami (patrz punkt 4.3 „Przeciwwskazania” i 4.4 „Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania”).
Należy unikać jednoczesnego podawania izotretynoiny i miejscowych produktów przeciwtrądzikowych o działaniu keratolitycznym lub złuszczającym, ponieważ może wystąpić nasilenie miejscowego podrażnienia (patrz punkt 4.4 „Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania”).
04.6 Ciąża i laktacja
Ciąża
Ciąża jest bezwzględnym przeciwwskazaniem do leczenia izotretynoiną (patrz punkt 4.3 „Przeciwwskazania”). Jeśli mimo tych środków ostrożności wystąpi ciąża podczas leczenia izotretynoiną lub w następnym miesiącu, istnieje wysokie ryzyko bardzo poważnych i poważnych wad rozwojowych płodu.
Wady rozwojowe płodu związane z ekspozycją na izotretynoinę obejmują wady ośrodkowego układu nerwowego (wodogłowie, wady/nieprawidłowości móżdżku, małogłowie), dymorfizm twarzy, rozszczep podniebienia, wady ucha zewnętrznego (brak ucha zewnętrznego, małe lub nieobecne), wady gałki ocznej (mikroftalmia), układu sercowo-naczyniowego anomalie (malformacje pnia stożka, takie jak tetralogia Fallota, transpozycja wielkich naczyń, ubytki przegrody), anomalie grasicy i przytarczyc. Istnieje również zwiększona częstość występowania poronień samoistnych.
W przypadku zajścia w ciążę u kobiety przyjmującej izotretynoinę, leczenie należy przerwać, a pacjentkę skierować do specjalisty lub mającego doświadczenie w teratologii w celu oceny i konsultacji.
Czas karmienia
Ponieważ izotretynoina jest wysoce lipofilna, bardzo prawdopodobne jest przenikanie leku do mleka matki.Ze względu na możliwość wystąpienia działań niepożądanych u narażonego niemowlęcia poprzez mleko matki, stosowanie izotretynoiny u matek karmiących jest przeciwwskazane.
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
W trakcie leczenia izotretynoiną wystąpiło wiele przypadków pogorszenia widzenia w nocy, w rzadkich przypadkach po zakończeniu leczenia (patrz punkty 4.4 „Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania” i 4.8 „Działania niepożądane”). ostrzec pacjentów o tym możliwym problemie i poinstruować ich, aby zachowali ostrożność podczas prowadzenia pojazdów i obsługiwania maszyn.
Bardzo rzadko zgłaszano senność, zawroty głowy i zaburzenia widzenia.
Pacjentów należy pouczyć, że jeśli doświadczyli tych zaburzeń, nie powinni prowadzić pojazdów, obsługiwać maszyn ani brać udziału w innych czynnościach, w przypadku których te objawy mogą narazić ich lub innych na ryzyko.
04.8 Działania niepożądane
Niektóre z działań niepożądanych związanych ze stosowaniem izotretynoiny są zależne od dawki.Działania niepożądane zwykle ustępują po modyfikacji dawki lub przerwaniu leczenia, jednak niektóre mogą utrzymywać się po przerwaniu leczenia. Najczęściej zgłaszanymi działaniami niepożądanymi izotretynoiny są następujące objawy: suchość skóry, suchość błon śluzowych np. warg (zapalenie warg), błony śluzowej nosa (krwawienie z nosa) i oczu (zapalenie spojówek).
Infekcje
Bardzo rzadkie (≤ 1/10.000)
Zakażenia bakteryjne Gram-dodatnie (śluzówkowo-skórne)
Zaburzenia układu krwionośnego i limfatycznego
Bardzo częste (≥ 1/10)
Niedokrwistość, zwiększona szybkość sedymentacji erytrocytów, małopłytkowość, trombocytoza
Pospolity (≥ 1/100,
Neutropenia
Bardzo rzadkie (≤ 1/10.000)
Limfadenopatia
Zaburzenia układu odpornościowego
Rzadki (≥ 1/10.000,
Skórna reakcja alergiczna, reakcje anafilaktyczne, nadwrażliwość
Zaburzenia metabolizmu i odżywiania
Bardzo rzadkie (≤ 1/10.000)
Cukrzyca, hiperurykemia
Zaburzenia psychiczne
Rzadki (≥ 1/10.000,
Depresja, nasilenie depresji, lęk, agresja, zmiany nastroju.
Bardzo rzadkie (≤ 1/10.000)
Zaburzenia behawioralne, zaburzenia psychotyczne, myśli samobójcze, samobójstwo
Zaburzenia układu nerwowego
Pospolity (≥ 1/100,
Bół głowy
Bardzo rzadkie (≤ 1/10.000)
Łagodne nadciśnienie śródczaszkowe, drgawki, senność, zawroty głowy
Zaburzenia oka
Bardzo częste (≥ 1/10)
Zapalenie powiek, zapalenie spojówek, suchość oczu, podrażnienie oka
Bardzo rzadkie (≤ 1/10.000)
Niewyraźne widzenie, zaćma, ślepota barw (niedobór widzenia kolorów), nietolerancja soczewek kontaktowych, zmętnienie rogówki, zmniejszone widzenie w nocy, zapalenie rogówki, obrzęk tarczy nerwu wzrokowego (jako objaw łagodnego nadciśnienia śródczaszkowego), światłowstręt, zaburzenia widzenia
Zaburzenia ucha i błędnika
Bardzo rzadkie (≤ 1/10.000)
Upośledzenie słuchu
Patologie naczyniowe
Bardzo rzadkie (≤ 1/10.000)
Zapalenie naczyń (np. ziarniniak Wegenera, alergiczne zapalenie naczyń)
Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia
Pospolity (≥ 1/100,
Krwawienie z nosa, suchość nosa, zapalenie nosogardzieli
Bardzo rzadkie (≤ 1/10.000)
Skurcz oskrzeli (szczególnie u chorych na astmę), chrypka
Zaburzenia żołądkowo-jelitowe
Bardzo rzadkie (≤ 1/10.000)
Zapalenie okrężnicy, zapalenie jelita krętego, suchość gardła, krwotok z przewodu pokarmowego, biegunka krwotoczna i choroba zapalna jelit, nudności, zapalenie trzustki (patrz punkt 4.4 „Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania”)
Zaburzenia wątroby i dróg żółciowych
Bardzo częste (≥ 1/10)
Zwiększenie aktywności aminotransferaz (patrz punkt 4.4 „Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania”)
Bardzo rzadkie (≤ 1/10.000)
Zapalenie wątroby
Zaburzenia skóry i tkanki podskórnej
Bardzo częste (≥ 1/10)
Zapalenie warg, zapalenie skóry, suchość skóry, miejscowe złuszczanie, świąd, wysypka rumieniowa, kruchość skóry (ryzyko urazu tarcia)
Rzadki (≥ 1/10.000,
Łysienie
Bardzo rzadkie (≤ 1/10.000)
Piorunujący trądzik, nasilenie trądziku (zaostrzenie trądziku), rumień (twarzy), wysypka, zaburzenia włosów, hirsutyzm, dystrofia paznokci, zanokcica, reakcje nadwrażliwości na światło, ziarniniak ropny, przebarwienia skóry, zwiększona potliwość
Częstość nieznana (brak możliwości oszacowania na podstawie dostępnych danych): rumień wielopostaciowy, zespół Stevena-Johnsona, martwica toksyczno-rozpływna naskórka
Zaburzenia mięśniowo-szkieletowe i tkanki łącznej
Bardzo częste (≥ 1/10)
Ból stawów, ból mięśni, ból pleców (szczególnie u dzieci i młodzieży)
Bardzo rzadkie (≤ 1/10.000)
Zapalenie stawów, zwapnienie (zwapnienie więzadeł i ścięgien), przedwczesne uszczelnianie nasad kości, egzostoza (hiperostoza), zmniejszenie gęstości kości, zapalenie ścięgien, rabdomioliza
Zaburzenia nerek i dróg moczowych
Bardzo rzadkie (≤ 1/10.000)
Kłębuszkowe zapalenie nerek
Zaburzenia ogólne i stany w miejscu podania
Bardzo rzadkie (≤ 1/10.000)
Tkanka ziarninowa (zwiększone tworzenie), złe samopoczucie
Testy diagnostyczne
Bardzo częste (≥ 1/10)
Wzrost trójglicerydemii, spadek lipoprotein o dużej gęstości
Pospolity (≥ 1/100,
podwyższony poziom cholesterolu, podwyższony poziom cukru we krwi, krwiomocz, białkomocz
Bardzo rzadkie (≤ 1/10.000)
Zwiększony poziom fosfokinazy kreatynowej we krwi.
Częstość występowania zdarzeń niepożądanych obliczono z puli danych z badań klinicznych z udziałem 824 pacjentów oraz z danych po wprowadzeniu do obrotu.
Zgłaszanie podejrzewanych działań niepożądanych
Zgłaszanie podejrzewanych działań niepożądanych występujących po dopuszczeniu produktu leczniczego do obrotu jest ważne, ponieważ umożliwia ciągłe monitorowanie stosunku korzyści do ryzyka produktu leczniczego. Osoby należące do fachowego personelu medycznego są proszone o zgłaszanie wszelkich podejrzewanych działań niepożądanych za pośrednictwem krajowego systemu zgłaszania. „adres https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Przedawkowanie
Izotretynoina jest pochodną witaminy A. Chociaż ostra toksyczność izotretynoiny jest niewielka, po przypadkowym przedawkowaniu mogą wystąpić objawy hiperwitaminozy A. Objawy ostrej toksyczności witaminy A obejmują silny ból głowy, nudności lub wymioty, senność, drażliwość i świąd . Oznaki i objawy przypadkowego lub celowego przedawkowania izotretynoiny są prawdopodobnie podobne. Oczekuje się, że objawy będą odwracalne i ustępują bez konieczności leczenia.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE
05.1 Właściwości farmakodynamiczne
Grupa farmakoterapeutyczna: preparat przeciwtrądzikowy do stosowania ogólnego
Kod ATC: D10BA01
Mechanizm akcji
Izotretynoina jest stereoizomerem wszystkichtrans retinowy (tretynoina). Dokładny mechanizm działania izotretynoiny nie został jeszcze szczegółowo wyjaśniony, ale ustalono, że poprawa obserwowana w obrazie klinicznym ciężkiego trądziku jest związana z zahamowaniem czynności gruczołów łojowych i histologicznie wykazanym zmniejszeniem wielkości gruczołów łojowych. żołądź. Ponadto wykazano przeciwzapalne działanie izotretynoiny na skórę.
Skuteczność
Nadmierne rogowacenie wyściółki nabłonka jednostki włosowo-łojowej prowadzi do odkładania się komórek zrogowaciałych wewnątrz przewodu i ich zablokowania przez keratynę i nadmiar sebum, co prowadzi do powstania zaskórnika i ewentualnie zmian zapalnych.
Izotretynoina hamuje proliferację komórek wytwarzających łój i wydaje się działać przeciw trądzikowi poprzez przywrócenie prawidłowego procesu różnicowania.Sebum jest ważnym substratem dla wzrostu Propionibacterium acnes więc zmniejszenie produkcji sebum hamuje kolonizację bakteryjną przewodu.
05.2 „Właściwości farmakokinetyczne
Wchłanianie
Wchłanianie izotretynoiny przez przewód pokarmowy jest zmienne i zależne od dawki w zakresie terapeutycznym.Całkowitej biodostępności izotretynoiny nie określono, ponieważ związek ten nie jest dostępny jako preparat dożylny do stosowania u ludzi, ale ekstrapolacja z badań na psach sugeruje dość niska i zmienna biodostępność ogólnoustrojowa.Jeśli izotretynoina jest przyjmowana z jedzeniem, biodostępność podwaja się w porównaniu z warunkami na czczo.
Dystrybucja
Izotretynoina silnie wiąże się z białkami osocza, głównie albuminami (99,9%). Objętość dystrybucji izotretynoiny u ludzi nie została określona, ponieważ izotretynoina nie jest dostępna w postaci preparatu dożylnego do stosowania u ludzi.Niewiele jest danych dotyczących dystrybucji izotretynoiny w tkankach u ludzi.Izotretynoina w naskórku jest tylko o połowę mniejsza niż w surowicy . Stężenia izotretynoiny w osoczu są około 1,7 razy większe niż w pełnej krwi z powodu słabej penetracji izotretynoiny do czerwonych krwinek.
Metabolizm
Po podaniu doustnym izotretynoiny w osoczu zidentyfikowano trzy główne metabolity: 4-oksoizotretynoina, tretinoina (wszystkietrans retinowy) i 4-oksy-tretynoina. W kilku badaniach wykazano, że te metabolity są biologicznie aktywne in vitro. Badanie kliniczne wykazało, że 4-oksy-tretynoina znacząco przyczynia się do aktywności izotretynoiny (zmniejszenie szybkości wydzielania łojowego, pomimo braku wpływu na stężenie izotretynoiny i tretinoiny w osoczu). Inne metabolity o mniejszym znaczeniu obejmują pochodne glukuronianowe. Głównym metabolitem jest 4-oksoizotretynoina, której stężenie w osoczu w stanie stacjonarnym jest 2,5 razy wyższe niż stężenie związku macierzystego.
Izotretynoina i tretinoina (wszystkietrans retinowe) wykazują odwracalny metabolizm (interkonwersję), a zatem metabolizm tretinoiny jest podobny do izotretynoiny.Oszacowano, że 20-30% dawki izotretynoiny jest metabolizowane przez izomeryzację.
Krążenie jelitowo-wątrobowe może odgrywać znaczącą rolę w farmakokinetyce izotretynoiny u ludzi. in vitro wykazały, że kilka enzymów CYP bierze udział w metabolizmie izotretynoiny do 4-okso-izotretynoiny i tretinoiny.Wydaje się, że nie ma jednej dominującej formy izomerycznej nad pozostałymi.Izotretynoina i jej metabolity nie wpływają znacząco na aktywność CYP.
Eliminacja
Po doustnym podaniu izotretynoiny znakowanej radioizotopem, w moczu i kale stwierdzono w przybliżeniu równe frakcje dawki.Po podaniu doustnym izotretynoiny, okres półtrwania w końcowej fazie eliminacji niezmienionego leku u pacjentów z trądzikiem wynosi średnio 19 godzin. Okres półtrwania 4-oksoizotretynoiny w końcowej fazie eliminacji jest dłuższy i wynosi średnio 29 godzin.
Izotretynoina jest fizjologicznym retinoidem, a stężenie endogennego retinoidu jest osiągane po około dwóch tygodniach od zakończenia leczenia izotretynoiną.
Farmakokinetyka w populacjach specjalnych
Ponieważ izotretynoina jest przeciwwskazana u pacjentów z niewydolnością wątroby, informacje na temat jej kinetyki w tej populacji pacjentów są ograniczone.Niewydolność nerek nie zmniejsza znacząco klirensu osoczowego izotretynoiny i 4-oksoizotretynoiny.
05.3 Przedkliniczne dane o bezpieczeństwie
Toksyczność ostra
Ostra toksyczność doustna izotretynoiny została określona u różnych gatunków zwierząt.LD50 wynosi około 2000 mg/kg u królików, około 3000 mg/kg u myszy i ponad 4000 mg/kg u szczurów.
Toksyczność przewlekła
Długotrwałe badanie na szczurach przez 2 lata (z dawkami izotretynoiny 2, 8 i 32 mg/kg/dobę) dostarczyło dowodów na częściową utratę włosów i podwyższony poziom triglicerydów w osoczu w grupie otrzymującej wyższe dawki. Spektrum działań niepożądanych izotretynoiny u gryzoni jest zatem bardzo podobne do działania witaminy A, ale nie obejmuje masywnych zwapnień tkanek i narządów obserwowanych po podaniu witaminy A szczurom. Zmiany obserwowane w hepatocytach z witaminą A nie wystąpiły w przypadku izotretynoiny.
Wszystkie obserwowane działania niepożądane zespołu hiperwitaminozy A ustępowały samoistnie po odstawieniu izotretynoiny. Nawet zwierzęta doświadczalne w ogólnie złym stanie zdrowia w większości wyzdrowiały w ciągu 1-2 tygodni.
Teratogenność
Podobnie jak w przypadku innych pochodnych witaminy A, wykazano, że izotretynoina ma działanie teratogenne i embriotoksyczne u zwierząt doświadczalnych.
Biorąc pod uwagę potencjał teratogenny izotretynoiny, istnieją terapeutyczne konsekwencje jej stosowania u pacjentek w wieku rozrodczym (patrz punkty 4.3 „Przeciwwskazania”, 4.4 „Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania” oraz 4.6 „Ciąża i laktacja”).
Płodność
Izotretynoina w dawkach terapeutycznych nie wpływa na liczbę, ruchliwość i morfologię plemników oraz nie zagraża powstawaniu i rozwojowi zarodka przez samców przyjmujących izotretynoinę.
Mutagenność
W testach nie wykazano mutagenności ani rakotwórczości izotretynoiny in vitro lub w testach in vivo na zwierzętach.
06.0 INFORMACJE FARMACEUTYCZNE
06.1 Zaróbki
Zawartość kapsułki:
Rafinowany olej sojowy, DL-alfa-tokoferol, wersenian disodowy, butylohydroksynizol, uwodorniony olej roślinny, częściowo uwodorniony olej sojowy, żółty wosk.
Powłoka kapsułki:
Kapsułki 10 mg: żelatyna, 98-101% glicerol, 70% sorbitol, woda oczyszczona, Ponceau 4R (E 124), czarny tlenek żelaza (E 172) i dwutlenek tytanu (E 171).
Kapsułki 20 mg: żelatyna, 98-101% glicerol, 70% sorbitol, woda oczyszczona, Ponceau 4R (E 124), indygotyna (E 132) i dwutlenek tytanu (E 171).
06.2 Niezgodność
Nieistotne.
06.3 Okres ważności
3 lata.
06.4 Specjalne środki ostrożności przy przechowywaniu
Nie przechowywać w temperaturze powyżej 30°C.
Przechowywać w oryginalnym opakowaniu w celu ochrony przed wilgocią i światłem.
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania
Blistry PVC / PVCD / folia aluminiowa.
Opakowania po 20, 30, 50, 60 lub 100 kapsułek miękkich.
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
06.6 Instrukcje użytkowania i obsługi
Pacjentów należy pouczyć, aby nigdy nie podawali tego leku innym osobom i zwracali niewykorzystane kapsułki do apteki po zakończeniu leczenia.
07.0 PODMIOT POZWOLENIA NA DOPUSZCZENIE DO OBROTU
Difa Cooper S.p.A., Via Milano 160, 21042 Caronno Pertusella (Varese)
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
20 miękkich kapsułek 10 mg AIC nr 036083018
30 miękkich kapsułek 10 mg AIC nr 036083020
50 miękkich kapsułek 10 mg AIC nr 036083032
60 kapsułek miękkich po 10 mg AIC nr 036083044
100 miękkich kapsułek 10 mg AIC nr 036083057 / M
20 miękkich kapsułek 20 mg AIC nr 036083069/M
30 miękkich kapsułek 20 mg AIC nr 036083071/M
50 miękkich kapsułek 20 mg AIC nr 036083083 / M
60 kapsułek miękkich 20 mg AIC nr 036083095/M
100 miękkich kapsułek 20 mg AIC nr 036083107/M
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA
Dekret AIC / ZAK nr. 978 z 13.05.2004 r. - GU n. 168 z 20.07.2004 r
10.0 DATA ZMIAN TEKSTU
listopad 2014



















-di-cottura.jpg)