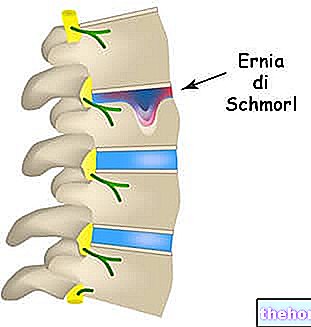
Choroba dziedziczna SMA jest spowodowana mutacjami w genie SMN1 lub SMN2, których celem jest wytworzenie białka zapewniającego przeżycie neuronów ruchowych.
Istnieje pięć różnych form rdzeniowego zaniku mięśni: typ 0, typ 1, typ 2, typ 3 i typ 4. Pierwsze trzy typy są bardzo poważne i powodują przedwczesną śmierć pacjenta; typ 3 i typ 4 to łagodniejsze warianty, które wpływają na standard życia chorego, ale nie powodują przedwczesnej śmierci.
Do zdiagnozowania SMA potrzebny jest test genetyczny na próbce krwi.
Obecnie terapia SMA opiera się głównie na leczeniu objawowym, mającym na celu łagodzenie zaburzeń i kontrolowanie powikłań. Lekarstwo jest dostępne, oparte na zasadach terapii genowej, ale jest to rozwiązanie bardzo drogie i możliwe do zastosowania tylko u niektórych pacjentów.
, co objawia się zanikiem i wynikającym z tego osłabieniem mięśni szkieletowych i trudnościami ruchowymi.
SMA to stan, który może spowodować śmierć pacjenta w młodym lub bardzo młodym wieku: najpoważniejsze postaci choroby w rzeczywistości wpływają na sprawność mięśni oddechowych i są odpowiedzialne za epizody niewydolności oddechowej lub zapalenia płuc z śmiertelny wynik.
Neurony ruchowe i SMA

Neurony ruchowe lub neurony ruchowe to komórki nerwowe, które powstają w ośrodkowym układzie nerwowym (mózgu i rdzeniu kręgowym) i które za pomocą swoich wydłużeń (aksonów) kontrolują pracę mięśni i gruczołów.
Istnieją dwa typy neuronów ruchowych: górne neurony ruchowe (lub pierwsze neurony ruchowe) i dolne neurony ruchowe (lub drugie neurony ruchowe).
Górne neurony ruchowe powstają w mózgu i kierują aktywnością dolnych neuronów ruchowych, które powstają głównie w rdzeniu kręgowym i są odpowiedzialne za kierowanie aktywnością mięśni szkieletowych (lub somatycznych), mięśni gładkich (lub trzewnych), mięśnia sercowego i serca.
Neurony ruchowe osób z SMA ulegają stopniowej degeneracji, powodując „zanik mięśni z powodu braku aktywności, który w najcięższych przypadkach prowadzi do paraliżu, niewydolności oddechowej i śmierci.
Epidemiologia: jak często występuje rdzeniowy zanik mięśni?
SMA ma „roczną częstość występowania 1 przypadku na 10 000 nowych urodzeń.
5 i od którego zależy produkcja tzw. białka przeżycia neuronów ruchowych (SMN).Jak sugeruje nazwa białka wytwarzanego przez SMN1 i SMN2, mutacja tych genów pozbawia neurony ruchowe substancji biologicznej niezbędnej do ich przetrwania; dokładniej obniża poziom białka: na przykład w obecności mutacji w SMN1 poziom białka SMN spada do 10-20% normy.
Oczywiście brak odpowiedniej ilości białka SMN warunkuje postępującą degenerację neuronów ruchowych.
Utrata neuronów ruchowych powoduje przerwanie sygnalizacji nerwowej, która pozwala kontrolować aktywność mięśni ludzkiego ciała, te ostatnie w wyniku ich nieprzydatności ulegają stopniowemu procesowi zaniku i osłabienia.
Czy wiedziałeś, że ...
Gen SMN2 jest, dla SMA, genem modyfikującym chorobę; w rzeczywistości u pacjentów z mutacją w SMN1 i posiadających z jakiegoś powodu trzy lub cztery kopie genu SMN2, SMA występuje w łagodniejszej postaci.
Rdzeniowy zanik mięśni: rodzaje mutacji
Gdy SMA jest spowodowane „zmianą SMN1, w 95-98% przypadków odpowiedzialna mutacja polega na delecji całego genu, a tylko w 2-5% na anomalii prawidłowej sekwencji genu.
Rdzeniowy zanik mięśni: choroba dziedziczna
Prawie we wszystkich przypadkach (98%) anomalia genetyczna odpowiedzialna za SMA jest dziedziczna, tzn. przekazują ją rodzice chorego osobnika.
2% niedziedzicznych przypadków SMA jest spowodowanych mutacją de novo wystąpił na bardzo wczesnym etapie rozwoju embrionalnego.
Model SMA i dziedziczenia
Model dziedziczenia rdzeniowego zaniku mięśni jest autosomalny recesywny, co oznacza, że aby odziedziczyć SMA, konieczne jest, aby oboje rodzice byli zdrowymi nosicielami defektu genetycznego w SMN1 lub SMN2 i aby oboje rodzice go przekazali.
W przypadku chorób dziedziczonych autosomalnie recesywnie, takich jak SMA, prawdopodobieństwo, że obaj zdrowi nosiciele przeniosą wadę genetyczną na dziecko, powodując jego zachorowanie, wynosi 25%, czyli co czwarty przypadek.
Rodzaje SMA
Na podstawie wieku zachorowania i ciężkości stanu eksperci rozpoznają pięć różnych postaci rdzeniowego zaniku mięśni:
- SMA typu 0: jest to najcięższa forma ze wszystkich. Objawia się jeszcze przed urodzeniem zmniejszoną ruchliwością płodu.
Niemowlęta zwykle przeżywają kilka tygodni po urodzeniu, nawet jeśli otrzymują wspomaganie oddechowe. - SMA typu 1: spośród form występujących w życiu jest najcięższa i najczęstsza (około 50% przypadków); pojawia się w młodym wieku, zwykle w szóstym miesiącu życia.
Z reguły jest przyczyną śmierci już w pierwszych latach życia; rzadko w okresie dojrzewania.
Śmierć zwykle następuje z powodu „niewydolności oddechowej lub” infekcji płuc. - SMA typ 2: jest to forma, która grawitacyjnie zajmuje drugie miejsce; na ogół zaczyna się między 7 a 18 miesiącem życia.
Średnia długość życia osób dotkniętych chorobą jest dłuższa niż w poprzednim przypadku: pacjentom w rzeczywistości udaje się osiągnąć dorosłość. - SMA typu 3: mniej dotkliwe niż dwa poprzednie, ta forma SMA zwykle pojawia się po 18 miesiącach życia (w niektórych przypadkach może również pojawić się w dzieciństwie lub okresie dojrzewania).
Wiąże się z poważnymi niepełnosprawnościami, ale nie wpływa na długość życia. - SMA typu 4: jest to postać choroby w wieku dorosłym, a także najmniej ciężka; zwykle zaczyna się około trzeciej dekady życia i ma bardzo powolny przebieg.
Na ogół nie odpowiada za problemy z oddychaniem i wiąże się z „normalną długością życia”.
Poziomy białka SMN wpływają na ciężkość SMA: im mniejsza ilość SMN, tym większe nasilenie choroby pokrewnej.
Zmniejszenie poziomów SMN jest ściśle związane z rozmiarem defektu genetycznego, który dotknął geny SMN1 lub SMN2: im bardziej rozległy jest ten defekt, tym bardziej znaczące jest zmniejszenie ilości białka SMN (tak jest w przypadku przykład delecji genu).
Ponadto SMA nie zaburza funkcji intelektualnych (iloraz inteligencji pacjentów jest w normie) i oszczędza narząd wzroku.
Więcej informacji: SMA: wszystkie objawyObjawy SMA typu 0
Jak już wspomniano, SMA typu 0 występuje już w wieku prenatalnym z obniżoną ruchomością płodu; po urodzeniu chore dziecko ma więc wyraźne trudności w połykaniu i oddychaniu.
Choroba kończy się śmiercią w ciągu kilku tygodni od urodzenia, nawet gdy pacjent otrzymuje wspomaganie oddechowe.
Objawy SMA typu 1
Dzieci z SMA typu 1 mają bardzo słabe mięśnie, które nie rozwijają się tak, jak powinny (zanik mięśni). Uniemożliwia im to wykonywanie czynności, takich jak podnoszenie głowy, poruszanie kończynami i przyjmowanie pozycji siedzącej; ponadto stopniowo komplikuje funkcje życiowe, takie jak ssanie mleka, połykanie, żucie i oddychanie.
Zazwyczaj SMA typu 1 kończy się śmiercią w ciągu pierwszych kilku lat życia; niektórym pacjentom udaje się jednak osiągnąć wiek dojrzewania.
Śmierć zwykle następuje z powodu niewydolności oddechowej lub „infekcji płuc z powodu trudności w połykaniu (zapalenie płuc po spożyciu lub odbyt pokarmowy).
Objawy SMA typu 2
SMA typu 2 klasycznie objawia się:
- Miękkość mięśni rąk i nóg;
- Drżenie palców i dłoni;
- Trudność w samodzielnym przyjmowaniu pozycji siedzącej (pacjentowi jednak udaje się ją utrzymać);
- Trudności ze staniem i chodzeniem
- Deformacje i problemy ze stawami;
- Trudności w oddychaniu i połykaniu pokarmu;
- Skolioza (zwykle pojawia się później).
Nawet w tej sytuacji trudności z oddychaniem i połykaniem pokarmu są przyczyną przedwczesnej śmierci, która zwykle pojawia się na początku dorosłości.
Objawy SMA typu 3
Typ 3 SMA powoduje problemy z postawą i równowagą, drżenie rąk oraz trudności w wstawaniu z pozycji siedzącej, chodzeniu, wchodzeniu po schodach i bieganiu.
Na początku dolegliwości nie wymagają wspomagania lokomocji, później, wraz z degeneracją większej liczby neuronów ruchowych, podstawą stają się kule, chodziki i wózki inwalidzkie.
Chociaż może się to zdarzyć, bardzo rzadko pacjenci z SMA typu 3 cierpią na problemy z oddychaniem i połykaniem jedzenia.
W obecności tej formy SMA oczekiwana długość życia jest normalna, ale występują wszystkie wyżej wymienione problemy.
Objawy SMA typu 4
Z początkiem choroby w wieku dorosłym, SMA typu 4 zazwyczaj wiąże się z:
- Osłabienie napięcia mięśniowego ramion i nóg;
- Trudności z chodzeniem
- Drżenie i nagłe drganie mięśni.
Początkowo powyższe skargi są umiarkowane; na starość stają się bardziej spójne.
Podobnie jak SMA typu 3, SMA typu 4 nie jest chorobą, która wpływałaby na długość życia pacjenta.
SMA: kiedy iść do lekarza?
Wszystkim rodzicom, którzy wiedzą, że są zdrowymi nosicielami SMA, zdecydowanie zaleca się skonsultowanie się z pediatrą z doświadczeniem w chorobach genetycznych i genetykiem.
Jeśli nie posiadasz tego typu informacji, dobrze jest oceniać z miesiąca na miesiąc rozwój motoryczny Twojego dziecka oraz funkcje, od których zależy życie (np. oddychanie).
Z pewnością niemożność siedzenia lub przyjęcia pozycji siedzącej, trudności w karmieniu, występowanie deficytów oddechowych oraz szczupła i mniej umięśniona niż u rówieśników mięśnie stanowią dzwonki alarmowe.
W przypadku postaci SMA u dorosłych podejrzewa się i należy monitorować mniej lub bardziej nagły początek osłabienia mięśni i trudności w chodzeniu.
Rdzeniowy zanik mięśni: powikłania
Najcięższe formy SMA mogą prowadzić do powikłań, takich jak:
- Uduszenie z jedzenia. Wynika to ze zmniejszonej zdolności do żucia i przyjmowania pokarmu.
- Niewydolność oddechowa. Jest to konsekwencja niemożności kontrolowania aktywności mięśni oddechowych.
- Zapalenie płuc odbyt pokarmowy (lub wziewne zapalenie płuc). Występuje, gdy obcy materiał przenoszący patogeny, taki jak pokarm, ślina lub wydzieliny z nosa, dostanie się lub nagromadzi w płucach.
Zapalenie płuc odbyt pokarmowy jest wynikiem trudności w połykaniu. - Paraliż w wyniku korzystania z wózków inwalidzkich. Dzieje się tak, gdy choroba nieodwracalnie upośledza zdolności ruchowe pacjenta.
- Niedożywienie. Jest to kolejna konsekwencja trudności w połykaniu: pacjent w rzeczywistości ma trudności z prawidłowym odżywianiem.
Należy zauważyć, że czasami podczas diagnozowania SMA można wykorzystać takie badania, jak elektromiografia lub biopsja mięśnia.
SMA: badanie fizykalne i wywiad
Badanie fizykalne pacjenta, który może cierpieć na SMA, obejmuje dokładną analizę objawów i poszukiwanie typowych objawów choroby, takich jak:
- osłabienie i tkliwość mięśni;
- Nagłe skurcze mięśni
- Zmniejszone lub brak odruchów ścięgnistych.
Jeśli chodzi o wywiad medyczny, skupia się on głównie na wywiadzie rodzinnym pacjenta, aby ustalić, czy jakikolwiek inny członek rodziny (rodzice, rodzeństwo, dziadkowie) skarży się lub skarży się na podobną symptomatologię.Oczywiście fakt, że SMA jest dziedziczna choroba przekazywana od rodziców.
Chociaż nie pozwalają na postawienie ostatecznej diagnozy, badanie fizykalne i wywiad lekarski mogą dostarczyć bardzo przydatnych informacji, które ukierunkowują badania na przeprowadzenie testu genetycznego.
Oczywiście, jeśli pacjent jest małym dzieckiem, rodzice będą kontaktować się z lekarzem podczas historii choroby.
SMA i test genetyczny

Test genetyczny do wykrywania SMA obejmuje poszukiwanie i badanie mutacji w genach SMN1/SMN2 w próbce komórek krwi pacjenta.
Obecność zmian genetycznych oznacza oczywiście chorobę.
Analiza wykrytych mutacji jest niezbędna do ustalenia rodzaju występującego rdzeniowego zaniku mięśni i ciężkości stanu.
Aby poznać wyniki wyżej wymienionego testu genetycznego, zazwyczaj należy odczekać od 3 do 4 tygodni (dokładny czas oczekiwania różni się w zależności od ośrodka genetycznego, który przeprowadza test).
SMA: czy możliwa jest diagnostyka prenatalna?
Możliwe jest zdiagnozowanie SMA w wieku prenatalnym.
Aby to zrobić, potrzebujesz badania genetycznego na próbce komórek płodowych, uzyskanej delikatnymi metodami, takimi jak villocentesis lub amniopunkcja.
Biorąc pod uwagę ryzyko aborcji, które charakteryzuje CVS i amniopunkcję, lekarze prowadzą badania prenatalne pod kątem wszelkich mutacji, które można przypisać „rdzeniowemu zanikowi mięśni tylko wtedy, gdy kryje się za tym rodzinna historia SMA lub jeśli nienarodzone dziecko jest dzieckiem zdrowych nosicieli choroby.
Badania przesiewowe SMA i noworodków
Należy zauważyć, że w kilku włoskich regionach (Lazio i Toskania) usługa jest aktywna ekranizacja do wczesnej diagnozy SMA i innych poważnych chorób genetycznych.
Wczesna diagnoza tych chorób pozwala na zaplanowanie w odpowiednim czasie najwłaściwszej terapii objawowej w celu opanowania objawów i powikłań.
Rdzeniowy zanik mięśni i planowanie ciąży
Poradnictwo genetyczne polecane jest wszystkim kobietom planującym ciążę, które:
- Mieli dziecko z SMA w poprzedniej ciąży;
- Mają za sobą rodzinną historię SMA;
- Czy są zdrowymi nosicielami choroby, czy ich partner jest.
Poradnictwo genetyczne może pomóc kobietom z tymi schorzeniami zrozumieć, na jakie ryzyko jest narażone przyszłe dziecko.
SMA i diagnostyka różnicowa
Istnieją dwie patologie bardzo podobne do SMA, które tylko „dokładne badanie diagnostyczne rozpoznaje i zapobiega pomyleniu z „rdzeniowym zanikiem mięśni”: są to „rdzeniowy zanik mięśni z niewydolnością oddechową (SMARD) i” opuszkowo-rdzeniowy zanik mięśni (BSMA) lub choroba Kennedy'ego); pierwsza jest spowodowana mutacją genu IGHMBP2 zlokalizowanego na chromosomie 11, natomiast druga wynika z mutacji chromosomu płci X.
i farmaceutyki) zatwierdził Zolgensma, metodę terapii genowej do leczenia rdzeniowego zaniku mięśni.
Zolgensma obejmuje wysoce zaawansowaną technikę biologii molekularnej, która obejmuje użycie wektora wirusa zdolnego do wstawienia normalnej kopii genu SMN1 / SMN2 do DNA obecnego w neuronach ruchowych pacjenta.
Podawanie wyżej wymienionego wektora wirusowego odbywa się poprzez wstrzyknięcie dożylne.
Zolgensma okazała się skuteczna. Jednak zgodnie z przewidywaniami ma dwa główne ograniczenia, które uniemożliwiają jego powszechne stosowanie:
- To jest bardzo drogie. Mówi się o milionach euro;
- Dotyczy tylko pacjentów z SMA poniżej 2 roku życia.
Rdzeniowy zanik mięśni: leczenie objawowe
Terapie objawowe dla SMA gwarantują większe korzyści, jeśli zostaną szybko przyjęte; to sprawia, że wczesne rozpoznanie choroby jest bardzo ważne.
SMA i wsparcie oddechowe
Właściwe wspomaganie oddychania pomaga osobom cierpiącym na SMA nie tylko oddychać, ale także zmniejszać ryzyko infekcji płuc.
Wśród różnych opcji terapeutycznych znajdują się maski do nieinwazyjnej wentylacji oraz bardziej inwazyjne rozwiązania, takie jak intubacja jamy ustnej i tchawicy, przy czym te pierwsze są idealne w lżejszych przypadkach, podczas gdy bardziej inwazyjne rozwiązania są niezbędne dla pacjentów z poważnymi problemami oddechowymi.
SMA i wsparcie żywieniowe
Najcięższe formy rdzeniowego zaniku mięśni wpływają na zdolność połykania i żucia pokarmu, narażając pacjenta na ryzyko zadławienia, zapalenia płuc po spożyciu i niedożywienia.
Aby kontrolować te niebezpieczne konsekwencje, konieczne jest skorzystanie z pomocy w karmieniu, takich jak zgłębnik nosowo-żołądkowy lub operacja gastrostomijna, oraz zdanie się na dietetyka, który zaplanuje dietę dostosowaną do potrzeb pacjenta.
SMA i Fizjoterapia
Trudności ruchowe, które charakteryzują pacjenta z rdzeniowym zanikiem mięśni, prowadzą do sztywności stawów i mięśni w wyniku braku aktywności.
Odpowiedni program fizjoterapii pozwala w miarę możliwości poprawić elastyczność mięśni i zmniejszyć sztywność stawów.
Oczywiście program ten zawiera ćwiczenia, których wykonanie jest w zasięgu możliwości pacjenta.
SMA i ortopedia
W przypadku wystąpienia skoliozy, typowej dla ciężkich postaci SMA, konieczna jest konsultacja z ortopedą; to ostatnie może wskazywać na użycie gorsetu ortopedycznego, jeśli deformacja jest łagodna, lub optowanie za operacją fuzji kręgosłupa, jeśli deformacja kręgosłupa jest poważna.
Leki przeciwko SMA
Od kilku lat istnieją również specyficzne leki przeciwko SMA.
Leki te zasługują na osobne leczenie w porównaniu z terapiami objawowymi, choć nie pozwalają wyleczyć choroby, a jedynie ją powstrzymać.
Obecnie dostępne specyficzne leki przeciw SMA to Spinraza (nusinersen) i Evrysdi (risdiplam): pierwszy działa poprzez korygowanie nieprawidłowej produkcji białka SMN w tym procesie; drugi zwiększa poziom produkcji SMN, również starając się utrzymać go na poziomie kontyngent adekwatny do potrzeb organizmu człowieka.
Zatwierdzone przez FDA odpowiednio w 2017 i 2020 roku Spinraza i Evrysdi gwarantują wyniki, w niektórych przypadkach nawet bardziej niż zadowalające, mają jednak ważne ograniczenie: są bardzo drogie.
Więcej informacji: Spinraza: Jak to działa, ryzyko i korzyści















-di-cottura.jpg)