Składniki aktywne: Kwas rizedronowy (sodowy rizedronian)
Actonel 5 mg tabletki powlekane
Dlaczego stosuje się Actonel? Po co to jest?
Podobnie Actonel
Actonel należy do grupy leków niehormonalnych zwanych bisfosfonianami, które są stosowane w leczeniu chorób kości. Działa bezpośrednio na kości wzmacniając je, a tym samym zmniejszając ryzyko złamań.
Kość to żywa tkanka.Stara tkanka kostna jest stale usuwana i zastępowana nową kością.
Osteoporoza pomenopauzalna to choroba, która rozwija się u kobiet po menopauzie, w wyniku której kości kobiety stają się bardziej kruche i bardziej podatne na złamania spowodowane upadkami lub przeciążeniem.
Osteoporoza występuje łatwiej u kobiet, które osiągnęły wczesną menopauzę, a także u pacjentek leczonych przez dłuższy czas kortyzonem.
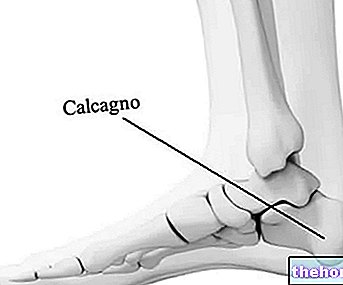
Kości najbardziej podatne na złamania to kręgosłup, biodro i nadgarstek, chociaż wszystkie kości w ciele mogą złamać.Złamania związane z osteoporozą mogą również powodować ból pleców, utratę wzrostu i skrzywienie pleców (garb). Wielu pacjentów z osteoporozą nie ma żadnych objawów i nawet nie wie, że je ma.
Do czego nadaje się Actonel
Do leczenia osteoporozy
- U kobiet po menopauzie
W profilaktyce osteoporozy
- U kobiet z wysokim ryzykiem osteoporozy (w tym niska gęstość kości, wczesna menopauza lub rodzinna historia osteoporozy)
- U kobiet po menopauzie poddawanych ogólnoustrojowej terapii kortyzonem przez dłuższy czas. Actonel utrzymuje lub zwiększa masę kostną.
Przeciwwskazania Kiedy nie należy stosować preparatu Actonel
Nie należy przyjmować leku Actonel:
- Jeśli pacjent ma uczulenie na sól sodową ryzedronianu lub którykolwiek z pozostałych składników tego leku
- Jeśli lekarz powiedział pacjentowi, że ma hipokalcemię (niski poziom wapnia we krwi);
- Jeśli jesteś w ciąży, jeśli możesz być w ciąży lub jeśli planujesz zajść w ciążę mimo wszystko;
- Jeśli karmisz piersią
- Jeśli masz poważne problemy z nerkami.
Środki ostrożności dotyczące stosowania Informacje ważne przed zastosowaniem leku Actonel
Przed rozpoczęciem stosowania leku Actonel należy omówić to z lekarzem lub farmaceutą:
- Jeśli nie jesteś w stanie utrzymać wyprostowanego tułowia (siedząc lub stojąc) przez co najmniej trzydzieści minut;
- jeśli u pacjenta występuje nieprawidłowy metabolizm kości i minerałów (taki jak niedobór witaminy D, zaburzenia parathormonu, które powodują niski poziom wapnia we krwi);
- Jeśli u pacjenta występują lub występowały w przeszłości problemy z przełykiem (przewodem łączącym jamę ustną z żołądkiem), na przykład pacjent mógł odczuwać ból lub trudności w połykaniu pokarmu lub pacjent został wcześniej poinformowany, że ma przełyk Barretta ( stan związany ze zmianami w komórkach wyścielających dolny przełyk);
- Jeśli pacjent został poinformowany przez lekarza, że nie toleruje niektórych cukrów (takich jak laktoza)
- Jeśli u pacjenta występuje lub występował ból, obrzęk lub drętwienie szczęki lub uczucie „ciężkiej szczęki i (lub) szczęki” lub obluzowania zęba;
- W przypadku leczenia stomatologicznego lub planowanego zabiegu dentystycznego należy poinformować dentystę o leczeniu lekiem Actonel.
W przypadku wystąpienia któregokolwiek z tych problemów lekarz poinformuje Cię, co należy zrobić, aby przyjmować Actonel.
Dzieci i młodzież
Nie zaleca się stosowania ryzedronianu sodu u dzieci w wieku poniżej 18 lat ze względu na niewystarczające dane dotyczące bezpieczeństwa i skuteczności.
Interakcje Jakie leki lub pokarmy mogą modyfikować działanie Actonelu
Leki zawierające którykolwiek z poniższych składników zmniejszają działanie leku Actonel, gdy są przyjmowane w tym samym czasie:
- piłka nożna
- magnez
- aluminium (np. niektóre preparaty na problemy trawienne)
- żelazo
Leki te należy przyjmować co najmniej trzydzieści minut po przyjęciu tabletki Actonel.
Należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent przyjmuje, ostatnio przyjmował lub może przyjmować jakiekolwiek inne leki.
Actonel z jedzeniem i piciem
Bardzo ważne jest, aby NIE przyjmować tabletki Actonel z jedzeniem lub piciem (z wyjątkiem wody z kranu), ponieważ może to zmniejszyć skuteczność leku.
W szczególności nie należy przyjmować tego leku razem z produktami mlecznymi (w tym mlekiem), ponieważ zawierają one wapń (patrz punkt „Inne leki i Actonel”).
Jedzenie i napoje (z wyjątkiem wody z kranu) należy przyjmować co najmniej 30 minut po przyjęciu tabletki Actonel.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
Ciąża i karmienie piersią
NIE WOLNO przyjmować leku Actonel, jeśli pacjentka jest w ciąży, może być w ciąży lub planuje zajść w ciążę (patrz punkt „Kiedy nie stosować leku Actonel”). Potencjalne zagrożenia związane ze stosowaniem „ryzedronianu sodu (substancji czynnej leku Actonel) u kobiet w ciąży są nieznane. NIE WOLNO przyjmować leku Actonel w okresie karmienia piersią (patrz punkt „Kiedy nie stosować leku Actonel”).
Prowadzenie i używanie maszyn
Actonel nie ma znanych działań wpływających na zdolność prowadzenia pojazdów lub obsługiwania maszyn.
Actonel zawiera niewielką ilość laktozy (patrz punkt „Ostrzeżenia i środki ostrożności”).
Dawka, sposób i czas podawania Jak stosować Actonel: dawkowanie
Ten lek należy zawsze stosować zgodnie z zaleceniami lekarza lub farmaceuty. W razie wątpliwości skonsultuj się z lekarzem lub farmaceutą.
Zalecana dawka:
Należy przyjmować JEDNĄ tabletkę Actonel (5 mg ryzedronianu sodu) raz na dobę.
Dla Twojej wygody na odwrocie blistra nadrukowano dni tygodnia, aby pomóc Ci pamiętać o zażyciu tabletki.
KIEDY przyjmować tabletkę Actonel?
Bardzo WAŻNE jest przyjmowanie leku Actonel co najmniej 30 minut przed posiłkiem lub napojem (z wyjątkiem wody z kranu) lub innym lekiem przyjmowanym w ciągu dnia.
W szczególnym przypadku, gdy podanie przed śniadaniem nie jest możliwe, Actonel można przyjmować codziennie o tej samej porze, na pusty żołądek, w jeden z następujących sposobów:
- między posiłkami: co najmniej 2 godziny po ostatnim spożyciu posiłku, napoju (oprócz wody z kranu) lub innego leku. Nie jeść ani nie pić (z wyjątkiem wody z kranu) przez 2 godziny po zażyciu tabletki Actonel.
Lub
- wieczorem: Actonel należy przyjmować co najmniej 2 godziny po ostatnim spożyciu w danym dniu posiłku, napoju (z wyjątkiem wody z kranu) lub produktu leczniczego. Actonel należy przyjmować co najmniej 30 minut przed snem.
JAK przyjmować tabletkę Actonel
- Tabletkę należy przyjmować trzymając tułów w pozycji pionowej (stojąc lub siedząc), aby uniknąć zgagi.
- Tabletkę należy połknąć, popijając co najmniej jedną szklanką (120 ml) wody z kranu.
- Tabletkę należy połykać w całości, nie rozpuszczać ani nie żuć.
- Po połknięciu tabletki nie należy kłaść się przez 30 minut.
Twój lekarz poinformuje Cię, czy potrzebujesz suplementów wapnia i witamin, jeśli masz niewystarczające spożycie tych substancji w swojej diecie.
Przedawkowanie Co zrobić, jeśli pacjent przyjął zbyt dużą dawkę leku Actonel
Przyjęcie większej niż zalecana dawki leku Actonel
Jeśli Ty lub ktokolwiek inny przypadkowo połknął więcej tabletek Actonel niż przepisano, wypij pełną szklankę mleka i skonsultuj się z lekarzem.
Pominięcie przyjęcia leku Actonel
Jeśli zapomniałeś przyjąć tabletkę o zaplanowanej porze, zażyj ją tak szybko, jak to możliwe, zgodnie z powyższymi instrukcjami (np. przed śniadaniem, między posiłkami lub wieczorem).
NIE NALEŻY przyjmować dwóch tabletek tego samego dnia w celu uzupełnienia pominiętej tabletki.
Przerwanie stosowania leku Actonel
Jeśli przestaniesz, możesz zacząć tracić masę kostną. Dlatego zaleca się skonsultowanie się z lekarzem przed przerwaniem leczenia.
W przypadku dalszych pytań dotyczących stosowania tego leku należy zwrócić się do lekarza lub farmaceuty.
Skutki uboczne Jakie są skutki uboczne Actonelu?
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Należy przerwać przyjmowanie leku Actonel i natychmiast skontaktować się z lekarzem, jeśli wystąpi którykolwiek z następujących działań niepożądanych:
- Objawy ciężkiej reakcji alergicznej, takie jak:
- Obrzęk twarzy, języka lub gardła
- Trudności z połykaniem
- Pokrzywka i trudności w oddychaniu
- Ciężkie reakcje skórne, które mogą obejmować powstawanie pęcherzy skórnych
Skonsultuj się z lekarzem, jeśli wystąpią następujące działania niepożądane:
- Zapalenie oka, zwykle z bólem, zaczerwienieniem i wrażliwością na światło
- Martwica kości szczęki (martwica kości) związana z opóźnionym gojeniem i zakażeniem, często po ekstrakcji zęba (patrz punkt „Ostrzeżenia i środki ostrożności”)
- Objawy przełyku, takie jak ból podczas przełykania, trudności w połykaniu, ból w klatce piersiowej lub początek / nasilenie zgagi
Rzadko może wystąpić nietypowe złamanie kości udowej, szczególnie u pacjentów długotrwale leczonych z powodu osteoporozy. W przypadku odczuwania bólu, osłabienia lub dyskomfortu w obrębie uda, biodra lub pachwiny należy skontaktować się z lekarzem, ponieważ może to być wczesnym wskazaniem możliwego złamanie kości udowej.
Jednak inne działania niepożądane obserwowane w badaniach klinicznych były na ogół łagodne i nie wymagały przerwania leczenia.
Częste działania niepożądane (mogą dotyczyć do 1 na 10 osób)
- Niestrawność, nudności, ból brzucha, skurcze lub rozstrój żołądka, zaparcia, uczucie sytości, wzdęcia, biegunka.
- Ból kości, mięśni lub stawów.
- Bół głowy.
Niezbyt częste działania niepożądane (mogą wystąpić u 1 na 100 osób)
- Zapalenie lub owrzodzenie przełyku (przewod łączący jamę ustną z żołądkiem), które powoduje trudności i ból w przełykaniu (patrz także punkt „Ostrzeżenia i środki ostrożności”), zapalenie żołądka i dwunastnicy (pierwsza część jelita, gdzie przepuszcza strawiony pokarm z żołądka).
- Zapalenie kolorowej części oka (tęczówki) (zaczerwienione i bolesne oczy z możliwymi zmianami widzenia).
Rzadkie działania niepożądane (mogą wystąpić u 1 na 1000 osób)
- Zapalenie języka (czerwony, opuchnięty, prawdopodobnie bolesny), zwężenie przełyku (przewod łączący jamę ustną z żołądkiem).
- Zgłaszano nieprawidłowości w testach czynności wątroby. Można to zdiagnozować dopiero po badaniu krwi.
Podczas wprowadzania do obrotu zgłoszono następujące działania niepożądane (częstość nieznana):
- Włosy i/lub wypadanie włosów
- Zaburzenia wątroby, w niektórych ciężkich przypadkach.
Rzadko na początku leczenia stężenie wapnia i fosforanów w osoczu pacjenta może spaść; zmiany te są zwykle niewielkie i nie powodują żadnych objawów.
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe działania niepożądane niewymienione w tej ulotce, należy porozmawiać z lekarzem lub farmaceutą.
Wygaśnięcie i przechowywanie
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na pudełku i blistrze po „EXP”.Termin ważności oznacza ostatni dzień podanego miesiąca.
Ten lek nie wymaga żadnych specjalnych warunków przechowywania.
Nie należy wyrzucać żadnych leków do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa.Pomoże to chronić środowisko.
Co zawiera Actonel
Substancją czynną jest rizedronian sodu. Każda tabletka zawiera 5 mg rizedronianu sodu, co odpowiada 4,64 mg kwasu rizedronowego.
Pozostałe składniki to:
Rdzeń tabletu: laktoza jednowodna (patrz punkt 2), krospowidon, stearynian magnezu i celuloza mikrokrystaliczna.
Powłoka: hypromeloza, makrogol, hydroksypropyloceluloza, dwutlenek krzemu, dwutlenek tytanu [E171], żółty tlenek żelaza [E172].
Jak wygląda Actonel i co zawiera opakowanie
Tabletki powlekane Actonel 5 mg są owalne i koloru żółtego z literami „RSN” po jednej stronie i „5 mg” po drugiej.Są one dostępne w opakowaniach po 14, 28 (2x14), 84 (6x14). , 140 (10x14) tabletek Niektóre wielkości opakowań mogą nie być dostępne w obrocie.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO
ACTONEL 5 MG TABLETKI POWLEKANE FOLIĄ
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY
Każda tabletka powlekana zawiera 5 mg rizedronianu sodu (co odpowiada 4,64 mg kwasu rizedronowego).
Substancje pomocnicze o znanym działaniu:
Każda tabletka powlekana zawiera 156,0 mg laktozy jednowodnej (co odpowiada 148,2 mg laktozy).
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
03.0 POSTAĆ FARMACEUTYCZNA
Tabletki powlekane.
Żółte, owalne tabletki powlekane z wytłoczonym RSN po jednej stronie i 5 mg po drugiej.
04.0 INFORMACJE KLINICZNE
04.1 Wskazania terapeutyczne
Leczenie osteoporozy pomenopauzalnej w celu zmniejszenia ryzyka złamań kręgów.
Leczenie jawnej osteoporozy pomenopauzalnej w celu zmniejszenia ryzyka złamań szyjki kości udowej. Zapobieganie osteoporozie pomenopauzalnej u kobiet ze zwiększonym ryzykiem osteoporozy (patrz punkt 5.1).
Utrzymanie lub zwiększenie masy kostnej u kobiet po menopauzie otrzymujących ogólnoustrojową terapię kortykosteroidami przez dłuższy czas (ponad trzy miesiące) w dawce równej lub większej niż 7,5 mg/dobę prednizonu lub równoważnych związków.
04.2 Dawkowanie i sposób podawania
Dawkowanie
Zalecana dzienna dawka dla dorosłych to jedna tabletka 5 mg doustnie.
Sposób podawania
Pokarm ma wpływ na wchłanianie preparatu Actonel, dlatego w celu zapewnienia odpowiedniego wchłaniania pacjenci powinni przyjmować preparat Actonel:
• Rano, przed śniadaniem: co najmniej 30 minut przed spożyciem pierwszego posiłku, innych produktów leczniczych lub napojów danego dnia (z wyjątkiem wody z kranu).
W szczególnym przypadku, gdy podanie przed śniadaniem nie jest możliwe, Actonel można przyjmować codziennie o tej samej porze, między posiłkami lub wieczorem, ściśle przestrzegając poniższych instrukcji, aby upewnić się, że Actonel jest przyjmowany na pusty żołądek:
• Między posiłkami: Actonel należy przyjmować co najmniej 2 godziny przed lub co najmniej 2 godziny po posiłku, produkcie leczniczym lub napoju (z wyjątkiem wody z kranu)
• Wieczorem: Actonel należy przyjmować co najmniej 2 godziny po ostatnim posiłku, lekarstwie lub napoju w ciągu dnia (z wyjątkiem wody z kranu). Actonel należy przyjmować co najmniej 30 minut przed snem.
Jeśli od czasu do czasu pominięto dawkę, Actonel można przyjmować rano przed śniadaniem, między posiłkami lub wieczorem, jak opisano w powyższej instrukcji.
Tabletkę należy połykać w całości, nie rozpuszczać ani nie żuć. Aby ułatwić przejście tabletki przez przełyk, należy zażywać Actonel popijając szklanką wody z kranu (≥120 ml), trzymając tułów w pozycji pionowej. Po spożyciu tabletki pacjenci powinni unikać kładzenia się spać przez 30 minut (patrz punkt 4.4).
W przypadku niedostatecznej podaży w diecie należy rozważyć suplementację wapnia i witaminy D.
Nie ustalono optymalnego czasu trwania leczenia bisfosfonianami osteoporozy.Konieczność kontynuacji leczenia powinna być okresowo oceniana u każdego pacjenta indywidualnie w oparciu o potencjalne korzyści i zagrożenia, szczególnie po 5 lub więcej latach stosowania.
Populacje specjalne
Starsi pacjenci
Nie jest wymagane dostosowanie dawki, ponieważ stwierdzono, że biodostępność, dystrybucja i eliminacja u osób w podeszłym wieku (>60 lat) są podobne do tych u młodszych osób.
Upośledzona czynność nerek
Nie ma konieczności dostosowania dawki u pacjentów z łagodnymi do umiarkowanych zaburzeniami czynności nerek. Stosowanie ryzedronianu sodu jest przeciwwskazane u pacjentów z ciężkimi zaburzeniami czynności nerek (klirens kreatyniny poniżej 30 ml/min) (patrz punkty 4.3 i 5.2).
Populacja pediatryczna
Nie zaleca się stosowania ryzedronianu sodu u dzieci w wieku poniżej 18 lat ze względu na niewystarczające dane dotyczące bezpieczeństwa i skuteczności (patrz również punkt 5.1).
04.3 Przeciwwskazania
- Nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1.
- Hipokalcemia (patrz punkt 4.4).
- Ciąża i karmienie piersią.
- Ciężkie zaburzenia czynności nerek (klirens kreatyniny
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania
Żywność, napoje (z wyjątkiem wody z kranu) i produkty lecznicze zawierające kationy wielowartościowe (takie jak wapń, magnez, żelazo i glin) zakłócają wchłanianie bisfosfonianów i nie należy ich przyjmować jednocześnie z preparatem Actonel (patrz punkt 4.5). Aby osiągnąć pożądaną skuteczność, należy ściśle przestrzegać instrukcji podawania (patrz punkt 4.2).
Skuteczność bisfosfonianów w leczeniu osteoporozy pomenopauzalnej jest związana z występowaniem zmniejszonej gęstości mineralnej kości obliczonej za pomocą Bone Mineral Density (T-score BMD dla kręgosłupa biodrowego lub lędźwiowego ≤-2,5 SD) i/lub występowaniem złamań.
Starszy wiek lub kliniczne czynniki ryzyka złamań same w sobie nie uzasadniają rozpoczęcia leczenia osteoporozy bisfosfonianami.
Istnieją ograniczone dowody potwierdzające skuteczność bisfosfonianów, w tym Actonelu, u kobiet w bardzo podeszłym wieku (powyżej 80 lat) (patrz punkt 5.1).
Bisfosfoniany są związane z zapaleniem przełyku, zapaleniem żołądka, wrzodami przełyku i wrzodami żołądka i dwunastnicy. Dlatego należy zachować ostrożność:
• u pacjentów z chorobami przełyku w wywiadzie powodującymi opóźniony pasaż przełykowy lub opróżnianie żołądka, takie jak zwężenie lub achalazja
• u pacjentów niezdolnych do utrzymania wyprostowanego tułowia przez co najmniej 30 minut po przyjęciu tabletki
• jeśli risedronian jest podawany pacjentom z aktualnymi lub niedawnymi problemami dotyczącymi górnego odcinka przewodu pokarmowego lub przełyku (w tym ze zdiagnozowanym przełykiem Barretta).
Lekarze powinni podkreślić pacjentom, jak ważne jest zwracanie uwagi na instrukcje dotyczące podawania i zwracanie uwagi na pojawienie się wszelkich oznak lub objawów wskazujących na możliwą reakcję przełyku.Pacjent powinien być poinformowany, że jeśli wystąpią objawy podrażnienia przełyku, takie jak dysfagia, ból przełykania , ból zamostkowy lub początek / nasilenie zgagi, należy natychmiast zwrócić się o pomoc lekarską.
Przed rozpoczęciem leczenia preparatem Actonel należy skorygować hipokalcemię. Niezbędna jest również korekta innych zaburzeń gospodarki kostnej i mineralnej (np. dysfunkcja przytarczyc, hipowitaminoza D) podczas rozpoczynania terapii preparatem Actonel.
Martwicę kości szczęki, zwykle związaną z ekstrakcją zęba i (lub) miejscowym zakażeniem (w tym zapaleniem kości i szpiku), zgłaszano u pacjentów z nowotworami, leczonych schematami obejmującymi bisfosfoniany podawanymi głównie dożylnie.Wielu z tych pacjentów było również leczonych chemioterapią i kortykosteroidami. zgłaszano również przypadki szczęki u pacjentów z osteoporozą leczonych doustnymi bisfosfonianami.
Przed rozpoczęciem leczenia bisfosfonianami u pacjentów ze współistniejącymi czynnikami ryzyka (takimi jak nowotwory, chemioterapia, radioterapia, kortykosteroidy, zła higiena jamy ustnej) należy rozważyć konieczność wykonania badania stomatologicznego z odpowiednimi profilaktycznymi zabiegami stomatologicznymi.
W trakcie leczenia pacjenci ci powinni w miarę możliwości unikać inwazyjnych zabiegów stomatologicznych. U pacjentów, u których podczas leczenia bisfosfonianami rozwinęła się martwica kości szczęki, chirurgia stomatologiczna może zaostrzyć stan. W przypadku pacjentów wymagających zabiegu stomatologicznego brak dostępnych danych sugerujących, że przerwanie leczenia bisfosfonianami zmniejsza ryzyko martwicy kości szczęki i (lub) szczęki.
Ocena kliniczna lekarza musi kierować programem leczenia każdego pacjenta, w oparciu o indywidualną ocenę stosunku ryzyka do korzyści.
Nietypowe złamania kości udowej
Zgłaszano nietypowe złamania podkrętarzowe i trzonu kości udowej, głównie u pacjentów długotrwale leczonych bisfosfonianami z powodu osteoporozy.Te krótkie złamania poprzeczne lub skośne mogą wystąpić w dowolnym miejscu kości udowej, od miejsca tuż poniżej krętarza mniejszego do powyżej linii nadkłykciowej. występują samoistnie lub po minimalnym urazie, a niektórzy pacjenci odczuwają ból uda lub pachwiny, często związany z wynikami badań obrazowych i radiograficznymi dowodami złamań przeciążeniowych, tygodnie lub miesiące przed wystąpieniem złamań przeciążeniowych. Złamania są często dwustronne; dlatego u pacjentów leczonych bisfosfonianami, u których doszło do złamania trzonu kości udowej, należy zbadać drugą kość udową. Zgłaszano również ograniczone gojenie tych złamań.U pacjentów z podejrzeniem atypowego złamania kości udowej należy rozważyć przerwanie leczenia bisfosfonianami do czasu oceny pacjenta w oparciu o indywidualne korzyści/ryzyko.
Podczas leczenia bisfosfonianami należy doradzić pacjentom, aby zgłaszali wszelkie bóle uda, biodra lub pachwiny, a każdego pacjenta, u którego występują takie objawy, należy zbadać pod kątem obecności niecałkowitego złamania kości udowej.
Ten produkt leczniczy zawiera laktozę. Pacjenci z rzadką dziedziczną nietolerancją galaktozy, niedoborem laktazy typu Lapp lub zespołem złego wchłaniania glukozy-galaktozy nie powinni przyjmować tego produktu leczniczego.
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji
Nie przeprowadzono badań interakcji z innymi lekami, jednak w badaniach klinicznych nie zaobserwowano klinicznie istotnych interakcji z innymi produktami leczniczymi.
Jednoczesne stosowanie produktów leczniczych zawierających kationy wielowartościowe (np. wapń, magnez, żelazo i glin) zaburza wchłanianie rizedronianu sodu (patrz punkt 4.4).
Ryzedronian sodu nie jest metabolizowany ogólnoustrojowo, nie indukuje enzymów cytochromu P-450 i słabo wiąże się z białkami.
W badaniach III fazy ryzedronianu sodu w leczeniu osteoporozy 33% i 45% pacjentów otrzymywało odpowiednio kwas acetylosalicylowy lub inne niesteroidowe leki przeciwzapalne (NLPZ).
Jeśli zostanie to uznane za właściwe, ryzedronian sodu można stosować jednocześnie z estrogenową terapią zastępczą.
04.6 Ciąża i laktacja
Nie ma wystarczających danych dotyczących leczenia kobiet w ciąży ryzedronianem sodu. Badania na zwierzętach wykazały toksyczny wpływ na reprodukcję (patrz punkt 5.3). Potencjalne ryzyko dla ludzi nie jest znane.Badania na zwierzętach wskazują, że niewielka ilość rizedronianu sodu przenika do mleka matki.
Ryzedronian sodu nie powinien być podawany kobietom w ciąży lub karmiącym piersią.
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Actonel nie ma wpływu lub ma nieistotny wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn.
04.8 Działania niepożądane
Ryzedronian sodu badano w badaniach klinicznych III fazy z udziałem ponad 15 000 pacjentów. Większość działań niepożądanych obserwowanych w badaniach klinicznych miała nasilenie łagodne lub umiarkowane i zwykle nie wymagała przerwania leczenia.
Wymieniono działania niepożądane, które wystąpiły podczas badań klinicznych III fazy u kobiet z osteoporozą pomenopauzalną leczonych przez okres do 36 miesięcy ryzedronianem w dawce 5 mg/dobę (n = 5020) lub placebo (n = 5048) i uważane za prawdopodobnie lub prawdopodobnie związane z ryzedronianem. stosując następującą definicję (częstość występowania w porównaniu z placebo podano w nawiasach): bardzo często (≥1/10), często (≥1/100;
Zaburzenia układu nerwowego.
Często: ból głowy (1,8% vs 1,4%)
Zaburzenia oka.
Niezbyt często: zapalenie tęczówki *
Zaburzenia żołądkowo-jelitowe.
Często: zaparcia (5,0% vs 4,8%), niestrawność (4,5% vs 4,1%), nudności (4,3% vs 4,0%), ból brzucha (3,5% vs 3,3%), biegunka (3,0% vs 2,7 %)
Niezbyt często: zapalenie żołądka (0,9% vs 0,7%), zapalenie przełyku (0,9% vs 0,9%), dysfagia (0,4% vs 0,2%), zapalenie dwunastnicy (0,2% vs 0,1%), owrzodzenie przełyku (0,2% vs 0,2) %)
Rzadko: zapalenie języka (zwężenie przełyku (
Zaburzenia mięśniowo-szkieletowe i tkanki łącznej.
Często: ból mięśniowo-szkieletowy (2,1% vs 1,9%)
Testy diagnostyczne.
Rzadko: nieprawidłowe wyniki testów czynności wątroby*
* Brak istotnej częstości występowania w badaniach klinicznych III fazy dotyczących osteoporozy; częstość jest oparta na danych dotyczących zdarzeń niepożądanych / danych laboratoryjnych / ponownego prowokacji z poprzednich badań klinicznych.
Parametry laboratoryjne.
U niektórych pacjentów obserwowano początkowe łagodne, przemijające i bezobjawowe zmniejszenie stężenia wapnia i fosforanów w surowicy.
Następujące dodatkowe działania niepożądane zostały zgłoszone po wprowadzeniu do obrotu (częstość nieznana)
Zaburzenia oka.
Zapalenie tęczówki, zapalenie błony naczyniowej oka
Zaburzenia mięśniowo-szkieletowe i tkanki łącznej.
Martwica kości żuchwy i/lub szczęki
Zaburzenia skóry i tkanki podskórnej.
Reakcje skórne i reakcje nadwrażliwości, w tym obrzęk naczynioruchowy, uogólniona wysypka, pokrzywka i pęcherzowe reakcje skórne, niektóre ciężkie, w tym pojedyncze przypadki zespołu Stevensa Johnsona, toksyczno-rozpływna martwica naskórka i leukocytoklastyczne zapalenie naczyń.
Włosy i/lub wypadanie włosów.
Zaburzenia układu odpornościowego.
Reakcje anafilaktyczne
Zaburzenia wątroby i dróg żółciowych.
Ciężka choroba wątroby. W większości zgłoszonych przypadków pacjenci byli również leczeni innymi produktami, o których wiadomo, że wywołują chorobę wątroby.
Po wprowadzeniu produktu do obrotu zgłaszano następujące reakcje (rzadko):
Nietypowe złamania podkrętarzowe i trzonu kości udowej (działanie niepożądane klasy bisfosfonianów).
04.9 Przedawkowanie
Brak konkretnych danych dotyczących leczenia przypadków przedawkowania ryzedronianu sodu.
W przypadku przedawkowania można spodziewać się zmniejszenia stężenia wapnia w surowicy. Niektórzy z tych pacjentów mogą również mieć oznaki i objawy hipokalcemii.
W celu związania ryzedronianu sodu i zmniejszenia jego wchłaniania należy podawać mleko lub leki zobojętniające zawierające magnez, wapń lub glin.W przypadku przedawkowania można rozważyć płukanie żołądka w celu usunięcia niewchłoniętego ryzedronianu sodu.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE
05.1 Właściwości farmakodynamiczne
Kategoria farmakoterapeutyczna: bisfosfoniany.
Kod ATC M05BA07.
Mechanizm akcji
Ryzedronian sodu jest pirydynylobisfosfonianem, który przyłącza się do hydroksyapatytu kości i hamuje resorpcję kości przez osteoklasty. Obrót kostny jest zmniejszony przy zachowaniu aktywności osteoblastów i mineralizacji kości.
Efekty farmakodynamiczne
W badaniach przedklinicznych ryzedronian sodu wykazywał silne działanie przeciwosteoklastyczne i przeciwresorpcyjne, powodując zależne od dawki zwiększenie masy kostnej i biomechanicznej wytrzymałości kości.Aktywność ryzedronianu sodu potwierdzono pomiarami wskaźników biochemicznych obrotu kostnego. badania farmakodynamiczne i kliniczne. Spadki wskaźników biochemicznych obrotu kostnego były obserwowane w pierwszym miesiącu i osiągały szczyt w ciągu 3-6 miesięcy.
Skuteczność kliniczna i bezpieczeństwo
Terapia i profilaktyka osteoporozy pomenopauzalnej
Z osteoporozą pomenopauzalną wiąże się wiele czynników ryzyka, w tym zmniejszenie masy kostnej, zmniejszenie gęstości mineralnej kości, wczesna menopauza, palenie tytoniu oraz występowanie osteoporozy w wywiadzie rodzinnym.Klinicznym następstwem osteoporozy jest zwiększona częstość złamań. Ryzyko złamań wzrasta wraz ze wzrostem czynników ryzyka.
Program rozwoju klinicznego oceniał wpływ sodu ryzedronianu na ryzyko złamań szyjki kości udowej i kręgów i obejmował kobiety po menopauzie, zarówno wczesne, jak i późne, ze złamaniami lub bez.Oceniano dawki 2,5 mg i 5 mg na dobę i wszystkie grupy, w tym kontrolne, otrzymywały wapń i witaminę D (jeśli poziom wyjściowy był obniżony).
Bezwzględne i względne ryzyko nowych złamań kręgów i szyjki kości udowej obliczono za pomocą „analizy”czas do pierwszego wydarzenia'.
• Dwa badania kontrolowane placebo (n = 3661) obejmowały kobiety po menopauzie w wieku poniżej 85 lat ze złamaniami kręgów w punkcie początkowym.Rizedronian sodu w dawce 5 mg na dobę podawany przez 3 lata powodował zmniejszenie ryzyka nowych złamań kręgów w porównaniu z grupą kontrolną Grupa.
U kobiet z co najmniej 2 złamaniami kręgów lub 1 złamaniem kręgów względne zmniejszenie ryzyka nowych złamań wynosiło odpowiednio 49% i 41% (częstość nowych złamań kręgów po podaniu ryzedronianu wynosiła odpowiednio 18,1% i 11,3%, podczas gdy placebo odpowiednio 29% i 16,3%).Efekt leczenia obserwowano już od końca pierwszego roku terapii. Korzyści wykazano również u kobiet z licznymi złamaniami na początku badania. Ryzedronian sodu w dawce 5 mg dziennie zmniejszał roczną utratę masy ciała w porównaniu z grupą kontrolną.
• Do dwóch dodatkowych badań kontrolowanych placebo włączono kobiety po menopauzie w wieku powyżej 70 lat ze złamaniami kręgów lub bez nich. gęstość szyjki kości udowej. Statystycznie skuteczność ryzedronianu sodu w porównaniu z placebo została osiągnięta tylko w przypadku połączenia dwóch grup leczonych dawką 2,5 mg i 5 mg Poniższe wyniki są oparte wyłącznie na analizie post-post podgrup pacjentów wybranych z przypadków klinicznych lub na podstawie aktualnej definicji osteoporozy:
° W podgrupie pacjentów z BMD T-score szyjki kości udowej ≤-2,5 SD (NHANES III) i co najmniej jednym początkowym złamaniem kręgu, ryzedronian podawany przez trzy lata zmniejszał ryzyko złamania szyjki kości udowej. grupa kontrolna (częstość złamań szyjki kości udowej w grupach leczonych ryzedronianem sodu 2,5 mg i 5 mg wynosiła 3,8%, w grupie placebo 7,4%).
° Dane sugerują, że bardziej ograniczona ochrona jest widoczna u starszych pacjentów (≥80 lat). Może to być konsekwencją rosnącego na przestrzeni lat znaczenia pozaszkieletowych czynników ryzyka złamania szyjki kości udowej.
° W tych badaniach analiza drugorzędowych punktów końcowych wykazała zmniejszone ryzyko nowych złamań kręgów u pacjentów ze zmniejszoną BMD szyjki kości udowej bez złamań oraz u pacjentów ze zmniejszoną BMD szyjki kości udowej ze złamaniami lub bez.
Ryzedronian sodu w dawce 5 mg na dobę podawany przez 3 lata zwiększał gęstość mineralną kości (BMD) kręgosłupa lędźwiowego, szyjki kości udowej, krętarza i nadgarstka w porównaniu z grupą kontrolną i zapobiegał utracie masy kostnej w dystalnej jednej trzeciej kości promieniowej.
• Szybkie zmniejszenie działania hamującego ryzedronianu sodu na wskaźnik obrotu kostnego zaobserwowano w „roku następującym po przerwaniu leczenia po trzech latach leczenia ryzedronianem w dawce 5 mg na dobę”.
• U kobiet po menopauzie otrzymujących zastępczą terapię estrogenową ryzedronian sodu w dawce 5 mg na dobę zwiększał w ograniczonym stopniu gęstość mineralną kości (BMD) w szyjce kości udowej i dystalnej jednej trzeciej kości promieniowej w porównaniu z pacjentkami stosującymi wyłącznie estrogeny.
• Biopsje kości wykonywane u kobiet po menopauzie leczonych preparatem Actonel 5 mg na dobę przez 2-3 lata wykazały oczekiwane umiarkowane zmniejszenie obrotu kostnego. Stwierdzono, że tkanka kostna podczas leczenia rizedronianem sodu ma prawidłową strukturę blaszkowatą i szybkość mineralizacji kości. Dane te, wraz ze zmniejszoną częstością osteoporotycznych złamań kręgów u kobiet z osteoporozą, wydają się wskazywać na brak szkodliwego wpływu na jakość kości.
• Pomiary endoskopowe przeprowadzone u wielu pacjentów, zarówno leczonych ryzedronianem sodu, jak i należących do grupy kontrolnej, cierpiących na różne zaburzenia żołądkowo-jelitowe o nasileniu od umiarkowanego do ciężkiego, nie wykazały owrzodzeń przełyku, żołądka lub dwunastnicy związanych z terapią, chociaż przypadki zapalenia dwunastnicy obserwowano niezbyt często w grupie rizedronianu sodu.
• W porównawczym badaniu klinicznym u kobiet z osteoporozą pomenopauzalną leczonych jedną dawką przed śniadaniem lub dawką o innej porze dnia, wzrost gęstości mineralnej kości kręgosłupa lędźwiowego był statystycznie wyższy w przypadku dawki przyjmowanej przed śniadaniem.
• U kobiet po menopauzie z osteopenią, ryzedronian sodu wykazywał przewagę nad placebo w zwiększaniu BMD kręgosłupa lędźwiowego po 12 i 24 miesiącach.
Osteoporoza wywołana kortykosteroidami
Program rozwoju klinicznego ryzedronianu sodu obejmował pacjentów, którzy rozpoczęli leczenie kortykosteroidami (≥ 7,5 mg/dobę prednizonu lub odpowiednika) w ciągu 3 miesięcy przed rozpoczęciem badań lub pacjentów, którzy otrzymywali kortykosteroidy przez ponad 6 miesięcy. następujące:
- Ryzedronian sodu 5 mg dziennie przez rok utrzymuje lub zwiększa gęstość mineralną kości w porównaniu z grupą kontrolną na poziomie odcinka lędźwiowego kręgosłupa, szyjki kości udowej i krętarza.
- Ryzedronian sodu w dawce 5 mg na dobę zmniejsza częstość występowania złamań kręgów po 1 roku w porównaniu z grupą kontrolną, ocenianą ze względów bezpieczeństwa na podstawie zbiorczej analizy badań.
- badanie histologiczne biopsji kości pacjentów leczonych kortykosteroidami i leczonych ryzedronianem sodu w dawce 5 mg na dobę nie wykazało zmian w procesie mineralizacji.
Populacja pediatryczna
Bezpieczeństwo i skuteczność ryzedronianu sodu są oceniane w trwającym badaniu u dzieci i młodzieży w wieku od 4 do mniej niż 16 lat z wrodzoną łamliwością kości. statystycznie istotny wzrost BMD kręgosłupa lędźwiowego wykazano w grupie ryzedronianu w porównaniu z grupą placebo; jednak w grupie ryzedronianu w porównaniu z placebo stwierdzono wzrost liczby co najmniej 1 nowego morfometrycznego złamania kręgu (ocenianego radiologicznie). wyniki nie potwierdzają stosowania rizedronianu sodu u dzieci i młodzieży z wrodzoną łamliwością kości.
05.2 „Właściwości farmakokinetyczne
Wchłanianie
Wchłanianie dawki doustnej jest stosunkowo szybkie (tmax ~ 1 godzina) i jest niezależne od dawki w badanych dawkach (2,5 do 30 mg). Biodostępność po podaniu doustnym tabletki wynosi średnio 0,63% i zmniejsza się, gdy rizedronian sodu jest podawany z pokarmem. Biodostępność była podobna u mężczyzn i kobiet.
Dystrybucja
Średnia objętość dystrybucji w stanie stacjonarnym u ludzi wynosi 6,3 l/kg, a frakcja związana z białkami osocza leku wynosi około 24%.
Biotransformacja
Nie ma dowodów na to, że ryzedronian sodu jest metabolizowany ogólnoustrojowo.
Eliminacja
Około połowa wchłoniętej dawki jest wydalana z moczem w ciągu 24 godzin, natomiast 85% dawki dożylnej wydalane jest z moczem po 28 dniach.Średni klirens nerkowy wynosi 105 ml/min, a całkowity klirens 122 ml/min: różnica jest prawdopodobnie związana z klirensem spowodowanym „adsorpcją do kości". Klirens nerkowy nie zależy od stężenia i istnieje liniowa zależność między klirensem nerkowym a klirensem kreatyniny. Niewchłonięty ryzedronian sodu jest wydalany w postaci niezmienionej z kałem Po podaniu doustnym krzywa zależności stężenia od czasu wykazuje trzy fazy eliminacji z końcowym okresem półtrwania wynoszącym 480 godzin.
Populacje specjalne
Starsi pacjenci
Nie jest konieczne dostosowanie dawki.
Pacjenci leczeni kwasem acetylosalicylowym lub innymi niesteroidowymi lekami przeciwzapalnymi (NLPZ)
Wśród pacjentów leczonych regularnie (trzy lub więcej dni w tygodniu) kwasem acetylosalicylowym lub innymi NLPZ, częstość występowania działań niepożądanych dotyczących górnego odcinka przewodu pokarmowego w grupie leczonej Actonelem była podobna jak w grupie kontrolnej.
05.3 Przedkliniczne dane o bezpieczeństwie
W badaniach toksykologicznych na szczurach i psach obserwowano zależne od dawki działanie hepatotoksyczne ryzedronianu sodu, głównie jako zwiększenie aktywności enzymów ze zmianami histologicznymi u szczurów. Znaczenie kliniczne tych obserwacji nie jest znane. Toksyczność dla jąder wystąpiła u szczurów i psów przy ekspozycji przekraczającej ekspozycję terapeutyczną u ludzi. U gryzoni często obserwowano zależne od dawki podrażnienie górnych dróg oddechowych.
Podobne efekty odnotowano w przypadku innych bisfosfonianów. W długoterminowych badaniach na gryzoniach obserwowano wpływ na dolne drogi oddechowe, jednak kliniczne znaczenie tych wyników nie jest jasne. W badaniach toksycznego wpływu na reprodukcję przy ekspozycji bliskiej klinicznemu zaobserwowano zmiany w kostnieniu na poziomie mostka i (lub) czaszki u płodów leczonych szczurów oraz hipokalcemię i śmiertelność u leczonych samic, które urodziły. 3,2 mg/kg/dobę u szczurów i 10 mg/kg/dobę u królików, chociaż dane są dostępne tylko dla ograniczonej liczby królików Toksyczność u matek uniemożliwiła badanie wyższych dawek. dla ludzi.
06.0 INFORMACJE FARMACEUTYCZNE
06.1 Zaróbki
Rdzeń tabletu: Monohydrat laktozy,
celuloza mikrokrystaliczna,
krospowidon,
stearynian magnezu.
Powłoka: Żółty tlenek żelaza E 172,
hypromeloza,
makrogol,
hydroksypropyloceluloza,
dwutlenek krzemu,
dwutlenek tytanu E171.
06.2 Niekompatybilność
Nieistotne.
06.3 Okres ważności
5 lat.
06.4 Specjalne środki ostrożności przy przechowywaniu
Ten lek nie wymaga żadnych specjalnych warunków przechowywania.
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania
Nieprzezroczysty blister PVC/Aluminium zawierający 14 tabletek w pudełku tekturowym, liczba tabletek 14, 28 (2 x 14), 84 (6 x 14) lub 10 x 14 (do użytku szpitalnego).
2 perforowane blistry po 10 tabletek (opakowanie do użytku szpitalnego).
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
06.6 Instrukcje użytkowania i obsługi
Brak specjalnych instrukcji dotyczących utylizacji.
Niewykorzystany lek i odpady pochodzące z tego leku należy usunąć zgodnie z lokalnymi przepisami.
07.0 PODMIOT POZWOLENIA NA DOPUSZCZENIE DO OBROTU
Warner Chilcott Włochy S.r.l.
Via dei Pratoni, 16
50018 Scandicci (FI) - Włochy
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
5 mg tabletki powlekane 14 tabletek w blistrze - AIC 034568016 / M
5 mg tabletki powlekane 20 (2 x 10) tabletek w blistrze - AIC 034568028 / M
5 mg tabletki powlekane 28 (2 x 14) tabletek w blistrze - AIC 034568030 / M
Tabletki powlekane 5 mg 84 (6 x 14) tabletek w blistrze - AIC. 034568042 / M
5 mg tabletki powlekane 140 (10 x 14) tabletek w blistrze - AIC 034568055 / M
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA
Data pierwszego zezwolenia: lipiec 2000
Data ostatniego przedłużenia: sierpień 2009
10.0 DATA ZMIAN TEKSTU
Marzec 2013