Składniki aktywne: Sofosbuwir
Sovaldi 400 mg tabletki powlekane
Dlaczego stosuje się Sovaldi? Po co to jest?
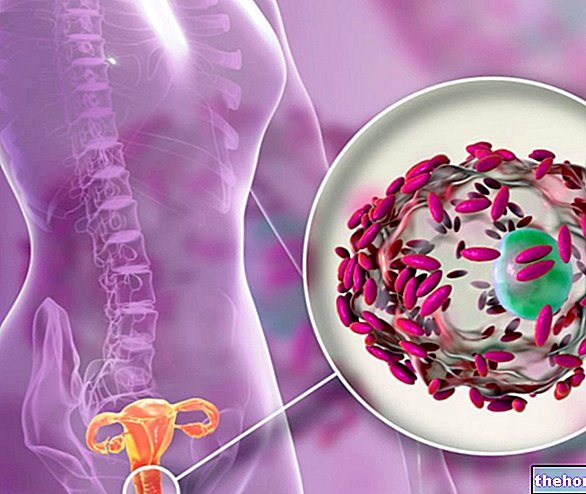
Sovaldi zawiera substancję czynną sofosbuwir, którą podaje się w leczeniu zakażenia wirusem zapalenia wątroby typu C u osób dorosłych w wieku 18 lat i starszych.
Wirusowe zapalenie wątroby typu C to infekcja wątroby wywołana przez wirusa. Ten lek działa poprzez zmniejszenie ilości wirusa zapalenia wątroby typu C w organizmie i usuwanie wirusa z krwi po określonym czasie.
Lek Sovaldi należy zawsze przyjmować z innymi lekami, ponieważ sam lek nie działa.
Zwykle przyjmuje się go z:
- rybawiryna lub
- peginterferon alfa i rybawiryna
Bardzo ważne jest również zapoznanie się z ulotkami dołączonymi do opakowań innych leków, które będą przyjmowane razem z lekiem Sovaldi.
W przypadku jakichkolwiek pytań dotyczących leków, należy zwrócić się do lekarza lub farmaceuty.
Przeciwwskazania Kiedy nie należy stosować leku Sovaldi
Nie należy przyjmować leku Sovaldi
- jeśli pacjent ma uczulenie na sofosbuwir lub którykolwiek z pozostałych składników tego leku
- Jeśli dotyczy to Ciebie, natychmiast poinformuj o tym lekarza.
Środki ostrożności dotyczące stosowania Informacje ważne przed przyjęciem leku Sovaldi
Sovaldi należy zawsze przyjmować z innymi lekami (patrz punkt 1 powyżej). Przed zastosowaniem tego leku należy porozmawiać z lekarzem lub farmaceutą, jeśli:
- masz problemy z wątrobą inne niż zapalenie wątroby typu C, na przykład jeśli oczekujesz na przeszczep wątroby
- masz zapalenie wątroby typu B, ponieważ lekarz może chcieć cię dokładniej monitorować
- mają problemy z nerkami. Należy porozmawiać z lekarzem lub farmaceutą, jeśli pacjent ma ciężką chorobę nerek lub jeśli pacjent jest poddawany dializie nerek, ponieważ działanie leku Sovaldi u pacjentów z ciężkimi zaburzeniami czynności nerek nie zostało w pełni zbadane.
Analiza krwi
Lekarz przeprowadzi określone badania krwi przed, w trakcie i po leczeniu lekiem Sovaldi. W ten sposób lekarz może:
- zdecydować, jakie inne leki należy przyjmować z lekiem Sovaldi i jak długo;
- potwierdź, że leczenie było skuteczne i nie masz już wirusa zapalenia wątroby typu C.
Dzieci i młodzież
Nie należy podawać tego leku dzieciom i młodzieży w wieku poniżej 18 lat. Stosowanie leku Sovaldi u dzieci i młodzieży nie zostało jeszcze zbadane.
Interakcje Jakie leki lub pokarmy mogą modyfikować efekt Sovaldiego
Należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent przyjmuje, ostatnio przyjmował lub może przyjmować inne leki, w tym leki ziołowe i leki wydawane bez recepty.
W szczególności nie należy przyjmować leku Sovaldi, jeśli pacjent przyjmuje którykolwiek z następujących leków:
- ryfampicyna (antybiotyk stosowany w leczeniu infekcji, takich jak gruźlica);
- ziele dziurawca (Hypericum perforatum, lek ziołowy stosowany w leczeniu depresji);
- karbamazepina i fenytoina (leki stosowane w leczeniu padaczki i zapobieganiu drgawkom), ponieważ leki te mogą zmniejszać skuteczność leku Sovaldi.
W przypadku dalszych pytań należy zwrócić się do lekarza lub farmaceuty.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
Ciąża i antykoncepcja
Należy unikać ciąży ze względu na stosowanie leku Sovaldi razem z rybawiryną Rybawiryna może być bardzo szkodliwa dla nienarodzonego dziecka W przypadku jakiejkolwiek możliwości zajścia w ciążę należy zachować szczególną ostrożność podczas stosunku płciowego.
- Sovaldi jest zwykle stosowany z rybawiryną. Rybawiryna może zaszkodzić nienarodzonemu dziecku. Dlatego bardzo ważne jest, abyś (lub Twój partner) unikała zajścia w ciążę podczas leczenia.
- Ty lub Twój partner musicie stosować skuteczną antykoncepcję w trakcie i po leczeniu. Bardzo ważne jest, aby uważnie przeczytać punkt „Ciąża” w ulotce dołączonej do opakowania rybawiryny. Zapytaj swojego lekarza, jaka skuteczna metoda antykoncepcji jest dla Ciebie odpowiednia.
- Jeśli pacjentka lub jej partnerka zajdą w ciążę podczas leczenia lekiem Sovaldi lub w ciągu następnych miesięcy, należy natychmiast skontaktować się z lekarzem.
Czas karmienia
Nie należy karmić piersią podczas leczenia lekiem Sovaldi. Nie wiadomo, czy sofosbuwir, substancja czynna leku Sovaldi, przenika do mleka matki.
Prowadzenie i używanie maszyn
Podczas przyjmowania leku Sovaldi razem z innymi lekami stosowanymi w leczeniu zakażenia wirusem zapalenia wątroby typu C pacjenci odczuwali zmęczenie, zawroty głowy, niewyraźne widzenie i zmniejszoną uwagę. W przypadku wystąpienia któregokolwiek z tych działań niepożądanych nie należy prowadzić pojazdów ani obsługiwać żadnych narzędzi ani maszyn.
Dawka, sposób i czas podawania Jak stosować lek Sovaldi: dawkowanie
Ten lek należy zawsze stosować zgodnie z zaleceniami lekarza. W razie wątpliwości skonsultuj się z lekarzem lub farmaceutą.
Zalecana dawka
Zalecana dawka to jedna tabletka raz dziennie, z jedzeniem. Lekarz poinformuje pacjenta, jak długo należy przyjmować lek Sovaldi.
Tabletkę należy połknąć w całości, bez żucia, łamania lub miażdżenia, ponieważ ma bardzo gorzki smak. Należy powiedzieć lekarzowi lub farmaceucie w przypadku trudności z połykaniem tabletek.
Sovaldi należy zawsze przyjmować razem z innymi lekami stosowanymi w leczeniu wirusowego zapalenia wątroby typu C.
Jeśli w ciągu 2 godzin od przyjęcia leku Sovaldi wystąpią wymioty, należy przyjąć kolejną tabletkę. W przypadku wymiotów po 2 godzinach przyjmowania, nie należy przyjmować kolejnej tabletki do następnej dawki o wyznaczonej porze.
Przedawkowanie Co zrobić w przypadku przyjęcia zbyt dużej dawki leku Sovaldi
Przyjęcie większej niż zalecana dawki leku Sovaldi
Jeśli przypadkowo przyjmiesz większą dawkę niż zalecana, natychmiast skonsultuj się z lekarzem lub najbliższym oddziałem ratunkowym. Zabierz ze sobą butelkę z tabletkami, aby łatwo wyjaśnić, co zażyłeś.
Pominięcie przyjęcia leku Sovaldi
Ważne jest, aby nie zapomnieć o żadnej dawce tego leku.
W przypadku pominięcia dawki:
- a jeśli zauważysz to w ciągu 18 godzin od zwykłej pory przyjmowania leku Sovaldi, należy jak najszybciej przyjąć tabletkę. Następnie przyjąć następną dawkę o zwykłej porze.
- a jeśli pacjent zauważy 18 lub więcej godzin po zwykłej porze przyjmowania leku Sovaldi, należy odczekać i przyjąć następną dawkę o zwykłej porze.Nie należy stosować dawki podwójnej (dwóch dawek znajdujących się blisko siebie).
Nie należy przerywać przyjmowania leku Sovaldi
Nie należy przerywać przyjmowania tego leku, chyba że tak zaleci lekarz. Bardzo ważne jest ukończenie całego leczenia, aby leki miały szansę zwalczyć zakażenie wirusem zapalenia wątroby typu C.
W przypadku dalszych pytań dotyczących stosowania tego leku należy zwrócić się do lekarza lub farmaceuty.
Skutki uboczne Jakie są skutki uboczne Sovaldi
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią. Podczas przyjmowania leku Sovaldi z rybawiryną lub peginterferonem alfa i rybawiryną może wystąpić jedno lub więcej z następujących działań niepożądanych:
Bardzo częste działania niepożądane
(może dotyczyć więcej niż 1 na 10 osób)
- gorączka, dreszcze, objawy grypopodobne
- biegunka, nudności, wymioty
- trudności w zasypianiu (bezsenność)
- uczucie zmęczenia i zirytowania
- bół głowy
- wysypka, swędzenie
- utrata apetytu
- zawroty głowy
- bóle mięśni, bóle stawów
- duszność, kaszel Badania krwi mogą wykazać:
- mała liczba czerwonych krwinek (niedokrwistość); objawy mogą obejmować uczucie zmęczenia, ból głowy, duszność podczas wysiłku fizycznego
- mała liczba białych krwinek (neutropenia); Objawy mogą obejmować więcej infekcji z gorączką i dreszczami lub bólem gardła lub owrzodzeniem jamy ustnej
- niska liczba płytek krwi
- zmiany w wątrobie (objawiające się zwiększeniem ilości substancji zwanej bilirubiną we krwi)
Częste skutki uboczne
(może dotyczyć do 1 na 10 osób)
- zmiany nastroju, obniżony nastrój, uczucie niepokoju i pobudzenia
- rozmazany obraz
- silny ból głowy (migrena), utrata pamięci, utrata koncentracji
- utrata wagi
- duszność podczas wysiłku fizycznego
- ból brzucha, zaparcia, suchość w ustach, niestrawność, refluks żołądkowy
- wypadanie i przerzedzanie włosów
- sucha skóra
- ból pleców, skurcze mięśni
- ból w klatce piersiowej, uczucie osłabienia
- przeziębienie (zapalenie nosogardzieli)
- Jeśli którykolwiek z działań niepożądanych stanie się poważny, należy poinformować o tym lekarza.
Zgłaszanie skutków ubocznych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe działania niepożądane niewymienione w tej ulotce, należy porozmawiać z lekarzem lub farmaceutą. Działania niepożądane można również zgłaszać bezpośrednio za pośrednictwem krajowego systemu zgłaszania wymienionego w załączniku V. Zgłaszanie działań niepożądanych może pomóc w uzyskaniu większej ilości informacji na temat bezpieczeństwa tego leku.
Wygaśnięcie i przechowywanie
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na butelce i pudełku po {EXP}. Termin ważności odnosi się do ostatniego dnia tego miesiąca.
Ten lek nie wymaga żadnych specjalnych warunków przechowywania.
Nie należy wyrzucać żadnych leków do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa.Pomoże to chronić środowisko.
Co zawiera lek Sovaldi
- Substancją czynną jest sofosbuwir. Każda tabletka powlekana zawiera 400 mg sofosbuwiru.
- Pozostałe składniki to
- Rdzeń tabletu: mannitol, celuloza mikrokrystaliczna, kroskarmeloza sodowa, krzemionka koloidalna bezwodna, magnezu stearynian.
- Folia powlekająca: alkohol poliwinylowy, dwutlenek tytanu, makrogol 3350, talk, żółty tlenek żelaza.
Opis wyglądu produktu Sovaldi i zawartości opakowania
Tabletki powlekane to żółte tabletki w kształcie kapsułki z wytłoczonym napisem „GSI” po jednej stronie i „7977” po drugiej stronie.
Każda butelka zawiera środek suszący z żelem krzemionkowym, który musi pozostać w butelce, aby chronić tabletki.Środek suszący z żelem krzemionkowym znajduje się w osobnej saszetce lub pojemniku i nie należy go połykać.
Dostępne są następujące wielkości opakowań: pudełka tekturowe zawierające 1 butelkę po 28 tabletek powlekanych i 84 (3 butelki po 28) tabletek powlekanych. Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO
SOVALDI 400 MG TABLETKI POWLEKANE FOLIĄ
▼ Produkt leczniczy podlegający dodatkowemu monitorowaniu. Umożliwi to szybką identyfikację nowych informacji dotyczących bezpieczeństwa. Osoby należące do fachowego personelu medycznego proszone są o zgłaszanie wszelkich podejrzewanych działań niepożądanych. Patrz punkt 4.8, aby uzyskać informacje na temat zgłaszania działań niepożądanych.
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY
Każda tabletka powlekana zawiera 400 mg sofosbuwiru.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
03.0 POSTAĆ FARMACEUTYCZNA
Tabletka powlekana.
Żółta tabletka powlekana w kształcie kapsułki, o wymiarach 20 mm x 9 mm, z wytłoczonym napisem „GSI” po jednej stronie i „7977” po drugiej stronie.
04.0 INFORMACJE KLINICZNE
04.1 Wskazania terapeutyczne
Sovaldi jest wskazany w skojarzeniu z innymi lekami w leczeniu przewlekłego wirusowego zapalenia wątroby typu C (przewlekłe zapalenie wątroby typu C, CHC) u dorosłych (patrz punkty 4.2, 4.4 i 5.1).
Specyficzna aktywność wobec genotypu wirusa zapalenia wątroby typu C (HCV), patrz punkty 4.4 i 5.1.
04.2 Dawkowanie i sposób podawania
Leczenie produktem Sovaldi powinien rozpoczynać i monitorować lekarz mający doświadczenie w leczeniu pacjentów z CHC.
Dawkowanie
Zalecana dawka to jedna tabletka 400 mg doustnie raz na dobę, przyjmowana z posiłkiem (patrz punkt 5.2).
Sovaldi należy stosować w skojarzeniu z innymi lekami. Nie zaleca się monoterapii produktem Sovaldi (patrz punkt 5.1). Należy również zapoznać się z Charakterystyką Produktu Leczniczego produktów leczniczych stosowanych w skojarzeniu z produktem Sovaldi. Zalecany(e) produkt(y) leczniczy(e) do podawania razem z produktem Sovaldi oraz czas trwania leczenia w terapii skojarzonej przedstawiono w Tabeli 1.
Tabela 1: Zalecany(e) produkt(y) leczniczy(e) do podawania razem z produktem Sovaldi i czas trwania leczenia w terapii skojarzonej
* Obejmuje pacjentów jednocześnie zakażonych ludzkim wirusem niedoboru odporności (HIV).
a W przypadku wcześniej leczonych pacjentów zakażonych wirusem HCV genotypu 1 nie ma danych dotyczących skojarzenia produktu Sovaldi, rybawiryny i peginterferonu alfa (patrz punkt 4.4).
b Należy rozważyć wydłużenie czasu trwania terapii poza 12 tygodni i do 24 tygodni, zwłaszcza w podgrupach z jednym lub więcej czynnikami historycznie związanymi z niskimi wskaźnikami odpowiedzi na terapie oparte na interferonie (np. zaawansowane zwłóknienie / marskość wątroby, podwyższone podstawowe stężenie wirusa rasy czarnej, genotyp IL28B inny niż CC, wcześniejszy brak odpowiedzi na leczenie peginterferonem alfa i rybawiryną).
c Patrz Specjalne populacje pacjentów: Pacjenci oczekujący na przeszczepienie wątroby.
Dawkę rybawiryny stosowanej w skojarzeniu z lekiem Sovaldi ustala się na podstawie masy ciała (doustnie, podzieloną na dwie dawki, z jedzeniem.
W przypadku równoczesnego podawania z innymi lekami przeciwwirusowymi działającymi bezpośrednio na HCV, patrz punkt 4.4.
Modyfikacje dawki
Nie zaleca się zmniejszania dawki produktu Sovaldi.
Jeśli sofosbuwir jest stosowany w skojarzeniu z peginterferonem alfa i u pacjenta wystąpi poważne działanie niepożądane potencjalnie związane z tym lekiem, dawkę peginterferonu alfa należy zmniejszyć lub przerwać podawanie. Więcej informacji na temat zmniejszenia dawki i (lub) zaprzestania podawania peginterferonu alfa znajduje się w Charakterystyce Produktu Leczniczego peginterferonu alfa.
Jeśli u pacjenta wystąpi ciężkie działanie niepożądane potencjalnie związane z rybawiryną, należy zmienić dawkę rybawiryny lub przerwać podawanie, jeśli to konieczne, do czasu ustąpienia działania niepożądanego lub jego łagodniejszego przebiegu. Tabela 2 zawiera porady dotyczące modyfikacji dawki i przerwania dawkowania w oparciu o stężenie hemoglobiny u pacjenta i czynność serca.
Tabela 2: Porady dotyczące modyfikacji dawki rybawiryny podawanej w skojarzeniu z produktem Sovaldi
Po odstawieniu rybawiryny z powodu nieprawidłowych wyników badań laboratoryjnych lub objawów klinicznych można podjąć próbę wznowienia dawki rybawiryny w dawce 600 mg na dobę, a następnie zwiększenia jej do 800 mg na dobę. Jednak zaleca się zwiększenie dawki rybawiryny do jego pierwotna wartość (1000 mg-1200 mg dziennie).
Zaprzestanie podawania
W przypadku całkowitego przerwania leczenia innymi produktami leczniczymi stosowanymi w skojarzeniu z produktem Sovaldi należy również przerwać podawanie produktu Sovaldi (patrz punkt 4.4).
Specjalne populacje pacjentów
Starsi mieszkańcy
Dostosowanie dawki u pacjentów w podeszłym wieku nie jest uzasadnione (patrz punkt 5.2).
Zaburzenia czynności nerek
Nie ma konieczności dostosowania dawki produktu Sovaldi u pacjentów z łagodnymi lub umiarkowanymi zaburzeniami czynności nerek. Nie ustalono bezpieczeństwa i odpowiedniej dawki produktu Sovaldi u pacjentów z ciężkimi zaburzeniami czynności nerek (szacowany współczynnik przesączania kłębuszkowego [szacowany współczynnik filtracji kłębuszkowej, eGFR] 2) lub schyłkowa niewydolność nerek (schyłkową niewydolnością nerek, ESRD) wymagających hemodializy (patrz punkt 5.2).
Zaburzenia czynności wątroby
U pacjentów z łagodnymi, umiarkowanymi lub ciężkimi zaburzeniami czynności wątroby (klasa A, B lub C w skali Child-Pugh-Turcotte [CPT]) nie jest konieczne dostosowanie dawki produktu Sovaldi (patrz punkt 5.2). Nie ustalono bezpieczeństwa i skuteczności produktu Sovaldi u pacjentów ze zdekompensowaną marskością wątroby.
Pacjenci oczekujący na przeszczep wątroby
Czas trwania podawania produktu Sovaldi pacjentom oczekującym na przeszczepienie wątroby należy określić na podstawie oceny potencjalnych korzyści i zagrożeń dla danego pacjenta (patrz punkt 5.1).
biorcy przeszczepu wątroby
Sovaldi w skojarzeniu z rybawiryną jest zalecany przez 24 tygodnie u biorców przeszczepu wątroby. Zalecana dawka początkowa rybawiryny 400 mg podawana doustnie, podzielona na dwie dawki, z posiłkiem. Jeśli początkowa dawka rybawiryny jest dobrze tolerowana, dawkę można stopniowo zwiększać do maksymalnie 1000-1200 mg na dobę (1000 mg dla pacjentów o masie ciała mniejszej niż 75 kg i 1200 mg dla pacjentów o masie ciała mniejszej niż 75 kg i 1200 mg dla pacjentów o masie ciała mniejszej niż 75 kg). pacjentów o masie ciała poniżej 75 kg) do 75 kg). Jeśli początkowa dawka rybawiryny nie jest dobrze tolerowana, dawkę należy zmniejszyć zgodnie ze wskazaniami klinicznymi na podstawie stężenia hemoglobiny (patrz punkt 5.1).
Populacja pediatryczna
Bezpieczeństwo i skuteczność produktu Sovaldi u dzieci i młodzieży w wieku poniżej 18 lat nie zostały jeszcze ustalone.Brak dostępnych danych.
Sposób podawania
Tabletka powlekana przeznaczona jest do stosowania doustnego. Pacjentów należy poinstruować, aby połykali tabletkę w całości. Tabletki powlekanej nie należy żuć ani kruszyć, ponieważ substancja czynna ma gorzki smak. Tabletkę należy przyjmować z jedzeniem (patrz punkt 5.2).
Należy pouczyć pacjentów, że jeśli zwymiotują w ciągu 2 godzin od przyjęcia nowej tabletki, jeśli wymiotują po upływie 2 godzin od przyjęcia nowej tabletki, nie jest wymagana dodatkowa dawka. Zalecenia te opierają się na kinetyce wchłaniania sofosbuwiru i GS-331007, co sugeruje, że większość dawki jest wchłaniana w ciągu 2 godzin od podania.
Jeśli pominięto dawkę i nastąpi to w ciągu 18 godzin od normalnego czasu przyjęcia, pacjentom należy zalecić jak najszybsze przyjęcie tabletki; następną dawkę należy przyjąć o zwykłej porze.Jeśli to nastąpi po ponad 18 godzinach, należy zalecić pacjentom odczekanie i przyjęcie następnej dawki o zwykłej porze. Pacjentom należy zalecić, aby nie przyjmowali podwójnej dawki.
04.3 Przeciwwskazania
Nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1.
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania
Ogólne ostrzeżenia
Produkt Sovaldi nie jest wskazany w monoterapii i powinien być przepisywany w skojarzeniu z innymi produktami leczniczymi do leczenia zakażenia wirusem zapalenia wątroby typu C. Jeśli leczenie innymi produktami leczniczymi stosowanymi w skojarzeniu z produktem Sovaldi zostanie całkowicie przerwane, należy również przerwać podawanie produktu Sovaldi (patrz pkt 4.2). Przed rozpoczęciem leczenia produktem Sovaldi należy zapoznać się z Charakterystyką Produktu Leczniczego wspólnie przepisanych produktów leczniczych.
Ciężka bradykardia i blok serca
Przypadki ciężkiej bradykardii i bloku serca obserwowano, gdy produkt Sovaldi był stosowany w skojarzeniu z produktem Daklinza i amiodaronem, z innymi lekami zmniejszającymi częstość akcji serca lub bez nich. Mechanizm nie został ustanowiony.
Jednoczesne stosowanie amiodaronu zostało ograniczone przez kliniczny rozwój sofosbuwiru z lekami przeciwwirusowymi o działaniu bezpośrednim (DAA).Przypadki mogą być śmiertelne, dlatego amiodaron należy stosować tylko u pacjentów leczonych produktem Sovaldi + Daklinza, gdy alternatywne terapie przeciwarytmiczne nie są dostępne.tolerowane lub przeciwwskazane .
Jeśli jednoczesne stosowanie amiodaronu zostanie uznane za konieczne, zaleca się uważną obserwację pacjentów po rozpoczęciu leczenia produktem Sovaldi + Daklinza. Pacjenci, u których stwierdzono duże ryzyko bradyarytmii, powinni być stale monitorowani przez 48 godzin w odpowiednich warunkach klinicznych.
Ze względu na długi okres półtrwania amiodaronu należy przewidzieć odpowiednie monitorowanie pacjentów, którzy przerwali leczenie amiodaronem w ciągu ostatnich kilku miesięcy i którzy powinni rozpocząć leczenie produktem Sovaldi w skojarzeniu z produktem Daklinza.
Wszystkich pacjentów leczonych produktem Sovaldi + Daklinza w skojarzeniu z amiodaronem, z innymi lekami zmniejszającymi częstość akcji serca lub bez nich, należy również ostrzec o objawach bradykardii i bloku serca oraz zalecić pilną pomoc lekarską, jeśli się pojawią.
Wcześniej leczeni pacjenci z zakażeniem HCV genotypu 1, 4, 5 i 6
Sovaldi nie był badany w badaniu III fazy z udziałem wcześniej leczonych pacjentów z zakażeniem HCV genotypu 1, 4, 5 i 6. W związku z tym nie ustalono optymalnego czasu trwania leczenia w tej populacji (patrz również punkty 4.2 i 5.1).
Należy rozważyć leczenie tych pacjentów i wydłużenie czasu leczenia sofosbuwirem, peginterferonem alfa i rybawiryną poza 12 tygodni i do 24 tygodni, zwłaszcza w podgrupach z jednym lub większą liczbą czynników historycznie związanych z niskimi wskaźnikami odpowiedzi na terapie oparte na interferonie (zaawansowane zwłóknienie / marskość wątroby, podwyższone podstawowe stężenie wirusa, pochodzenie etniczne rasy czarnej, genotyp inny niż CC IL28B).
Leczenie pacjentów z zakażeniem HCV genotypu 5 lub 6
Dane kliniczne uzasadniające stosowanie produktu Sovaldi u pacjentów z zakażeniem HCV genotypu 5 i 6 są bardzo ograniczone (patrz punkt 5.1).
Terapia bezinterferonowa w przypadku zakażenia HCV genotypu 1, 4, 5 i 6
W badaniach III fazy nie oceniano schematów leczenia produktem Sovaldi niezawierających interferonu u pacjentów zakażonych HCV o genotypie 1, 4, 5 i 6 (patrz punkt 5.1). Nie ustalono optymalnego schematu i czasu trwania leczenia. Schematy te należy stosować wyłącznie u pacjentów, którzy nie tolerują lub nie kwalifikują się do leczenia interferonem i którzy wymagają pilnego leczenia.
Podawanie w skojarzeniu z innymi lekami przeciwwirusowymi o bezpośrednim działaniu przeciwko HCV
Sovaldi należy podawać w skojarzeniu z innymi przeciwwirusowymi produktami leczniczymi o działaniu bezpośrednim tylko wtedy, gdy na podstawie dostępnych danych uzna się, że korzyści przewyższają ryzyko. Brak danych uzasadniających podawanie produktu Sovaldi w skojarzeniu z telaprewirem lub boceprewirem. Takie równoczesne podawanie nie jest zalecane (patrz również punkt 4.5).
Ciąża i jednoczesne stosowanie rybawiryny
Gdy produkt Sovaldi jest stosowany w skojarzeniu z rybawiryną lub peginterferonem alfa/rybawiryną, kobiety w wieku rozrodczym lub ich partnerzy powinni stosować skuteczną antykoncepcję podczas leczenia i przez okres po leczeniu zalecany w Charakterystyce Produktu Leczniczego rybawiryny. Więcej informacji znajduje się w Charakterystyce Produktu Leczniczego rybawiryny.
Używaj z potężnymi cewkami indukcyjnymi P-gp
Leki, które są silnymi induktorami glikoproteiny P (P-gp) w jelicie (np. ryfampicyna, ziele dziurawca [Hypericum perforatum], karbamazepina i fenytoina) mogą znacząco zmniejszać stężenie sofosbuwiru w osoczu, co skutkuje osłabieniem działania terapeutycznego produktu Sovaldi. Tych produktów leczniczych nie wolno stosować z produktem Sovaldi (patrz punkt 4.5).
Zaburzenia czynności nerek
Nie ustalono bezpieczeństwa stosowania produktu Sovaldi u osób z ciężkimi zaburzeniami czynności nerek (eGFR 2) lub ESRD wymagających hemodializy. Nie ustalono również odpowiedniej dawki. Jeśli produkt Sovaldi jest stosowany w skojarzeniu z rybawiryną lub peginterferonem alfa/rybawiryną, należy zapoznać się również z Charakterystyka Produktu Leczniczego rybawiryny dla pacjentów z klirensem kreatyniny (CrCl)
Współzakażenie HCV/HBV (wirusem zapalenia wątroby typu B)
Brak danych dotyczących stosowania produktu Sovaldi u pacjentów ze współistniejącym zakażeniem HCV/HBV.
Populacja pediatryczna
Sovaldi nie jest zalecany do stosowania u dzieci i młodzieży w wieku poniżej 18 lat, ponieważ nie ustalono bezpieczeństwa i skuteczności w tej populacji.
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji
Sofosbuvir jest prolekiem nukleotydowym. Po podaniu doustnym produktu Sovaldi sofosbuwir jest szybko wchłaniany i podlega intensywnemu metabolizmowi pierwszego przejścia w wątrobie oraz intensywnemu metabolizmowi jelitowemu. Wewnątrzkomórkowe hydrolityczne rozszczepienie proleku katalizowane przez enzymy takie jak karboksyloesteraza 1 oraz kolejne etapy fosforylacji katalizowane przez kinazy nukleotydowe prowadzą do powstania trifosforanowego analogu nukleozydu urydyny, który jest farmakologicznie czynny.Główny krążący nieaktywny metabolit GS- 331007, odpowiedzialny za ponad 90% ogólnoustrojowej ekspozycji na lek, powstaje poprzez sekwencyjne i równoległe drogi powstawania aktywnego metabolitu. Cząsteczka macierzysta, sofosbuwir, odpowiada za około 4% ogólnoustrojowej ekspozycji na lek (patrz punkt 5.2).W badaniach farmakologii klinicznej zarówno sofosbuwir, jak i GS-331007 monitorowano pod kątem analizy farmakokinetycznej.
Sofosbuwir jest substratem transportera leków P-gp i białka oporności raka piersi (białko oporności na raka piersiBCRP), w przeciwieństwie do GS-331007. Produkty lecznicze, które są silnymi induktorami P-gp w jelicie (np. ryfampicyna, ziele dziurawca, karbamazepina i fenytoina) mogą zmniejszać stężenie sofosbuwiru w osoczu, powodując osłabienie działania terapeutycznego produktu Sovaldi, dlatego nie należy ich stosować z Sovaldi ( patrz punkt 4.4) Podawanie produktu Sovaldi w skojarzeniu z produktami leczniczymi hamującymi P-gp i (lub) BCRP może zwiększać stężenie sofosbuwiru w osoczu bez zwiększania stężenia GS-331007, dlatego produkt Sovaldi można podawać w skojarzeniu z inhibitorami P-gp i (lub) BCRP Sofosbuvir i GS-331007 nie są inhibitorami P-gp i BCRP i dlatego nie oczekuje się zwiększenia ekspozycji na leki będące substratami tych transporterów.
Wewnątrzkomórkowa aktywacja metaboliczna sofosbuwiru odbywa się za pośrednictwem szlaków hydrolazy i fosforylacji nukleotydów, które na ogół mają niskie powinowactwo i dużą pojemność, na które wpływ jednocześnie stosowanych produktów leczniczych jest mało prawdopodobny (patrz punkt 5.2).
Inne interakcje
Interakcje leku Sovaldi z produktami leczniczymi, które mogą być podawane jednocześnie, podsumowano w Tabeli 3 (gdzie przedział ufności (przedział ufności, CI) przy 90% stosunku średniej geometrycznej najmniejszych kwadratów (geometryczna średnia najmniejszych kwadratów, GLSM) pozostał w granicach „↔” lub był powyżej „↑” lub poniżej „↓” ustalonych granic równoważności). Tabela nie jest wyczerpująca.
Tabela 3: Interakcje między produktem Sovaldi a innymi produktami leczniczymi
NA = niedostępne / nieistotne
a Średni stosunek (90% CI) farmakokinetyki leku podawanego z/bez sofosbuwiru oraz średni stosunek sofosbuwiru do GS-331007 z/bez równoczesnego podawania leku. Brak efektu = 1,00
b Wszystkie badania interakcji przeprowadzono na zdrowych ochotnikach
c Porównanie oparte na kontroli historycznej
d Podawany jako Atripla
e Granica biorównoważności 80% -125%
f Granica równoważności 70% -143%
Produkty lecznicze, które są silnymi induktorami P-gp w jelicie (ryfampicyna, ziele dziurawca, karbamazepina i fenytoina) mogą znacząco zmniejszać stężenie sofosbuwiru w osoczu, co skutkuje zmniejszeniem efektu terapeutycznego. podawany ze znanymi induktorami P-gp.
04.6 Ciąża i laktacja
Kobiety w wieku rozrodczym / antykoncepcja u mężczyzn i kobiet
W przypadku stosowania produktu Sovaldi w skojarzeniu z rybawiryną lub peginterferonem alfa/rybawiryną należy zachować szczególną ostrożność, aby uniknąć ciąży u pacjentek i u partnerów pacjentów płci męskiej. U wszystkich gatunków zwierząt narażonych na rybawirynę wykazano istotne działanie teratogenne i (lub) embriobójcze (patrz punkt 4.4). Kobiety w wieku rozrodczym lub ich partnerzy powinni stosować skuteczną antykoncepcję w trakcie leczenia i po jego zakończeniu, zgodnie z zaleceniami zawartymi w Charakterystyce Produktu Leczniczego rybawiryny. Więcej informacji znajduje się w Charakterystyce Produktu Leczniczego rybawiryny.
Ciąża
Dane dotyczące stosowania sofosbuwiru u kobiet w ciąży nie istnieją lub są ograniczone (mniej niż 300 narażonych ciąż).
Badania na zwierzętach nie wykazują bezpośredniego ani pośredniego szkodliwego wpływu na reprodukcję. Nie zaobserwowano wpływu na rozwój płodu u szczurów i królików po podaniu największych badanych dawek. Jednak nie było możliwe dokładne oszacowanie marginesów narażenia uzyskanych dla sofosbuwiru u szczurów w stosunku do narażenia u ludzi w zalecanej dawce klinicznej (patrz punkt 5.3).
Jako środek ostrożności zaleca się unikanie stosowania produktu Sovaldi w czasie ciąży.
Jednak w przypadku stosowania rybawiryny w skojarzeniu z sofosbuwirem obowiązują przeciwwskazania związane ze stosowaniem rybawiryny w czasie ciąży (patrz również Charakterystyka Produktu Leczniczego rybawiryny).
Czas karmienia
Nie wiadomo, czy sofosbuwir i jego metabolity przenikają do mleka ludzkiego.
Dostępne dane farmakokinetyczne na zwierzętach wykazały przenikanie metabolitów do mleka (szczegóły patrz punkt 5.3).
Nie można wykluczyć zagrożenia dla noworodków/niemowląt. Dlatego Sovaldi nie powinien być stosowany podczas karmienia piersią.
Płodność
Brak danych dotyczących wpływu produktu Sovaldi na płodność u ludzi Badania na zwierzętach nie wykazują szkodliwego wpływu na płodność.
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Sovaldi umiarkowanie wpływa na zdolność prowadzenia pojazdów i obsługiwania maszyn. Należy poinformować pacjentów, że podczas leczenia sofosbuwirem w skojarzeniu z peginterferonem alfa i rybawiryną zgłaszano zmęczenie, zaburzenia uwagi, zawroty głowy i niewyraźne widzenie (patrz punkt 4.8).
04.8 Działania niepożądane
Podsumowanie profilu bezpieczeństwa
Podczas leczenia sofosbuwirem w skojarzeniu z rybawiryną lub z peginterferonem alfa i rybawiryną najczęściej zgłaszane działania niepożądane leku były zgodne z oczekiwanym profilem bezpieczeństwa leczenia rybawiryną i peginterferonem alfa, bez zwiększenia częstości lub nasilenia działań niepożądanych działań leku .
Ocena działań niepożądanych opiera się na zbiorczych danych z pięciu badań klinicznych III fazy (zarówno kontrolowanych, jak i niekontrolowanych).
Odsetek pacjentów, którzy ostatecznie przerwali leczenie z powodu działań niepożądanych, wynosił 1,4% dla pacjentów, którzy otrzymywali placebo, 0,5% dla pacjentów, którzy otrzymywali sofosbuwir + rybawirynę przez 12 tygodni, 0% dla pacjentów, którzy otrzymywali sofosbuwir + rybawirynę przez 16 tygodni, 11,1% u pacjentów otrzymujących peginterferon alfa + rybawirynę przez 24 tygodnie i 2,4% u pacjentów otrzymujących sofosbuwir + peginterferon alfa + rybawirynę przez 12 tygodni .
Tabela działań niepożądanych
Produkt Sovaldi badano głównie w skojarzeniu z rybawiryną, z peginterferonem alfa lub bez peginterferonu alfa. W tym kontekście nie stwierdzono żadnych specyficznych działań niepożądanych sofosbuwiru. Najczęściej zgłaszanymi działaniami niepożądanymi leku u osób otrzymujących sofosbuwir i rybawirynę lub sofosbuwir, rybawirynę i peginterferon alfa są zmęczenie, ból głowy, nudności i bezsenność.
Następujące działania niepożądane zgłaszano podczas stosowania sofosbuwiru w skojarzeniu z rybawiryną lub w skojarzeniu z peginterferonem alfa i rybawiryną (Tabela 4). Działania niepożądane są wymienione poniżej według układów narządowych i częstości. Częstotliwości zdefiniowano w następujący sposób: bardzo często (≥1 / 10), często (≥1/100,
Tabela 4: Działania niepożądane obserwowane w przypadku sofosbuwiru w skojarzeniu z rybawiryną lub peginterferonem alfa i rybawiryną.
a SOF = sofosbuwir;
b RBV = rybawiryna;
c PEG = peginterferon alfa
Inne szczególne populacje
koinfekcja HIV/HCV
Profil bezpieczeństwa sofosbuwiru i rybawiryny u osób zakażonych jednocześnie HCV i HIV był podobny do obserwowanego u osób zakażonych HCV jednorazowo leczonych sofosbuwirem i rybawiryną w badaniach klinicznych III fazy (patrz punkt 5.1).
Pacjenci oczekujący na przeszczep wątroby
Profil bezpieczeństwa sofosbuwiru i rybawiryny u osób zakażonych HCV przed przeszczepieniem wątroby był podobny do obserwowanego u osób leczonych sofosbuwirem i rybawiryną w badaniach klinicznych III fazy (patrz punkt 5.1).
biorcy przeszczepu wątroby
Profil bezpieczeństwa sofosbuwiru i rybawiryny u biorców przeszczepu wątroby z przewlekłym wirusowym zapaleniem wątroby typu C był podobny do obserwowanego u osób leczonych sofosbuwirem i rybawiryną w badaniach klinicznych III fazy (patrz punkt 5.1). W badaniu 0126 zmniejszenie stężenia hemoglobiny podczas leczenia było bardzo częste, przy czym 32,5% pacjentów (13/40) miało zmniejszenie stężenia hemoglobiny do epoetyny i (lub) produktu krwiopochodnego. U 5 badanych (12,5%) badane leki zostały wstrzymane, zmienione lub odstawione z powodu działań niepożądanych.
Opis wybranych działań niepożądanych
Zaburzenia rytmu serca
Przypadki ciężkiej bradykardii i bloku serca obserwowano, gdy produkt Sovaldi był stosowany w skojarzeniu z produktem Daklinza i jednocześnie z amiodaronem i (lub) innymi lekami zmniejszającymi częstość akcji serca (patrz punkty 4.4 i 4.5).
Zgłaszanie podejrzewanych działań niepożądanych
Zgłaszanie podejrzewanych działań niepożądanych występujących po dopuszczeniu produktu leczniczego do obrotu jest ważne, ponieważ umożliwia ciągłe monitorowanie stosunku korzyści do ryzyka produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem krajowego systemu zgłaszania:
Włoska Agencja Leków strona internetowa: https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse
04.9 Przedawkowanie
Największą udokumentowaną dawką sofosbuwiru była pojedyncza dawka supraterapeutyczna 1200 mg podana 59 zdrowym osobom. W badaniu tym nie zaobserwowano działań niepożądanych przy tym poziomie dawki, a częstość i nasilenie działań niepożądanych były podobne do tych zgłaszanych w grupach otrzymujących placebo i sofosbuwir 400 mg. Skutki wyższych dawek nie są znane.
Nie ma swoistego antidotum na przedawkowanie produktu Sovaldi. W przypadku przedawkowania pacjenta należy monitorować pod kątem objawów toksyczności. Leczenie przedawkowania produktu Sovaldi obejmuje ogólne środki wspomagające, w tym monitorowanie parametrów życiowych i obserwację stanu klinicznego pacjenta.Główny krążący metabolit GS-331007 można z powodzeniem usunąć (53% wskaźnik ekstrakcji) za pomocą hemodializy. % podanej dawki.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE
05.1 Właściwości farmakodynamiczne
Grupa farmakoterapeutyczna: leki przeciwwirusowe działające bezpośrednio.
Kod ATC: J05AX15.
Mechanizm akcji
Sofosbuwir jest pangenotypowym inhibitorem polimerazy RNA zależnej od RNA HCV NS5B, która jest niezbędna do replikacji wirusa. Sofosbuwir jest prolekiem nukleotydowym podlegającym metabolizmowi wewnątrzkomórkowemu, dając początek farmakologicznie czynnemu trifosforanowi analogu urydyny (GS-461203), który może być włączony do RNA HCV przez polimerazę NS5B i działać jako terminator łańcucha. W teście biochemicznym GS-461203 hamował aktywność polimerazy rekombinowanego NS5B genotypów 1b, 2a, 3a i 4a HCV przy wartości stężenia hamującego 50% (stężenie hamujące, IC50) między 0,7 a 2,6 mcM. GS-461203 (aktywny metabolit sofosbuwiru) nie jest inhibitorem ludzkich polimeraz DNA i RNA ani inhibitorem mitochondrialnej polimerazy RNA.
Aktywność przeciwwirusowa
W testach przeprowadzonych z replikonami HCV wartości stężeń efektywnych (efektywna koncentracja, EC50) sofosbuwiru wobec całych replikonów genotypów 1a, 1b, 2a, 3a i 4a wynosiły odpowiednio 0,04, 0,11, 0,05, 0,05 i 0,04 mcM, a wartości EC50 sofosbuwiru wobec replikonów chimerycznych 1b kodujących genotypy 2b, 5a lub 6a NS5B od 0,014 do 0,015 mcM Średnia ± SD EC50 dla sofosbuwiru wobec replikonów chimerycznych kodujących sekwencje NS5B izolatów klinicznych wyniosła 0,068 ± 0,024 mcM dla genotypu 1a (n = 67), 0,11 ± 0,029 mcM dla genotypu 1b (n = 29), 0,035 ± 0,018 mcM dla genotypu 2 (n = 15) i 0,085 ± 0,034 mcM dla genotypu 3a (n = 106). in vitro sofosbuwiru przeciwko mniej powszechnym genotypom 4, 5 i 6 był podobny do obserwowanego dla genotypów 1, 2 i 3.
Obecność 40% surowicy ludzkiej nie miała wpływu na aktywność sofosbuwiru przeciw HCV.
Opór
W kulturach komórkowych
Replikony HCV o zmniejszonej wrażliwości na sofosbuwir wyselekcjonowano z hodowli komórkowych dla kilku genotypów, w tym 1b, 2a, 2b, 3a, 4a, 5a i 6a. Zmniejszona wrażliwość na sofosbuwir była związana z pierwotną substytucją S282T w NS5B we wszystkich testowanych genotypach replikonu.Swoista mutageneza substytucji S282T w replikonach 8 genotypów powodowała 2-18-krotne zmniejszenie wrażliwości na sofosbuwir i 2-18-krotne zmniejszenie wrażliwości na sofosbuwir sofosbuwir zmniejszał zdolność replikacji wirusa o 89-99% w porównaniu do typ dziki odpowiedni. W analizach biochemicznych rekombinowana polimeraza NS5B genotypów 1b, 2a, 3a i 4a z ekspresją podstawienia S282T wykazała zmniejszoną wrażliwość na GS-461203 w porównaniu z typ dziki korespondentów.
W badaniach klinicznych
W zbiorczej analizie 991 osób, które otrzymywały sofosbuwir w badaniach fazy 3, 226 osób kwalifikowało się do analizy oporności z powodu niepowodzenia wirusologicznego lub wczesnego przerwania leczenia badanego leku oraz ze względu na poziom HCV. Sekwencje NS5B były dostępne dla 225 z 226 osobników, a dla 221 z tych osobników uzyskano ogromne dane dotyczące sekwencjonowania (głębokie sekwencjonowanie) (wartość odcięcia testu wynosząca 1%). Podstawienie S282T związane z opornością na sofosbuwir nie zostało wykryte u żadnego z tych pacjentów za pomocą sekwencjonowania masowego lub sekwencjonowania populacyjnego. Podstawienie NS5B S282T wykryto tylko u jednego pacjenta otrzymującego produkt Sovaldi w monoterapii w badaniu fazy 2 U tego osobnika wyjściowo wykryto mniej niż 1% S282T HCV i 4 tygodnie po leczeniu doszło do zastąpienia S282T (> 99%), co skutkowało 13,5-krotną zmianą wartości EC50 sofosbuwiru i zmniejszeniem zdolności do replikacji wirusa. Zamiennik S282T powraca do typ dziki w ciągu następnych 8 tygodni i nie był już wykrywalny przez masowe sekwencjonowanie 12 tygodni po leczeniu.
W badaniach klinicznych III fazy w próbkach od wielu pacjentów zakażonych HCV genotypu 3 wykryto dwie substytucje NS5B, L159F i V321A, z nawrotami po leczeniu. Nie było zmian we wrażliwości fenotypowej na sofosbuwir lub rybawirynę izolatów z tymi podstawieniami. Substytucje S282R i L320F wykryto również podczas leczenia przez masowe sekwencjonowanie u biorcy przeszczepu z częściową odpowiedzią na leczenie. Kliniczne znaczenie tych wyników nie jest znane.
Wpływ początkowych polimorfizmów HCV na wynik leczenia
U 1292 pacjentów włączonych do badań fazy 3 sekwencje NS5B uzyskano w punkcie początkowym przez sekwencjonowanie populacyjne, a podstawienia S282T nie wykryto u żadnego osobnika w dostępnej sekwencji początkowej. W analizie mającej na celu określenie wpływu wyjściowych polimorfizmów na wynik leczenia nie zaobserwowano statystycznie istotnego związku między obecnością jakiegokolwiek wariantu HCV NS5B a wynikiem leczenia.
Opór krzyżowy
Replikony HCV z ekspresją podstawienia S282T związanego z opornością na sofosbuwir były w pełni wrażliwe na inne klasy leków przeciw HCV. Sofosbuwir pozostał aktywny wobec podstawień NS5B L159F i L320F związanych z opornością na inne inhibitory nukleozydowe. Sofosbuwir był w pełni aktywny wobec podstawień związanych z opornością na inne bezpośrednio działające leki przeciwwirusowe o różnych mechanizmach działania, takie jak nienukleozydowe inhibitory NS5B, inhibitory proteazy NS3 i inhibitory NS5A.
Skuteczność kliniczna i bezpieczeństwo
Skuteczność sofosbuwiru określono w pięciu badaniach fazy 3 z udziałem łącznie 1568 pacjentów z przewlekłym wirusowym zapaleniem wątroby typu C o genotypie 1 do 6. Przeprowadzono jedno badanie u nieleczonych wcześniej pacjentów z przewlekłym wirusowym zapaleniem wątroby typu C, 4, 5 lub 6 o genotypie 1 w peginterferon alfa 2a i rybawiryna, a pozostałe cztery badania przeprowadzono u pacjentów z przewlekłym wirusowym zapaleniem wątroby typu C genotypu 2 lub 3 w skojarzeniu z rybawiryną, w tym jedno z udziałem osób nieleczonych wcześniej, jedno z nietolerancją pacjentów, którzy nie kwalifikują się lub nie wyrażają zgody na leczenie interferonem, jeden z pacjentów wcześniej leczonych w schemacie opartym na interferonie i jeden na wszystkich pacjentów, niezależnie od ich wcześniejszego leczenia lub ich zdolności do otrzymywania leczenia opartego na interferonie Pacjenci objęci tymi badaniami mieli wyrównane choroby wątroby, w tym marskość wątroby Sofosbuwir podawano w dawce 400 mg raz na dobę.Dawka rybawiryny wynosiła 1000–1200 mg na dobę w oparciu o masę ciała, podawana w dwóch dawkach podzielonych, a dawka peginterferonu alfa 2a, w stosownych przypadkach, wynosiła 180 mcg na tydzień. W każdym badaniu czas trwania leczenia był z góry określony i nie był zależny od poziomu RNA HCV uczestników (brak algorytmu zależnego od odpowiedzi).
Wartości RNA HCV w osoczu mierzono w badaniach klinicznych testem COBAS TaqMan HCV (wersja 2.0), stosowanym z High Pure System. Test miał dolną granicę kwantyfikacji (dolna granica oznaczalności, LLOQ) 25 jm/ml. We wszystkich badaniach trwała odpowiedź wirusologiczna (trwała odpowiedź wirusologiczna, SVR) był głównym punktem końcowym określania wskaźnika wyleczeń HCV i został zdefiniowany jako poziomy RNA HCV poniżej LLOQ 12 tygodni po zakończeniu leczenia (SVR12).
Badania kliniczne u osób z przewlekłym wirusowym zapaleniem wątroby typu C o genotypie 1, 4, 5 i 6
Osoby wcześniej nieleczone – NEUTRYNA (badanie 110)
NEUTRINO było otwartym, jednoramiennym badaniem oceniającym 12-tygodniowe leczenie sofosbuwirem w skojarzeniu z peginterferonem alfa 2a i rybawiryną u nieleczonych wcześniej pacjentów z zakażeniem HCV o genotypie 1, 4, 5 lub 6. .
Leczeni pacjenci (n = 327) mieli medianę wieku 54 lata (zakres: 19 do 70); 64% pacjentów stanowili mężczyźni; 79% było rasy białej, 17% rasy czarnej; 14% było pochodzenia latynoskiego lub latynoamerykańskiego; średnia budowa ciała wskaźnik masy wyniósł 29 kg/m2 (zakres: 18 do 56 kg/m2); 78% miało wyjściowe poziomy RNA HCV większe niż 6 log10 j.m./ml; 17% miało marskość wątroby; 89% miało HCV genotypu 1, a 11% miało HCV genotypu 4, 5 lub 6. Tabela 5 przedstawia wskaźniki odpowiedzi w grupie leczonej sofosbuwirem + peginterferonem alfa + rybawiryną.
Tabela 5: Wskaźniki odpowiedzi w badaniu NEUTRINO
a Mianownikiem nawrotu jest liczba pacjentów z HCV RNA
b „Inne” obejmuje pacjentów, którzy nie osiągnęli SVR12 i nie spełnili kryteriów niepowodzenia wirusologicznego (np. utraconych z obserwacji).
Odsetki odpowiedzi dla wybranych podgrup przedstawiono w Tabeli 6.
Tabela 6: Odsetki SVR12 dla wybranych podgrup w badaniu NEUTRINO
Odsetki SVR12 były podobnie podwyższone u pacjentów z allelem IL28B C/C [94/95 (99%)] i nie-C/C (C/T lub T/T) [202/232 (87%)] na początku badania.
27/28 pacjentów z zakażeniem HCV genotypu 4 osiągnęło SVR12. Tylko jedna osoba zakażona HCV genotypu 5 i wszystkich 6 osób zakażonych HCV genotypu 6 w tym badaniu osiągnęło SVR12.
Badania kliniczne u osób z przewlekłym wirusowym zapaleniem wątroby typu C o genotypie 2 i 3
Dorośli wcześniej nieleczeni - ROZDZIELENIE (badanie 1231)
FISSION było randomizowanym, otwartym, aktywnie kontrolowanym badaniem oceniającym 12-tygodniowe leczenie sofosbuwirem i rybawiryną w porównaniu z 24-tygodniowym leczeniem peginterferonem alfa 2a i rybawiryną u nieleczonych wcześniej pacjentów z genotypem 2 lub 3 HCV. rybawiryny stosowanej w ramionach sofosbuwir + rybawiryna i peginterferon alfa 2a + rybawiryna wynosiły odpowiednio 1000–1200 mg/dobę w zależności od masy ciała i 800 mg/dobę niezależnie od masy ciała. Pacjenci zostali przydzieleni losowo 1:1 i stratyfikowani według marskości wątroby (obecność przeciw brak), na genotyp HCV (2 przeciw 3) i wyjściowy poziom RNA HCV (w porównaniu z ≥6 log10 j.m./ml). Pacjenci z genotypem 2 lub 3 HCV zostali zakwalifikowani w stosunku około 1:3.
Leczeni pacjenci (n = 499) mieli medianę wieku 50 lat (zakres: 19 do 77), 66% pacjentów stanowili mężczyźni, 87% było rasy białej, 3% rasy czarnej; 14% było pochodzenia latynoskiego lub latynoamerykańskiego; średni wskaźnik masy ciała wynosił 28 kg/m2 (zakres: od 17 do 52 kg/m2); 57% miało początkowe poziomy RNA HCV większe niż 6 log10 j.m./ml; 20% miało marskość wątroby; 72% miało HCV genotypu 3. Tabela 7 raportów odsetki odpowiedzi w grupach leczonych sofosbuwir + rybawiryna i peginterferon alfa + rybawiryna.
Tabela 7: Wskaźniki odpowiedzi w badaniu FISSION
a Analiza skuteczności obejmuje 3 pacjentów z zakażeniem HCV o rekombinowanym genotypie 2/1.
b Mianownikiem nawrotu jest liczba pacjentów z HCV RNA
c „Inne” obejmuje osobników, którzy nie osiągnęli SVR12 i nie spełnili kryteriów niepowodzenia wirusologicznego (np. utraconych z obserwacji).
Różnica w całkowitych odsetkach SVR12 między grupami leczonymi sofosbuwirem + rybawiryną i peginterferonem alfa + rybawiryną wyniosła 0,3% (95% przedział ufności: -7,5% do 8,0%), a badanie spełniło wstępnie zdefiniowane kryterium równoważności.
Wskaźniki odpowiedzi dla pacjentów z marskością wątroby na początku badania przedstawiono w Tabeli 8 według genotypu HCV.
Tabela 8: Odsetki SVR12 według marskości i genotypu w badaniu FISSION
Genotyp 3do. Analiza skuteczności obejmuje 3 osoby z zakażeniem HCV o rekombinowanym genotypie 2/1.
Dorośli nietolerujący, niekwalifikujący się lub niechętni do leczenia interferonem - POSITRON (badanie 107)
POSITRON było randomizowanym, podwójnie zaślepionym, kontrolowanym placebo badaniem oceniającym 12 tygodni leczenia sofosbuwirem i rybawiryną (n = 207) w porównaniu z placebo (n = 71) u pacjentów z nietolerancją, niekwalifikujących się lub nie wyrażających zgody na leczenie interferonem. Pacjentów przydzielono losowo w stosunku 3:1 i stratyfikowano według marskości wątroby (obecność przeciw brak).
Leczeni pacjenci (n = 278) mieli medianę wieku 54 lata (zakres: 21 do 75), 54% pacjentów stanowili mężczyźni, 91% było rasy białej, 5% rasy czarnej, 11% było pochodzenia latynoskiego lub latynoamerykańskiego; średni wskaźnik masy ciała wynosił 28 kg/m2 (zakres: 18 do 53 kg/m2); 70% miało wyjściowe poziomy RNA HCV większe niż 6 log10 j.m./ml; 16% miało marskość wątroby; 49% miało HCV genotypu 3. Odsetek liczba pacjentów nietolerujących, niekwalifikujących się lub nie wyrażających zgody na leczenie interferonem wynosiła odpowiednio 9%, 44% i 47%. Większość pacjentów nigdy nie była leczona z powodu „HCV” (81,3%). Tabela 9 przedstawia wskaźniki odpowiedzi dla grup leczonych sofosbuwirem + rybawiryną i placebo.
Tabela 9: Wskaźniki odpowiedzi w badaniu POSITRON
a Mianownikiem nawrotu jest liczba pacjentów z HCV RNA
b „Inne” obejmuje pacjentów, którzy nie osiągnęli SVR12 i nie spełnili kryteriów niepowodzenia wirusologicznego (np. utraconych z obserwacji).
Odsetek SVR12 w grupie sofosbuwiru + rybawiryny był statystycznie istotny w porównaniu z placebo (p
Tabela 10 przedstawia analizę podgrup według genotypu na podstawie marskości wątroby i leczenia interferonem u niekwalifikujących się, nietolerujących, nie wyrażających zgody osobników.
Tabela 10: Odsetki SVR12 według podgrup wybranych genotypowo w badaniu POSITRON
Wcześniej leczeni dorośli – FUSION (badanie 108)
FUSION było randomizowanym, podwójnie ślepym badaniem oceniającym 12 lub 16 tygodni leczenia sofosbuwirem i rybawiryną u pacjentów, którzy nie osiągnęli SVR po wcześniejszym leczeniu opartym na interferonie (z nawrotem lub bez odpowiedzi). Pacjenci byli randomizowani w stosunku 1:1 i stratyfikowani według marskości wątroby (obecność przeciw brak) i genotyp HCV (2 przeciw 3).
Leczeni pacjenci (n = 201) mieli medianę wieku 56 lat (zakres: od 24 do 70), 70% pacjentów stanowili mężczyźni, 87% było rasy białej, 3% rasy czarnej; 9% było pochodzenia latynoskiego lub latynoamerykańskiego; średni wskaźnik masy ciała wynosił 29 kg/m2 (zakres: 19 do 44 kg/m2); 73% miało wyjściowe poziomy RNA HCV większe niż 6 log10 j.m./ml; 34% miało marskość wątroby; 63% miało genotyp 3 HCV; 75% miało już nawrócił. W tabeli 11 przedstawiono wskaźniki odpowiedzi dla grup leczonych sofosbuwirem + rybawiryną przez 12 tygodni i 16 tygodni.
Tabela 11: Wskaźniki odpowiedzi w badaniu FUSION
a Analiza skuteczności obejmuje 6 pacjentów z zakażeniem HCV o rekombinowanym genotypie 2/1.
b Mianownikiem nawrotu jest liczba pacjentów z HCV RNA
c „Inne” obejmuje osobników, którzy nie osiągnęli SVR12 i nie spełnili kryteriów niepowodzenia wirusologicznego (np. utraconych z obserwacji).
W tabeli 12 przedstawiono analizę podgrup według genotypu pod kątem marskości wątroby i odpowiedzi na wcześniejsze leczenie anty-HCV.
Tabela 12: Odsetki SVR12 według podgrup wybranych genotypowo w badaniu FUSION
Dorośli wcześniej nieleczeni i wcześniej leczeni – VALENCE (badanie 133)
VALENCE było badaniem III fazy, w którym oceniano sofosbuwir w skojarzeniu z rybawiryną na podstawie masy ciała w leczeniu zakażenia HCV genotypu 2 lub 3 u wcześniej nieleczonych pacjentów lub u osób, które nie osiągnęły SVR po wcześniejszym leczeniu opartym na interferonie, w tym u osób z wyrównanym marskość wątroby. Badanie obejmowało bezpośrednie porównanie sofosbuwiru i rybawiryny z placebo przez 12 tygodni. Jednak na podstawie pojawiających się danych badanie nie było już prowadzone w sposób zaślepiony. i wszyscy pacjenci z genotypem 2 HCV nadal otrzymywali sofosbuwir i rybawirynę przez 12 tygodni, natomiast leczenie pacjentów z genotypem 3 HCV przedłużono do 24. Jedenaście pacjentów z genotypem 3 HCV ukończyło już 12-tygodniowe leczenie sofosbuwirem i rybawiryną w momencie zmiany.
Leczeni pacjenci (n = 419) mieli medianę wieku 51 lat (zakres: 19 do 74), 60% badanych stanowili mężczyźni, mediana wskaźnika masy ciała wynosiła 25 kg/m2 (zakres: od 17 do 44 kg/m2); średni początkowy poziom RNA HCV wynosił 6,4 log10 j.m./ml; 21% miało marskość wątroby; 78% miało HCV genotypu 3; 65% zgłosiło już nawrót. Tabela 13 przedstawia wskaźniki odpowiedzi dla grup leczonych sofosbuwirem + rybawiryną przez 12 i 24 tygodnie.
Osoby, które otrzymały placebo, nie zostały uwzględnione w tabelach, ponieważ żaden z nich nie osiągnął SVR12.
Tabela 13: Odsetki odpowiedzi w badaniu VALENCE
a Mianownikiem nawrotu jest liczba pacjentów z HCV RNA
b „Inne” obejmuje pacjentów, którzy nie osiągnęli SVR12 i nie spełnili kryteriów niepowodzenia wirusologicznego (np. utraconych z obserwacji).
W tabeli 14 przedstawiono analizę podgrup według genotypu pod względem marskości wątroby i ekspozycji na wcześniejsze leczenie anty-HCV.
Tabela 14: Odsetki SVR12 według podgrup wybranych genotypowo w badaniu VALENCE
Zgodność SVR12-SVR24
Zgodność między SVR12 i SVR24 (SVR 24 tygodnie po zakończeniu leczenia) po leczeniu sofosbuwirem w skojarzeniu z rybawiryną lub rybawiryną i pegylowanym interferonem wykazuje dodatnią wartość predykcyjną 99% i ujemną wartość predykcyjną 99%.
Skuteczność kliniczna i bezpieczeństwo w szczególnych populacjach
Pacjenci z koinfekcją HCV/HIV – PHOTON-1 (badanie 123)
Sofosbuwir oceniano w otwartym badaniu klinicznym w celu określenia skuteczności klinicznej i bezpieczeństwa 12 lub 24 tygodniowego leczenia sofosbuwirem i rybawiryną u pacjentów z przewlekłym wirusowym zapaleniem wątroby typu C o genotypie 1, 2 lub 3 i jednocześnie zakażonych HIV-1. z genotypem 2 i 3 byli wcześniej nieleczeni lub wcześniej nieleczeni, podczas gdy wcześniej nieleczeni byli pacjenci z genotypem 1. Czas trwania leczenia wynosił 12 tygodni u nieleczonych wcześniej pacjentów zakażonych wirusem HIV-1. wcześniej leczeni pacjenci, zakażeni HCV o genotypie 3, a także pacjenci z zakażeniem HCV genotypu 1. Pacjenci otrzymywali 400 mg sofosbuwiru i rybawiryny dziennie w zależności od masy ciała (1000 mg dla osób o masie ciała poniżej 75 kg lub 1200 mg dla osób o masie ciała 75 kg). kg lub więcej). i CD4+ powyżej 500 komórek/mm3 lub wykazywały supresję wirusologiczną HIV-1 i liczbę komórek CD4+ powyżej 200 komórek/mm3. Dziewięćdziesiąt pięć procent pacjentów otrzymywało leczenie przeciwretrowirusowe w momencie włączenia do badania.Wstępne dane dotyczące SVR12 są dostępne dla 210 pacjentów.
Tabela 15 przedstawia wskaźniki odpowiedzi według genotypu i ekspozycji na wcześniejsze leczenie anty-HCV.
Tabela 15: Wskaźniki odpowiedzi w badaniu PHOTON-1
a Mianownikiem nawrotu jest liczba pacjentów z HCV RNA
b „Inne” obejmuje pacjentów, którzy nie osiągnęli SVR12 i nie spełnili kryteriów niepowodzenia wirusologicznego (np. utraconych z obserwacji).
W tabeli 16 przedstawiono analizę podgrup według genotypu pod kątem marskości wątroby.
Tabela 16: Odsetki SVR12 według podgrup z wybranym genotypem w badaniu PHOTON-1
NT = nieleczone; PT = wcześniej leczony.
Pacjenci oczekujący na przeszczep wątroby – badanie 2025
Sofosbuwir badano u pacjentów zakażonych HCV oczekujących na przeszczepienie wątroby w otwartym badaniu klinicznym w celu określenia bezpieczeństwa i skuteczności sofosbuwiru i rybawiryny podawanych przed przeszczepem w celu zapobiegania ponownemu zakażeniu HCV po przeszczepie. odpowiedź wirusologiczna przeszczepu (odpowiedź wirusologiczna po przeszczepie, pTVR, HCV RNA Tabela 17: Odpowiedź wirusologiczna po przeszczepieniu u pacjentów z RNA HCV a Podmioty, które mogą być oceniane, to z definicji osoby, które osiągnęły przedział obserwacji określony w czasie wstępnej analizy. b pTVR: odpowiedź wirusologiczna po przeszczepie (HCV RNA
U pacjentów, którzy przerwali terapię po 24 tygodniach, zgodnie z protokołem, odsetek nawrotów wynosił 11/15. Biorcy przeszczepu wątroby — badanie 0126 Sofosbuwir badano w otwartym badaniu klinicznym w celu określenia bezpieczeństwa i skuteczności 24-tygodniowego leczenia sofosbuwirem i rybawiryną u biorców przeszczepu wątroby z przewlekłym wirusowym zapaleniem wątroby typu C.Zakwalifikowani pacjenci mieli co najmniej 18 lat i przeszli przeszczep wątroby na 6 do 150 miesięcy przed badaniem przesiewowym. W badaniu przesiewowym badani mieli RNA HCV ≥104 IU/ml i udokumentowane dowody przewlekłego zakażenia HCV przed przeszczepem. Dawka początkowa rybawiryny wynosiła 400 mg, podzielona na dwie dawki dobowe. Jeśli pacjenci utrzymywali poziom hemoglobiny ≥12 g/dl, dawkę rybawiryny zwiększano w tygodniach 2., 4. i do 4 tygodni do czasu podania odpowiedniej dawki w oparciu o masę ciała (1000 mg na dobę u osób o masie ciała poniżej 75 kg, 1200 mg dziennie u osób ważących 75 kg lub więcej). Mediana dawki rybawiryny wynosiła 600 mg-800 mg na dobę w tygodniach 4-24. Do badania włączono czterdziestu pacjentów (33 z zakażeniem HCV genotypu 1, 6 z zakażeniem HCV genotypu 3 i 1 z zakażeniem HCV genotypu 4), u 35 z których wcześniejsza terapia oparta na interferonie nie powiodła się, a 16 z nich cierpiało na marskość wątroby. Dwadzieścia osiem z 40 pacjentów (70%) osiągnęło SVR12: 22/33 (73%) z zakażeniem HCV genotypu 1, 6/6 (100%) z zakażeniem HCV genotypu 3 i 0/1 HCV (0%) zakażonym genotypem HCV 4. Wszyscy badani, którzy osiągnęli SVR12, osiągnęli SVR24 i SVR48. Przegląd wyników według schematu leczenia i czasu trwania leczenia, porównanie badań Poniższe tabele (Tabela 18 do Tabeli 21) przedstawiają dane dotyczące dawkowania z badań fazy 2 i fazy 3, aby pomóc klinicystom określić najlepszy schemat dla poszczególnych pacjentów. Tabela 18: Wyniki według schematu terapeutycznego i czasu trwania leczenia, porównanie badań dotyczących zakażenia HCV genotypu 1 n = liczba pacjentów z odpowiedzią SVR12; N = całkowita liczba osób w grupie. a W przypadku wcześniej leczonych pacjentów z zakażeniem HCV genotypu 1 brak danych dotyczących skojarzenia sofosbuwiru, peginterferonu alfa i rybawiryny Należy rozważyć leczenie tych pacjentów i wydłużenie czasu trwania leczenia sofosbuwirem peginterferon alfa i rybawiryna powyżej 12 tygodni i do 24 tygodni, zwłaszcza w podgrupach z jednym lub więcej czynnikami historycznie związanymi z niskimi wskaźnikami odpowiedzi na terapie oparte na interferonie (uprzedni brak odpowiedzi na leczenie peginterferonem alfa i rybawiryną, zwłóknienie/zaawansowana marskość wątroby, podwyższone podstawowe stężenie wirusa, pochodzenie etniczne rasy czarnej, genotyp inny niż CC IL28B). b Badania eksploracyjne lub badania fazy 2. Wyniki należy interpretować z ostrożnością, ponieważ liczba pacjentów jest niewielka, a wybór pacjenta może mieć wpływ na częstość występowania SVR. c Dane podsumowujące z obu badań. Tabela 19: Wyniki według schematu terapeutycznego i czasu trwania leczenia, porównanie badań dotyczących zakażenia HCV genotypu 2 n = liczba pacjentów z odpowiedzią SVR12; N = całkowita liczba osób w grupie. a Dane te mają charakter wstępny. b Badania eksploracyjne lub badania fazy 2. Wyniki należy interpretować z ostrożnością, ponieważ liczba pacjentów jest niewielka, a wybór pacjenta może mieć wpływ na odsetek SVR. W badaniu ELECTRON (N = 11) czas leczenia peginterferonem alfa w skojarzeniu z sofosbuwirem + rybawiryną wynosił od 4 do 12 tygodni. c W tych dwóch badaniach wszyscy pacjenci nie mieli marskości wątroby. Tabela 20: Wyniki według schematu terapeutycznego i czasu trwania leczenia, porównanie między badaniami dotyczącymi zakażenia HCV genotypu 3 n = liczba pacjentów z odpowiedzią SVR12; N = całkowita liczba osób w grupie. a Dane te mają charakter wstępny. b Badania eksploracyjne lub badania fazy 2. Wyniki należy interpretować z ostrożnością, ponieważ liczba pacjentów jest niewielka, a wybór pacjenta może mieć wpływ na częstość występowania SVR. W badaniu ELECTRON (N = 11) czas leczenia peginterferonem alfa w skojarzeniu z sofosbuwirem + rybawiryną wynosił od 4 do 12 tygodni. C. W tych dwóch badaniach wszyscy pacjenci nie mieli marskości wątroby. Tabela 21: Wyniki według schematu terapeutycznego i czasu trwania leczenia, porównanie badań dotyczących zakażenia HCV genotypu 4, 5 lub 6 n = liczba pacjentów z odpowiedzią SVR12; N = całkowita liczba osób w grupie. Populacja pediatryczna Europejska Agencja Leków odroczyła obowiązek przedstawienia wyników badań sofosbuwiru w co najmniej jednej podgrupie populacji pediatrycznej w leczeniu przewlekłego wirusowego zapalenia wątroby typu C (informacje na temat stosowania u dzieci, patrz punkt 4.2). Sofosbuvir jest prolekiem nukleotydowym, który jest intensywnie metabolizowany. Aktywny metabolit powstaje w hepatocytach i nie jest obserwowany w osoczu. Główny (> 90%) metabolit, GS-331007, jest nieaktywny i jest tworzony poprzez sekwencyjne i równoległe szlaki do tworzenia aktywnego metabolitu. Wchłanianie Właściwości farmakokinetyczne sofosbuwiru i głównego krążącego metabolitu GS-331007 określono u zdrowych osób dorosłych oraz u osób z przewlekłym wirusowym zapaleniem wątroby typu C. Po podaniu doustnym sofosbuwir był szybko wchłaniany, a maksymalne stężenia w osoczu obserwowano po 0,5-2 godzinach od podania, niezależnie od poziomu dawki. Maksymalne stężenie GS-331007 w osoczu zaobserwowano 2 do 4 godzin po podaniu. W oparciu o analizę farmakokinetyki populacyjnej pacjentów zakażonych HCV o genotypie 1 do 6 (n = 986), AUC0-24 w stanie stacjonarnym dla sofosbuwiru i GS-331007 wynosiło 1010 ng • h / ml i 7 200 ng • h / ml. W porównaniu ze zdrowymi osobami (n = 284), AUC0-24 dla sofosbuwiru i GS-331007 było odpowiednio o 57% wyższe i 39% niższe u osób zakażonych HCV. Skutki przyjmowania pokarmu W porównaniu do postu, podanie pojedynczej dawki sofosbuwiru ze standaryzowanym wysokotłuszczowym posiłkiem spowolniło tempo wchłaniania sofosbuwiru.Zakres wchłaniania sofosbuwiru wzrósł około 1,8-krotnie, z ograniczonym wpływem na stężenie maksymalne. 331007 nie uległ zmianie w obecności posiłku o wysokiej zawartości tłuszczu. Dystrybucja Sofosbuwir nie jest substratem dla transporterów wychwytu wątrobowego, polipeptydu transportującego aniony organiczne (polipetyd transportujący aniony organiczne, OATP) 1B1 lub 1B3 oraz transporter kationów organicznych (transporter kationów organicznych, OCT) 1. Chociaż podlega aktywnemu wydzielaniu kanalikowemu, GS-331007 nie jest substratem transporterów nerkowych, takich jak transporter anionów organicznych (organiczny transporter anionów, OAT) 1 lub 3, OCT2, MRP2, P-gp, BCRP lub MATE1. Sofosbuvir i GS-331007 nie są inhibitorami transporterów leków P-gp, BCRP, MRP2, BSEP, OATP1B1, OATP1B3 i OCT1. GS-331007 nie jest inhibitorem OAT1, OCT2 i MATE1. Sofosbuwir w około 85% wiąże się z białkami osocza ludzkiego (dane ex vivo) i wiązanie jest niezależne od stężenia leku w zakresie od 1 mcg/ml do 20 mcg/ml Wiązanie GS-331007 z białkami w ludzkim osoczu było minimalne.Po pojedynczej dawce 400 mg [14C]-sofosbuwiru u osób zdrowych, stosunek radioaktywności 14C w krwi do osocza wynosił około 0,7. Biotransformacja Sofosbuwir jest intensywnie metabolizowany w wątrobie z wytworzeniem farmakologicznie czynnego trifosforanu analogu nukleozydu GS-461203. Szlak aktywacji metabolicznej obejmuje sekwencyjną hydrolizę reszty estru karboksylowego, katalizowaną przez ludzkie enzymy katepsynę A (CatA) lub karboksyloesterazę 1 (CES1). rozszczepienie fosforoamidu przez białko HINT1 (białko wiążące nukleotydy triady histydynowej 1), po której następuje fosforylacja na szlaku biosyntezy nukleotydów pirymidynowych. Defosforylacja indukuje tworzenie metabolitu nukleozydu GS-331007, który nie może być skutecznie refosforylowany i nie wykazuje aktywności przeciw HCV. in vitro. Sofosbuwir i GS-331007 nie są substratami ani inhibitorami enzymów UGT1A1 lub CYP3A4, CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19 i CYP2D6. Po podaniu pojedynczej dawki doustnej 400 mg [14C]-sofosbuwiru, sofosbuwir i GS-331007 były odpowiedzialne odpowiednio za około 4% i > 90% ogólnoustrojowej ekspozycji związanej z lekiem (suma skorygowanej względem masy AUC sofosbuwiru i jego metabolitów ). Eliminacja Po podaniu pojedynczej dawki doustnej 400 mg [14C]-sofosbuwiru średni całkowity odzysk dawki był większy niż 92% i obejmował odpowiednio około 80%, 14% i 2,5% na podstawie odzysku w moczu w kale i wydychanym powietrzu. Większość dawki sofosbuwiru odzyskanej w moczu stanowił GS-331007 (78%), natomiast 3,5% odzyskano w postaci sofosbuwiru. Dane te wskazują, że klirens nerkowy jest główną drogą eliminacji GS-331007 i że wysoki odsetek jest aktywnie wydzielany. Mediana końcowych okresów półtrwania sofosbuwiru i GS-331007 wynosiła odpowiednio 0,4 i 27 godzin. Liniowość / Nieliniowość Liniowość dawki sofosbuwiru i jego głównego metabolitu GS-331007 została określona u zdrowych osób na czczo. AUC sofosbuwiru i GS-331007 są w przybliżeniu proporcjonalne do dawki w zakresie od 200 mg do 400 mg. Właściwości farmakokinetyczne w poszczególnych populacjach Płeć i pochodzenie etniczne Nie stwierdzono klinicznie istotnych różnic w farmakokinetyce sofosbuwiru i GS-331007 ze względu na płeć lub pochodzenie etniczne. Starsi mieszkańcy Analiza farmakokinetyki populacyjnej u osób zakażonych HCV wykazała, że w analizowanej grupie wiekowej (19-75 lat) wiek nie miał klinicznie istotnego wpływu na narażenie na sofosbuwir i GS-331007. Badania kliniczne przeprowadzone z sofosbuwirem obejmowały 65 osób w wieku 65 lat i starszych. Wskaźniki odpowiedzi obserwowane u osób w wieku powyżej 65 lat były podobne do tych u młodszych osób we wszystkich leczonych grupach. Zaburzenia czynności nerek Farmakokinetykę sofosbuwiru badano u pacjentów z ujemnym wynikiem oznaczenia HCV z łagodnymi (eGFR ≥50 i 2), umiarkowanymi (eGFR ≥30 i 2) i ciężkimi (eGFR 2) zaburzeniami czynności nerek oraz u pacjentów z ESRD i wymagających hemodializy po podaniu pojedynczej dawki. mg sofosbuwiru. W porównaniu z osobami z prawidłową czynnością nerek (eGFR > 80 ml/min/1,73 m2), AUC0-inf sofosbuwiru było odpowiednio o 61%, 107% i 171% większe w przypadku łagodnych zaburzeń czynności nerek, umiarkowanych i ciężkich, podczas gdy AUC0-inf GS-331007 był o 55%, 88% i 451% wyższy. U pacjentów z ESRD, w porównaniu z osobami z prawidłową czynnością nerek, AUC0-inf sofosbuwiru było o 28% wyższe, gdy sofosbuwir podawano 1 godzinę przed hemodializą i 60% wyższe, gdy sofosbuwir był podawany 1 godzinę po hemodializie. wiarygodnie określić AUC0-inf GS-331007 u pacjentów z ESRD. Jednak dane wskazują na co najmniej 10-krotnie i 20-krotnie większą ekspozycję na GS-331007 u osób z ESRD w porównaniu ze zdrowymi osobami, gdy produkt Sovaldi podawano odpowiednio 1 godzinę przed lub 1 godzinę po hemodializie. Dzięki hemodializie możliwe jest skuteczne usunięcie (53% wskaźnika ekstrakcji) głównego krążącego metabolitu GS-331007. 4-godzinna „hemodializa" usunęła około 18% podanej dawki. Nie ma konieczności dostosowania dawki u pacjentów z łagodnymi lub umiarkowanymi zaburzeniami czynności nerek. Nie ustalono bezpieczeństwa stosowania produktu Sovaldi u pacjentów z ciężkimi zaburzeniami czynności nerek lub ESRD (patrz punkt 4.4 ). Zaburzenia czynności wątroby Farmakokinetykę sofosbuwiru badano po podaniu 400 mg sofosbuwiru przez 7 dni u pacjentów z zakażeniem HCV i umiarkowanymi lub ciężkimi zaburzeniami czynności wątroby (klasa B i C według CPT). W porównaniu z osobami z prawidłową czynnością wątroby, AUC0-24 dla sofosbuwiru było odpowiednio o 126% i 143% większe w umiarkowanych i ciężkich zaburzeniach czynności wątroby, podczas gdy AUC0-24 dla GS-331007 było wyższe niż 18% i 9%. Analiza farmakokinetyki populacyjnej u osób zakażonych HCV wykazała, że marskość wątroby nie ma klinicznie istotnego wpływu na ekspozycję na sofosbuwir i GS-331007. Nie zaleca się dostosowywania dawki u pacjentów z łagodnymi, umiarkowanymi lub ciężkimi zaburzeniami czynności wątroby (patrz punkt 4.2). Populacja pediatryczna Nie ustalono farmakokinetyki sofosbuwiru i GS-331007 u dzieci i młodzieży (patrz punkt 4.2). Zależność farmakokinetyczna (która) / farmakodynamiczna (która) Wykazano, że skuteczność pod względem szybkiej odpowiedzi wirusologicznej koreluje z ekspozycją na sofosbuwir oraz GS-331007. Nie wykazano jednak, aby jednostki te były ogólnymi zastępczymi markerami skuteczności (SVR12) przy dawce terapeutycznej 400 mg. W badaniach toksykologicznych po podaniu wielokrotnym u szczurów i psów, wysokie dawki mieszaniny diastereoizomerów 1:1 powodowały niepożądane działania na wątrobę (psy) i serce (szczury) oraz reakcje żołądkowo-jelitowe (psy). W badaniach na gryzoniach nie można było wykryć ekspozycji na sofosbuwir, prawdopodobnie ze względu na wysoką aktywność esterazy; jednak ekspozycja na główny metabolit GS-331007 w dawce niepożądanej była 29 razy (szczur) i 123 razy (ps) wyższa niż ekspozycja kliniczna po 400 mg sofosbuwiru. W badaniach toksyczności przewlekłej nie obserwowano objawów ze strony wątroby i serca przy ekspozycji 9-krotnie (szczury) i 27-krotnie (psy) większej niż ekspozycja kliniczna. Sofosbuwir nie był genotoksyczny w serii testów in vitro lub in vivo w tym mutagenność bakteryjna, aberrację chromosomową z ludzkimi limfocytami krwi obwodowej i test mikrojądrowy u myszy in vivo. Badania rakotwórczości na myszach i szczurach wskazują na brak potencjału rakotwórczego sofosbuwiru podawanego w dawkach do 600 mg/kg/dobę u myszy i 750 mg/kg/dobę u szczurów. Narażenie na GS-331007 w tych badaniach było do 30 razy (myszy) i 15 razy (szczury) większe niż narażenie kliniczne po podaniu 400 mg sofosbuwiru. Sofosbuwir nie miał wpływu na żywotność zarodków i płodów ani na płodność szczurów i nie wykazywał działania teratogennego w badaniach rozwojowych u szczurów i królików. U szczurów nie zgłoszono żadnego niekorzystnego wpływu na zachowanie, reprodukcję lub rozwój potomstwa. W badaniach na królikach ekspozycja na sofosbuwir była 9-krotnie większa niż oczekiwana ekspozycja kliniczna. W badaniach na szczurach nie można było określić narażenia na sofosbuwir, ale marginesy narażenia w oparciu o główny metabolit ludzki wynosiły od 8 do 28 razy większe niż narażenie kliniczne po podaniu 400 mg sofosbuwiru. Materiał pochodzący z sofosbuwiru był przenoszony przez łożysko ciężarnych szczurów i do mleka karmiących szczurów. Rdzeń tabletu Mannitol (E421) Celuloza mikrokrystaliczna (E460 (i)) Kroskarmeloza sodowa Krzemionka koloidalna bezwodna (E551) Stearynian magnezu (E470b) Folia powlekająca Alkohol poliwinylowy (E1203) Dwutlenek tytanu (E171) Makrogol 3350 (E1521) Talk (E553b) Żółty tlenek żelaza (E172) Nieistotne. 3 lata. Ten lek nie wymaga żadnych specjalnych warunków przechowywania. Tabletki Sovaldi są dostępne w butelkach z polietylenu o wysokiej gęstości (HDPE) z zamknięciem zabezpieczającym przed dostępem dzieci, zawierających 28 tabletek powlekanych ze środkiem osuszającym z żelu krzemionkowego i spiralą poliestrową. Dostępne są następujące wielkości opakowań: pudełka tekturowe zawierające 1 butelkę z 28 tabletkami powlekanymi i pudełka tekturowe zawierające 84 (3 butelki po 28) tabletek powlekanych. Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek. Niewykorzystany lek i odpady pochodzące z tego leku należy usunąć zgodnie z lokalnymi przepisami. Gilead Sciences International Ltd. Cambridge CB21 6GT Wielka Brytania UE / 1/13/894/001 043196017 UE / 1/13/894/002 043196029 Data pierwszej autoryzacji: 16 stycznia 2014 r. 10/2015
12. tydzień po przeszczepie (pTVR) b
Odpowiedź wirusologiczna u ocenianych osób 23/37 (62%)
Populacja pacjentów (numer badania/nazwa) Schemat / Czas trwania Podgrupa Procenty SVR12 (n / N) Leczenie naiwne (NEUTRYNA) SOF + PEG + RBV 12 tygodni Światowy 90% (262/292) Genotyp 1a 92% (206/225) Genotyp 1b 83% (55/66) Nie ma marskości 93% (253/273) marskość wątroby 80% (43/54) Nieleczeni i współzakażeni HIV (PHOTON-1) SOF + RBV 24 tygodnie Światowy 76% (87/114) Genotyp 1a 82% (74/90) Genotyp 1b 54% (13/24) Nie ma marskości 77% (84/109) marskość wątroby 60% (3/5) Osoby nieleczone (QUANTUMbe 11-1-0258b) SOF + RBV 24 tygodnie Globalny 65% (104/159) Genotyp 1ac 69% (84/121) Genotyp 1bc 53% (20/38) Nie ma cirotic 68% (100/148)
Ciroticic 36% (4/11)
Populacja pacjentów (numer badania/nazwa) Schemat / Czas trwania Podgrupa Procenty SVR12 (n / N) Leczenie naiwne (ROZDZIAŁ) SOF + RBV 12 tygodni Światowy 95% (69/73) Nie ma marskości 97% (59/61) marskość wątroby 83% (10/12) Nietolerancja, niekwalifikacja lub niechęć do leczenia interferonem (POSITRON) SOF + RBV 12 tygodni Światowy 93% (101/109) Nie ma marskości 92% (85/92) marskość wątroby 94% (16/17) Wcześniej poddane obróbce (FUSION) SOF + RBV 12 tygodni Światowy 82% (32/39) Nie ma marskości 90% (26/29) marskość wątroby 60% (6/10) Leczenie naiwne (WALENCJA) SOF + RBV 12 tygodni Światowy 97% (31/32) Nie ma marskości 97% (29/30) marskość wątroby 100% (2/2) Wcześniej leczone (WALENCJA) SOF + RBV 12 tygodni Światowy 90% (37/41) Nie ma marskości 91% (30/33) marskość wątroby 88% (7/8) Wcześniej poddane obróbce (FUSION) SOF + RBV 16 tygodni Światowy 89% (31/35) Nie ma marskości 92% (24/26) marskość wątroby 78% (7/9) Nieleczeni i współzakażeni HIV (PHOTON-1) SOF + RBV 12 tygodni Światowy 88% (23/26) Nie ma marskości 88% (22/25) marskość wątroby 100% (1/1) Wcześniej leczeni i współzakażeni HIV (PHOTON-1) SOF + RBV 24 tygodnie Globale 93% (14/15) Nie marskość wątroby 92% (12/13) Cirroticia 100% (2/2) Osoby nieleczone (ELECTRONbe PROTONb) SOF + PEG + RBV 12 tygodni Światowy 96% (25/26) c Wcześniej leczone (LONE STAR-2b) SOF + PEG + RBV 12 tygodni Światowy 96% (22/23) Nie ma marskości 100% (9/9)
marskość wątroby 93% (13/14)
Populacja pacjentów (numer badania/nazwa) Schemat / Czas trwania Podgrupa Procenty SVR12 (n / N) Leczenie naiwne (ROZDZIAŁ) SOF + RBV 12 tygodni Światowy 56% (102/183) Nie ma marskości 61% (89/145) marskość wątroby 34% (13/38) Nietolerancja, niekwalifikacja lub niechęć do leczenia interferonem (POSITRON) SOF + RBV 12 tygodni Światowy 61% (60/98) Nie ma marskości 68% (57/84) marskość wątroby 21% (3/14) Wcześniej poddane obróbce (FUSION) SOF + RBV 12 tygodni Światowy 30% (19/64) Nie ma marskości 37% (14/38) marskość wątroby 19% (5/26) Wcześniej poddane obróbce (FUSION) SOF + RBV 16 tygodni Światowy 62% (39/63) Nie ma marskości 63% (25/40) marskość wątroby 61% (14/23) Leczenie naiwne (WALENCJA) SOF + RBV 24 tygodnie Światowy 93% (98/105) Nie ma marskości 94% (86/92) marskość wątroby 92% (12/13) Wcześniej leczone (WALENCJA) SOF + RBV 24 tygodnie Światowy 77% (112/145) Nie ma marskości 85% (85/100) marskość wątroby 60% (27/45) Nieleczeni i współzakażeni HIV (PHOTON-1) SOF + RBV 12 tygodni Światowy 67% (28/42) Nie ma marskości 67% (24/36) marskość wątroby 67% (4/6) Wcześniej leczeni i współzakażeni HIV (PHOTON-1) SOF + RBV 24 tygodnie Globale 92% (12/13) Nie marskość wątroby 100% (8/8) Cirroticia 80% (4/5) Osoby nieleczone (ELECTRONbe PROTONb) SOF + PEG + RBV 12 tygodni Globalny 97% (38/39) Wcześniej leczone (LONE STAR-2b) SOF + PEG + RBV 12 tygodni Światowy 83% (20/24) Nie ma marskości 83% (10/12)
marskość wątroby 83% (10/12)
Populacja pacjentów (numer badania/nazwa) Schemat / Czas trwania Podgrupa Procenty SVR12 (n / N) Leczenie naiwne (NEUTRYNA) SOF + PEG + RBV 12 tygodni Światowy 97% (34/35) Nie ma marskości 100% (33/33)
marskość wątroby 50% (1/2)
05.2 Właściwości farmakokinetyczne
05.3 Przedkliniczne dane o bezpieczeństwie
06.0 INFORMACJE FARMACEUTYCZNE
06.1 Zaróbki
06.2 Niekompatybilność
06.3 Okres ważności
06.4 Specjalne środki ostrożności przy przechowywaniu
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania
06.6 Instrukcje użytkowania i obsługi
07.0 PODMIOT POZWOLENIA NA DOPUSZCZENIE DO OBROTU
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA
10.0 DATA ZMIAN TEKSTU
11.0 W PRZYPADKU RADIOLEKÓW KOMPLETNE DANE DOTYCZĄCE WEWNĘTRZNEJ DOZYMETRII PROMIENIOWANIA
12.0 DLA RADIOLEKÓW, DODATKOWE INSTRUKCJE SZCZEGÓŁOWE DOTYCZĄCE PRZYGOTOWAWCZEGO PRZYGOTOWANIA I KONTROLI JAKOŚCI