Składniki aktywne: skoniugowana szczepionka przeciw meningokokom z grup A, C, W135 i Y
Proszek i roztwór do sporządzania roztworu do wstrzykiwań (proszek i roztwór do wstrzykiwań).
Dlaczego stosuje się Menveo? Po co to jest?
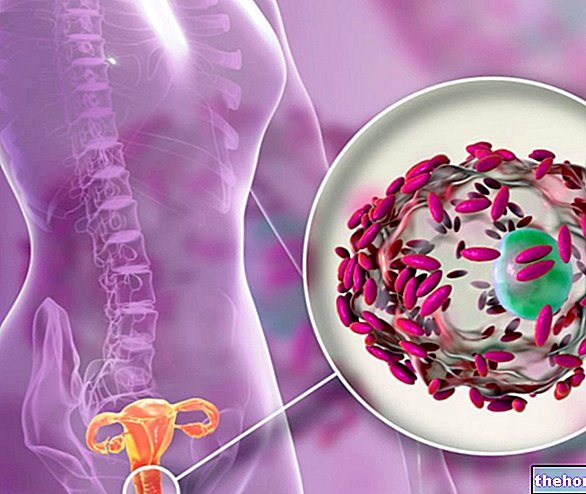
Menveo jest szczepionką stosowaną do czynnego uodporniania dzieci (w wieku od 2 lat), młodzieży (w wieku od 11 lat) i dorosłych zagrożonych ekspozycją na serogrupy A, C, W135 i Y bakterii o nazwie Neisseria meningitidis aby zapobiec wystąpieniu chorób inwazyjnych. Szczepionka działa poprzez wywołanie w organizmie ochrony (przeciwciał) przeciwko tym bakteriom.
Bakterie Neisseria meningitidis z grup A, C, W135 i Y mogą powodować poważne, a czasem zagrażające życiu infekcje, takie jak zapalenie opon mózgowych i posocznica (zatrucie krwi).
Menveo nie może powodować bakteryjnego zapalenia opon mózgowych. Szczepionka zawiera białko (o nazwie CRM197) z bakterii wywołującej błonicę. Menveo nie chroni przed błonicą. Oznacza to, że Ty (lub Twoje dziecko) będziesz potrzebował innych szczepień, aby chronić się przed błonicą, gdy są one konieczne lub zalecone przez lekarza.
Przeciwwskazania Kiedy nie należy stosować Menveo
Nie stosować Menveo, jeśli osoba, która ma być zaszczepiona
- wystąpiła reakcja alergiczna na substancje czynne lub którykolwiek składnik tej szczepionki (wymienione w punkcie 6)
- miałeś reakcję alergiczną na toksoid błoniczy (substancję stosowaną w kilku innych szczepionkach)
- ma chorobę z wysoką gorączką. Jednak sam łagodny epizod gorączkowy i/lub „zakażenie górnych dróg oddechowych (np. przeziębienie)” nie jest wystarczającym powodem do odroczenia szczepienia.
Środki ostrożności dotyczące stosowania Informacje ważne przed przyjęciem leku Menveo
Należy poinformować lekarza lub pielęgniarkę przed otrzymaniem leku Menveo, jeśli osoba, która ma zostać zaszczepiona:
- osłabiony układ odpornościowy. Istnieje niewiele danych na temat skuteczności Menveo podawanego osobom, których układ odpornościowy jest osłabiony z powodu stosowania leków immunosupresyjnych, zakażenia wirusem HIV i innych możliwych przyczyn.U tych osób skuteczność Menveo może być zmniejszona.
- hemofilia lub jakikolwiek inny problem, który może zatrzymać prawidłowe krzepnięcie krwi, na przykład u pacjentów otrzymujących leki przeciwzakrzepowe.
W odpowiedzi na każde wstrzyknięcie igły może wystąpić omdlenie, uczucie omdlenia lub inne reakcje związane ze stresem. Porozmawiaj ze swoim lekarzem lub pielęgniarką, jeśli miałeś wcześniej tego typu reakcje.
Ta szczepionka może chronić jedynie przed bakteriami meningokokowymi z grupy A, C, W135 i Y. Nie może chronić przed innymi typami bakterii meningokokowych innych niż grupy A, C, W135 i Y ani innymi czynnikami powodującymi zapalenie opon mózgowych i posocznicę (zatrucie krwi).
Podobnie jak w przypadku innych szczepionek, Menveo może nie chronić 100% osób, które otrzymały szczepionkę.
Można rozważyć hipotezę podania dawki przypominającej w celu utrzymania ochrony, jeśli osoba zaszczepiona otrzymywała dawkę Menveo przez ponad rok i nadal jest narażona na szczególne ryzyko ekspozycji na bakterie meningokokowe z grupy A. Lekarz poinformuje Cię o tym czy i kiedy przyjąć dawkę przypominającą.
Interakcje Jakie leki lub pokarmy mogą modyfikować działanie Menveo
Należy powiedzieć lekarzowi lub pielęgniarce, jeśli pacjent przyjmuje, ostatnio przyjmował lub może przyjmować jakiekolwiek inne leki.
Menveo można podawać jednocześnie z innymi szczepionkami, ale wszelkie inne szczepionki najlepiej wstrzyknąć w ramię inne niż miejsce wstrzyknięcia Menveo.
Należą do nich: szczepionka przeciw krztuścowi, tężcowi i krztuścowi (Tdap), szczepionka przeciwko wirusowi brodawczaka ludzkiego (HPV), szczepionka przeciw żółtej febrze, szczepionka dur brzuszny (polisacharyd Vi), szczepionka przeciwko japońskiemu zapaleniu mózgu, szczepionka przeciwko wściekliźnie oraz szczepionka przeciw wirusowemu zapaleniu wątroby typu A i B.
Działanie Menveo może być osłabione, jeśli zostanie podane osobom przyjmującym leki hamujące układ odpornościowy.
W przypadku wstrzyknięcia wielu szczepionek w tym samym czasie, należy użyć oddzielnych miejsc wstrzyknięcia.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
Ciąża, karmienie piersią i płodność
Należy poinformować lekarza przed przyjęciem tego leku, jeśli pacjentka jest w ciąży, karmi piersią, podejrzewa ciążę lub planuje zajść w ciążę. Jednak lekarz lub pielęgniarka może zalecić Menveo, jeśli ryzyko zakażenia bakteriami meningokokowymi z grup A, C, W-135 i Y jest wysokie.
Prowadzenie i używanie maszyn
Nie przeprowadzono badań nad zdolnością prowadzenia pojazdów i obsługiwania maszyn.Po szczepieniu zgłaszano bardzo rzadkie przypadki zawrotów głowy.Zdolność do prowadzenia pojazdów i obsługiwania maszyn może być przejściowo osłabiona.
Menveo zawiera
Ten lek zawiera mniej niż 1 mmol sodu (23 mg) na dawkę i dlatego zasadniczo jest „wolny od sodu”.
Ten lek zawiera mniej niż 1 mmol potasu (39 mg) na dawkę i dlatego zasadniczo jest „wolny od potasu”.
Dawkowanie i sposób użycia Jak stosować Menveo: Dawkowanie
Menveo zostanie podane Tobie lub Twojemu dziecku przez lekarza lub pielęgniarkę.
Szczepionka jest zwykle wstrzykiwana w mięsień ramienia (naramienny) u dzieci (w wieku od 2 lat), młodzieży i dorosłych. Lekarz lub pielęgniarka zachowają ostrożność, aby nie wstrzyknąć szczepionki do naczynia krwionośnego i sprawdzi, czy jest ona wstrzykiwana do mięśnia, a nie do skóry.
Dzieci (w wieku od 2 lat), młodzież i dorośli: zostanie podane jedno wstrzyknięcie (0,5 ml).
Bezpieczeństwo i skuteczność stosowania leku Menveo u dzieci w wieku poniżej 2 lat nie zostały jeszcze ustalone.Dane dotyczące osób w wieku od 56 do 65 lat są ograniczone i brak jest danych dla osób w wieku powyżej 65 lat.
Należy poinformować lekarza, jeśli pacjent otrzymał wcześniej „wstrzyknięcie leku Menveo lub inną szczepionkę przeciw meningokokom. Lekarz poinformuje pacjenta, czy konieczne jest kolejne” wstrzyknięcie leku Menveo.
Informacje dotyczące rekonstytucji szczepionki znajdują się w części przeznaczonej dla lekarza lub pracownika służby zdrowia na końcu tej ulotki.
W przypadku dalszych pytań dotyczących stosowania tego leku należy zwrócić się do lekarza lub pielęgniarki.
Skutki uboczne Jakie są skutki uboczne Menveo
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Najczęstsze działania niepożądane zgłaszane podczas badań klinicznych zwykle trwały od jednego dnia do dwóch dni i na ogół nie były poważne.
Poniżej wymieniono działania niepożądane zgłaszane podczas badań klinicznych u dzieci (2-10 lat).
Bardzo często (mogą wystąpić u więcej niż 1 na 10 osób): senność, ból głowy, drażliwość, ogólne złe samopoczucie, ból w miejscu wstrzyknięcia, zaczerwienienie w miejscu wstrzyknięcia (≤50 mm), stwardnienie w miejscu wstrzyknięcia (≤50 mm)
Często (mogą wystąpić u nie więcej niż 1 na 10 osób): zmiana nawyków żywieniowych, nudności, wymioty, biegunka, wysypka, ból mięśni, ból stawów, dreszcze, gorączka ≥38 °C, zaczerwienienie w miejscu wstrzyknięcia (>50 mm) i stwardnienie miejsca wstrzyknięcia (> 50 mm)
Niezbyt często (mogą wystąpić u nie więcej niż 1 na 100 osób): swędzenie w miejscu wstrzyknięcia
Poniżej wymieniono najczęstsze działania niepożądane zgłaszane podczas badań klinicznych u młodzieży (w wieku 11 lat i starszych) i dorosłych.
Bardzo często: ból głowy, nudności, ból w miejscu wstrzyknięcia, zaczerwienienie w miejscu wstrzyknięcia (≤50 mm), stwardnienie w miejscu wstrzyknięcia (≤50 mm), ból mięśni, ogólne złe samopoczucie
Często: wysypka, zaczerwienienie w miejscu wstrzyknięcia (>50 mm), stwardnienie w miejscu wstrzyknięcia (>50 mm), ból stawów, gorączka ≥38 °C, dreszcze
Niezbyt często: zawroty głowy, swędzenie w miejscu wstrzyknięcia
Działania niepożądane zgłaszane od czasu wprowadzenia leku Menveo na rynek: reakcje alergiczne, które mogą obejmować silny obrzęk warg, jamy ustnej, gardła (co może powodować trudności w połykaniu), trudności w oddychaniu ze świszczącym oddechem lub kaszlem, wysypkę i obrzęk rąk , stopy i kostki, utrata przytomności, bardzo niskie ciśnienie krwi; napady (napady), w tym napady związane z gorączką; zaburzenia równowagi, omdlenia, zakażenie skóry w miejscu wstrzyknięcia, obrzęk w miejscu wstrzyknięcia, w tym rozległy obrzęk kończyny, w którą wykonano wstrzyknięcie.
Jeśli wystąpi ciężka reakcja alergiczna, natychmiast skontaktuj się z lekarzem lub udaj się / zabierz dziecko na pogotowie, ponieważ może wymagać „pilnej pomocy medycznej”.
Zgłaszanie skutków ubocznych
Jeśli wystąpią jakiekolwiek działania niepożądane, w tym wszelkie możliwe działania niepożądane niewymienione w tej ulotce, należy porozmawiać z lekarzem, farmaceutą lub pielęgniarką.Można również zgłaszać działania niepożądane bezpośrednio za pośrednictwem krajowego systemu zgłaszania wymienionego w załączniku V. działania niepożądane, którym możesz pomóc dostarczyć więcej informacji na temat bezpieczeństwa tego leku.
Wygaśnięcie i przechowywanie
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na pudełku i fiolce po oznaczeniu EXP.Termin ważności oznacza ostatni dzień miesiąca.
Przechowywać w lodówce (2°C - 8°C). Nie zamrażać. Fiolki przechowywać w opakowaniu zewnętrznym w celu ochrony leku przed światłem.
Produkt należy zużyć natychmiast po rekonstytucji. Wykazano jednak stabilność fizykochemiczną przez 8 godzin po rekonstytucji w temperaturze poniżej 25°C.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Lekarz lub pielęgniarka zorganizują usunięcie leku. Pomoże to chronić środowisko.
Termin ">Inne informacje
Co zawiera Menveo
Jedna dawka (0,5 ml zrekonstytuowanej szczepionki) zawiera:
Aktywnymi składnikami są:
- pierwotnie zawarty w proszku
- meningokokowy oligosacharyd grupy A 10 mikrogramów sprzężony z białkiem Corynebacterium diphtheriae CRM197 16,7 do 33,3 mikrogramów
- pierwotnie zawarty w rozwiązaniu
- Oligosacharyd meningokoków grupy C 5 mikrogramów skoniugowany z białkiem CRM197 Corynebacterium diphtheriae 7,1 do 12,5 mikrogramów
- Oligosacharyd meningokoków grupy W135 5 mikrogramów sprzężony z białkiem Corynebacterium diphtheriae CRM197 od 3,3 do 8,3 mikrograma
- Oligosacharyd meningokokowy grupy Y 5 mikrogramów skoniugowany z białkiem CRM197 Corynebacterium diphtheriae 5,6 do 10,0 mikrogramów
Pozostałe składniki (substancje pomocnicze) to:
W proszku: jednozasadowy fosforan potasu i sacharoza.
W roztworze: chlorek sodu, jednowodny diwodorofosforan sodu, dwuwodny wodorofosforan sodu i woda do wstrzykiwań (patrz także koniec sekcji 2).
Opis wyglądu Menveo i zawartości opakowania
Menveo to proszek i roztwór do wstrzykiwań.
Każda dawka Menveo jest dostarczana jako:
- 1 fiolka zawierająca liofilizowany składnik koniugatu MenA w postaci białego do białawego proszku;
- 1 fiolka zawierająca płynny składnik koniugatu MenCWY w postaci klarownego roztworu;
- Wielkość opakowania to jedna dawka (2 fiolki) lub pięć dawek (10 fiolek).
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
Zawartość dwóch składników (fiolki i fiolki) należy wymieszać przed szczepieniem, aby uzyskać 1 dawkę 0,5 ml.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO -
MNIEJ PROSZKU I ROZTWORU DO ROZTWORU DO WTRYSKU
SKOJAGOWANA SZCZEPIONKA PRZECIW MENINGOKOKOM GRUPY A, C, W135 I Y
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY -
Jedna dawka (0,5 ml zrekonstytuowanej szczepionki) zawiera:
(pierwotnie zawarty w proszku)
• 10 μg oligosacharydów meningokokowych grupy A sprzężonych z białkiem Corynebacterium diphtheriae CRM197 od 16,7 do 33,3 mcg (pierwotnie zawarty w roztworze)
• oligosacharyd meningokoków grupy C 5 mcg sprzężony z białkiem Corynebacterium diphtheriae CRM197 od 7,1 do 12,5 mcg
• oligosacharyd z grupy meningokoków W135 5 mcg sprzężony z białkiem Corynebacterium diphtheriae CRM197 od 3,3 do 8,3 mcg
• 5 μg oligosacharydu meningokokowego grupy Y sprzężonego z białkiem Corynebacterium diphtheriae CRM197 od 5,6 do 10,0 mcg
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
03.0 POSTAĆ FARMACEUTYCZNA -
Proszek i roztwór do sporządzania roztworu do wstrzykiwań (proszek i roztwór do wstrzykiwań).
Proszek jest aglomeratem o barwie od białej do prawie białej.
Roztwór jest przejrzysty i bezbarwny.
04.0 INFORMACJE KLINICZNE -
04.1 Wskazania terapeutyczne -
Menveo jest wskazany do czynnego uodporniania dzieci (w wieku 2 lat i starszych), młodzieży i osób dorosłych zagrożonych narażeniem na grupy A, C, W135 i Y Neisseria meningitidis aby zapobiec wystąpieniu chorób inwazyjnych.
Stosowanie tej szczepionki musi być zgodne z oficjalnymi zaleceniami.
04.2 Dawkowanie i sposób podawania -
Dawkowanie
Dzieci (od 2 lat), młodzież i dorośli
Menveo należy podawać w pojedynczej dawce (0,5 ml).
Aby zapewnić optymalny poziom przeciwciał przeciwko wszystkim serogrupom szczepionkowym, harmonogram szczepienia podstawowego preparatem Menveo należy zakończyć na miesiąc przed ryzykiem narażenia na Neisseria meningitidis grupy A, C, W135 i Y; Przeciwciała bakteriobójcze (hSBA≥1: 8) obserwowano u co najmniej 64% pacjentów 1 tydzień po szczepieniu (dane dotyczące immunogenności poszczególnych grup serologicznych, patrz punkt 5.1).
Starsi mieszkańcy
Dane dotyczące osób w wieku 56-65 lat są ograniczone, a dane dotyczące osób w wieku > 65 lat nie są dostępne.
Szczepienie przypominające
Dostępne są dane dotyczące długotrwałego utrzymywania się przeciwciał po szczepieniu produktem Menveo przez okres do 5 lat (patrz punkty 4.4 i 5.1).
Menveo można podać jako dawkę przypominającą pacjentom, którzy wcześniej otrzymali szczepionkę podstawową Menveo, inną skoniugowaną szczepionkę przeciwko meningokokom lub nieskoniugowaną polisacharydową szczepionkę przeciwko meningokokom. Potrzebę i czas podania dawki przypominającej u osób wcześniej zaszczepionych preparatem Menveo należy określić zgodnie z zaleceniami krajowymi.
Populacja pediatryczna (w wieku poniżej 2 lat)
Bezpieczeństwo i skuteczność produktu Menveo u dzieci w wieku poniżej 2 lat nie zostały jeszcze ustalone.Obecnie dostępne dane opisano w punkcie 5.1, ale nie można sformułować zaleceń dotyczących dawkowania.
Sposób podawania
Menveo podaje się we wstrzyknięciu do mięśnia, najlepiej w mięsień naramienny.
Nie wolno go podawać donaczyniowo, podskórnie ani śródskórnie.
W celu podania więcej niż jednej szczepionki w tym samym czasie należy użyć oddzielnych miejsc wstrzyknięcia.
Instrukcja dotycząca przygotowania i rekonstytucji produktu leczniczego przed podaniem, patrz punkt 6.6.
04.3 Przeciwwskazania -
Nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1 lub na toksoid błoniczy (CRM197), lub zagrażająca życiu reakcja po uprzednim podaniu szczepionki zawierającej podobne składniki (patrz punkt 4.4).
Podobnie jak w przypadku innych szczepionek, podanie szczepionki Menveo należy odroczyć u pacjentów z ostrym, ciężkim epizodem gorączkowym. Obecność drobnej infekcji nie jest przeciwwskazaniem.
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania -
Przed wstrzyknięciem jakiejkolwiek szczepionki osoba odpowiedzialna za podanie musi podjąć wszelkie znane środki ostrożności, aby zapobiec reakcjom alergicznym lub innym reakcjom, w tym zebrać informacje na temat historii medycznej pacjenta i aktualnego stanu zdrowia. Podobnie jak w przypadku wszystkich szczepionek. łatwo dostępne w rzadkich przypadkach reakcji anafilaktycznych po podaniu szczepionki.
W związku ze szczepieniem mogą wystąpić reakcje lękowe, w tym reakcje wazowagalne (omdlenie), hiperwentylacja lub reakcje związane ze stresem, ponieważ w związku ze szczepieniem może wystąpić reakcja psychogenna na podanie igły (patrz punkt 4.8 Działania niepożądane). uniknąć omdlenia obrażeń.
Menveo w żadnym wypadku nie powinien być podawany donaczyniowo.
Menveo nie chroni przed zakażeniami wywołanymi przez żadną inną serogrupę N. meningitidis nie występuje w szczepionce.
Podobnie jak w przypadku wszystkich szczepionek, u wszystkich zaszczepionych może nie wystąpić ochronna odpowiedź immunologiczna (patrz punkt 5.1).
Badania z użyciem preparatu Menveo wykazały zmniejszenie miana przeciwciał bakteriobójczych w surowicy w porównaniu z serogrupą A podczas stosowania w teście ludzkiego dopełniacza (hSBA) (patrz punkt 5.1).
Kliniczne znaczenie zmniejszenia miana przeciwciał hSBA dla serogrupy A nie jest znane.
Konieczność podania dawki przypominającej należy rozważyć, jeśli uważa się, że dana osoba jest szczególnie narażona na ekspozycję na MenA i otrzymywała poprzednią dawkę Menveo przez ponad rok.
Brak danych dotyczących zastosowania szczepionki w profilaktyce poekspozycyjnej.
U osób z obniżoną odpornością szczepienie może nie wywołać odpowiedniej ochronnej odpowiedzi przeciwciał. Zakażenie ludzkim wirusem niedoboru odporności (HIV) nie jest przeciwwskazaniem, jednak Menveo nie było specjalnie oceniane u osób z obniżoną odpornością. Osoby z niedoborem dopełniacza oraz osoby z asplenią anatomiczną lub czynnościową mogą nie rozwinąć odpowiedzi immunologicznej na skoniugowane szczepionki przeciw meningokokom z grup A, C, W135 i Y.
Menveo nie był oceniany u osób z trombocytopenią, zaburzeniami hemostazy lub leczonych przeciwzakrzepowo ze względu na ryzyko wystąpienia krwiaka.. Personel medyczny powinien ocenić stosunek korzyści do ryzyka u osób z ryzykiem powstania krwiaka po wstrzyknięciu domięśniowym.
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji -
Menveo można podawać jednocześnie z którąkolwiek z następujących szczepionek: monowalentną i skojarzoną szczepionką przeciwko wirusowemu zapaleniu wątroby typu A i B, szczepionką przeciw żółtej febrze, szczepionką przeciw durowi brzusznemu (polisacharyd Vi), szczepionką przeciwko japońskiemu zapaleniu mózgu oraz szczepionką przeciw wściekliźnie.
U młodzieży (w wieku 11-18 lat) Menveo oceniano w dwóch badaniach dotyczących jednoczesnego stosowania wyłącznie adsorbowanej szczepionki przeciw krztuścowi tężcowi i krztuścowi (Tdap) lub
Tdap i czterowalentna szczepionka rekombinowana przeciwko wirusowi brodawczaka (typy 6, 11, 16 i 18) (HPV); oba badania popierają jednoczesne podawanie szczepionek.
Nie ma dowodów z badań na zwiększenie szybkości reaktogenności lub na zmianę profilu bezpieczeństwa szczepionek.Odpowiedź przeciwciał na Menveo i bezkomórkowe składniki szczepionki przeciw krztuścowi i tężcowi lub HPV nie była osłabiona przez jednoczesne podanie .
Podanie Menveo miesiąc po Tdap spowodowało statystycznie istotne zmniejszenie odpowiedzi serologicznych serogrupy W135. Ponieważ nie odnotowano bezpośredniego wpływu na wskaźnik seroprotekcji, konsekwencje kliniczne są obecnie nieznane. Były dowody na pewne tłumienie odpowiedzi przeciwciał na dwa z trzech antygenów krztuśca. Kliniczne znaczenie tej obserwacji nie jest znane.
Po szczepieniu ponad 97% osób miało wykrywalne miana krztuśca dla wszystkich trzech antygenów krztuśca.
U dzieci w wieku od 2 do 10 lat brak jest danych umożliwiających ocenę bezpieczeństwa i immunogenności innych szczepionek dla dzieci podawanych jednocześnie z Menveo.
Nie badano równoczesnego podawania Menveo i innych szczepionek innych niż wymienione powyżej. Szczepionki towarzyszące należy zawsze podawać w różne miejsca wstrzyknięcia, najlepiej w przeciwległe kończyny.Należy zbadać, czy jednoczesne podawanie może nasilać działania niepożądane.
Jeśli osoba zaszczepiona jest leczona immunosupresyjnie, odpowiedź immunologiczna może być zmniejszona.
04.6 Ciąża i karmienie piersią -
Nie ma wystarczających danych klinicznych dotyczących ekspozycji w ciąży.
Badania niekliniczne wykazują, że Menveo nie ma bezpośredniego ani pośredniego szkodliwego wpływu na ciążę, rozwój zarodka/płodu, przebieg porodu lub rozwój pourodzeniowy. Biorąc pod uwagę nasilenie inwazyjnej choroby meningokokowej wywołanej przez serogrupy A, C, W135 i Y Neisseria meningitidisciąża nie jest przeszkodą w szczepieniu, gdy ryzyko narażenia jest jasno określone.
Chociaż dane kliniczne dotyczące stosowania Menveo podczas karmienia piersią nie są kompletne, jest mało prawdopodobne, aby przeciwciała wydzielane do mleka stanowiły zagrożenie przy asymilacji przez karmione niemowlę. Dlatego Menveo można stosować podczas karmienia piersią.
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn -
Nie przeprowadzono badań nad zdolnością prowadzenia pojazdów i obsługiwania maszyn.Po szczepieniu zgłaszano bardzo rzadkie przypadki zawrotów głowy.Zdolność do prowadzenia pojazdów i obsługiwania maszyn może być przejściowo osłabiona.
04.8 Działania niepożądane -
W obrębie każdej klasy częstości działania niepożądane są zgłaszane w kolejności zmniejszającej się ciężkości.
Częstotliwość definiuje się w następujący sposób:
Bardzo często: (≥ 1/10)
Często: (≥1/100 do
Niezbyt często: (≥1/1000 do
Rzadko: (≥1/10 000 do
Bardzo rzadkie: (
Nieznana (częstość nie może być określona na podstawie dostępnych danych)
Działania niepożądane obserwowane w badaniach klinicznych
Dzieci w wieku od 2 do 10 lat
Łącznie 3464 pacjentów w wieku od 2 do 10 lat otrzymało szczepionkę Menveo w zakończonych badaniach klinicznych. Charakterystyka profilu bezpieczeństwa Menveo u dzieci w wieku od 2 do 10 lat jest oparta na danych z czterech badań klinicznych, w których 3181 pacjentów otrzymało Menveo.
Najczęstsze działania niepożądane podczas badań klinicznych trwały na ogół jeden lub dwa dni i nie były poważne. Działania niepożądane to:
Zaburzenia metabolizmu i odżywiania:
Często: zaburzenia odżywiania
Zaburzenia układu nerwowego:
Bardzo często: senność, ból głowy
Zaburzenia żołądkowo-jelitowe:
Często: nudności, wymioty, biegunka
Zaburzenia skóry i tkanki podskórnej:
Często: wysypka
Zaburzenia mięśniowo-szkieletowe i tkanki łącznej:
Często: bóle mięśni, bóle stawów
Zaburzenia ogólne i stany w miejscu podania:
Bardzo często: drażliwość, złe samopoczucie, ból w miejscu wstrzyknięcia, rumień w miejscu wstrzyknięcia (≤ 50 mm), stwardnienie w miejscu wstrzyknięcia (≤ 50 mm)
Często: rumień w miejscu wstrzyknięcia (>50 mm), stwardnienie w miejscu wstrzyknięcia (>50 mm), dreszcze, gorączka ≥38 °C
Niezbyt często: swędzenie w miejscu wstrzyknięcia
Osoby w wieku od 11 do 65 lat
Charakterystyka profilu bezpieczeństwa Menveo u młodzieży i dorosłych opiera się na danych z pięciu randomizowanych kontrolowanych badań obejmujących 6401 uczestników (w wieku od 11 do 65 lat), którzy otrzymali Menveo.
Menveo należało odpowiednio w odsetkach 58,9%, 16,4%, 21,3% i 3,4% do następujących grup wiekowych 11-18 lat, 19-34 lata, 35-55 lat i 56-65 lat. Dwa główne badania dotyczące bezpieczeństwa były randomizowanymi i aktywnie kontrolowanymi badaniami, do których włączono uczestników w wieku odpowiednio od 11 do 55 lat (N = 2663) oraz 19 i 55 lat (N = 1606).
Częstość występowania i nasilenie wszelkich reakcji miejscowych, ogólnoustrojowych i innych zasadniczo pokrywały się we wszystkich badaniach leczonych produktem Menveo oraz w grupach wiekowych młodzieży i dorosłych.Profil reaktogenności i odsetek zdarzeń niepożądanych u osób w wieku od 56 do 65 lat które otrzymały Menveo (N = 216) były podobne do tych obserwowanych u osób, które otrzymały Menveo w wieku od 11 do 55 lat.
Najczęstszymi ogólnoustrojowymi i miejscowymi działaniami niepożądanymi obserwowanymi w badaniach klinicznych były: ból w miejscu wstrzyknięcia i ból głowy.
Poniższa lista przedstawia działania niepożądane zgłoszone w trzech głównych badaniach klinicznych i dwóch badaniach pomocniczych, z podziałem na układy narządowe.Najczęstsze działania niepożądane zgłaszane podczas badań klinicznych zwykle trwały od jednego dnia do dwóch dni i były na ogół niepoważnie.
Zaburzenia układu nerwowego:
Bardzo często: ból głowy
Niezbyt często: zawroty głowy
Zaburzenia żołądkowo-jelitowe:
Bardzo często: nudności
Zaburzenia skóry i tkanki podskórnej:
Często: wysypka
Zaburzenia mięśniowo-szkieletowe i tkanki łącznej:
Bardzo często: bóle mięśni
Często: bóle stawów
Zaburzenia ogólne i stany w miejscu podania:
Bardzo często: ból w miejscu wstrzyknięcia, rumień w miejscu wstrzyknięcia (≤50 mm), stwardnienie w miejscu wstrzyknięcia (≤50 mm), złe samopoczucie
Często: rumień w miejscu wstrzyknięcia (>50 mm), stwardnienie w miejscu wstrzyknięcia (>50 mm), gorączka ≥38 °C, dreszcze
Niezbyt często: swędzenie w miejscu wstrzyknięcia
W grupie młodzieży bezpieczeństwo i tolerancja szczepionki były korzystne w odniesieniu do Tdap i nie zmieniały się istotnie po jednoczesnym podaniu lub kolejnych innych szczepionkach.
Doświadczenie postmarketingowe (wszystkie grupy wiekowe)
Zaburzenia układu odpornościowego
Nieznana: nadwrażliwość, w tym anafilaksja
Zaburzenia układu nerwowego
Częstość nieznana: drgawki toniczne, drgawki gorączkowe, omdlenia
Zaburzenia ucha i błędnika
Nieznane: zawroty głowy
Zaburzenia ogólne i stany w miejscu podania
Częstość nieznana: zapalenie tkanki łącznej w miejscu wstrzyknięcia, obrzęk w miejscu wstrzyknięcia, w tym rozległy obrzęk kończyny, w którą podano wstrzyknięcie
Zgłaszanie podejrzewanych działań niepożądanych
Zgłaszanie podejrzewanych działań niepożądanych występujących po dopuszczeniu produktu leczniczego do obrotu jest ważne, ponieważ umożliwia ciągłe monitorowanie stosunku korzyści do ryzyka produktu leczniczego. Osoby należące do fachowego personelu medycznego są proszone o zgłaszanie wszelkich podejrzewanych działań niepożądanych za pośrednictwem krajowego systemu zgłaszania. w „Załączniku V
04.9 Przedawkowanie -
Nie zgłoszono żadnych przypadków przedawkowania.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE -
05.1 "Właściwości farmakodynamiczne -
Grupa farmakoterapeutyczna: szczepionki przeciw meningokokom.
Kod ATC: J07AH08.
Immunogenność
Skuteczność preparatu Menveo wywnioskowano na podstawie pomiaru wytwarzania przeciwciał przeciwotoczkowych specyficznych dla grupy serologicznej o działaniu bakteriobójczym.Aktywność bakteriobójczą surowicy (SBA) mierzono przy użyciu surowicy ludzkiej jako źródła egzogennego dopełniacza (hSBA). HSBA był oryginalnym korelatem ochrony przed chorobą meningokokową.
Immunogenność oceniano w randomizowanych, wieloośrodkowych, aktywnie kontrolowanych badaniach klinicznych obejmujących dzieci (2-10 lat), młodzież (11-18 lat), dorosłych (19-55 lat) i osoby starsze (56-65 lat).
Immunogenność u dzieci w wieku od 2 do 10 lat
W głównym badaniu V59P20 immunogenność Menveo porównywano z ACWY-D: 1170 dzieci zostało zaszczepionych Menveo, a 1161 otrzymało szczepionkę porównawczą w populacjach zgodnych z protokołem.W dwóch uzupełniających badaniach V59P8 i V59P10 immunogenność Menveo porównywano z że z ACWY-PS.
W głównym, randomizowanym, zaślepionym badaniu V59P20, w którym uczestnicy byli stratyfikowani według wieku (2 do 5 lat i 6 do 10 lat), immunogenność pojedynczej dawki szczepionki Menveo, miesiąc później, została porównana z immunogennością pojedyncza dawka ACWY-D. Wyniki immunogenności miesiąc po szczepieniu szczepionką Menveo u osób w wieku od 2 do 5 i od 6 do 10 lat podsumowano w Tabeli 1.
Tabela 1: Odpowiedzi bakteriobójcze przeciwciał w surowicy po podaniu szczepionki Menveo miesiąc po szczepieniu u osób w wieku od 2 do 5 do 6 do 10 lat
W innym randomizowanym, zaślepionym badaniu (V59P8) dzieci w USA były szczepione pojedynczą dawką Menveo (n = 284) lub ACWY-PS (n = 285). stratyfikacją wiekową (2-5 i 6-10 lat), odpowiedzi immunologiczne mierzone jako odsetek osób z odpowiedzią serologiczną, hSBA≥1:8 i GMT nie tylko nie były gorsze od szczepionki porównawczej ACWY-PS, ale również wszystkie były statystycznie wyższy niż komparator dla wszystkich serogrup i wszystkich pomiarów odporności jeden miesiąc po szczepieniu Rok po szczepieniu Menveo pozostawał statystycznie lepszy od ACWY-PS dla serogrup A, W-135 i Y, mierzony jako odsetek osób z hSBA≥1 : 8 i GMT.
Menveo nie był gorszy dla tych punktów końcowych dla serogrupy C (tab. 2). Kliniczne znaczenie silniejszych odpowiedzi immunologicznych po szczepieniu nie jest znane.
Tabela 2: Immunogenność dawki szczepionki Menveo lub ACWY-PS u osób w wieku od 2 do 10 lat, mierzona miesiąc i dwanaście miesięcy po szczepieniu
W randomizowanym, zaślepionym badaniu (V59P10) przeprowadzonym w Argentynie dzieci szczepiono pojedynczą dawką Menveo (N = 949) lub ACWY-PS (N = 551).
Immunogenność oceniano w podgrupie 150 osób w każdej grupie zaszczepionej.
Odpowiedź immunologiczna obserwowana u dzieci w wieku od 2 do 10 lat była bardzo podobna do obserwowanej w badaniu V59P8 przedstawionym powyżej: odpowiedź immunologiczna na Menveo miesiąc po szczepieniu, mierzona jako odsetek osób z odpowiedzią serologiczną, hSBA ≥1: 8 i GMT, było to nie mniej niż ACWY-PS.
Przeprowadzono randomizowane, zaślepione badanie z udziałem obserwatora u dzieci w wieku od 12 do 59 miesięcy w Finlandii i Polsce (V59P7).Łącznie 199 pacjentów w wieku od 2 do 5 lat znalazło się w populacji zgodnej z protokołem pod kątem immunogenności preparatu Menveo i 81 osób w wieku od 3 do 5 lat tworzyła grupę ACWY-PS.
Miesiąc po pierwszym szczepieniu odsetek osób z hSBA ≥ 1: 8 był znacząco wyższy w grupie Menveo dla wszystkich czterech serogrup (63% vs 39%, 46% vs 39%, 78% vs 59% i 65% % vs 57% dla Menveo w porównaniu z ACWY-PS odpowiednio dla serogrup A, C, W135 i Y).
W randomizowanym, zaślepionym badaniu (V59_57) przeprowadzonym w Stanach Zjednoczonych porównywano immunogenność schematu dwudawkowego i jednodawkowego Menveo u dzieci w wieku od 2 do 5 do 6 do 10 lat. .
Na początku odsetek pacjentów z hSBA ≥ 1: 8 w dwóch stratyfikacjach wiekowych wynosił 1% -5% dla serogrupy A, 13% -28% dla serogrupy C, 42% -64% dla serogrupy W135 i 6% -19 % dla serogrupy Y. Miesiąc po ostatnim szczepieniu odsetek osób z hSBA ≥ 1:8 w grupie otrzymującej dwie dawki i w grupie otrzymującej pojedynczą dawkę w dwóch grupach wiekowych wynosił: 90% -95% vs 76% -80% dla serogrupy A, 98% -99% wobec 76% -87% dla serogrupy C, 99% wobec 93% -96% dla serogrupy W135 i 96% wobec 65% - 69% dla serogrupy Y. Miesiąc po szczepieniu , GMTs były wyższe w grupie dwudawkowej niż w grupie jednodawkowej w obu stratyfikacjach wiekowych, jednak różnica ta była mniej wyraźna w starszej stratyfikacji wiekowej.
Rok po ostatnim szczepieniu odsetek osób z hSBA ≥ 1:8 po leczeniu schematem dwudawkowym i schematem jednodawkowym był niższy niż odsetek odnotowany 1 miesiąc po szczepieniu (30% po schemacie dwudawkowym, 11 % -20% po schemacie pojedynczej dawki dla serogrupy A; 61% -81% i 41% -55% dla serogrupy C; 92% -94% i 90% -91% dla serogrupy W135; 67% -75% i 57 % -65% dla serogrupy Y) Rok po szczepieniu różnice między hSBA GMTs w grupie otrzymującej 2 dawki i pojedynczej dawki były mniejsze niż te stwierdzone 1 miesiąc po szczepieniu.
Korzyści kliniczne ze schematu 2-dawkowego u dzieci w wieku od 2 do 10 lat nie są znane.
Utrzymywanie się odpowiedzi immunologicznej i odpowiedź na dawkę przypominającą u starszych dzieci od 2 do 10 lat
Utrzymywanie się przeciwciał 5 lat po szczepieniu podstawowym oceniano w badaniu V59P20E1, będącym rozszerzeniem badania V59P20. Obserwowano utrzymywanie się przeciwciał przeciwko serogrupom C, W135 i Y. Odsetki osób z hSBA ≥1: 8 wynosiły 32% i 56% odpowiednio wobec serogrupy C u osób w wieku od 2 do 5 lat i od 6 do 10 lat, 74% i 80% wobec serogrupy W135 oraz 48% i 53% wobec serogrupy Y, z wartościami GMT wynoszącymi odpowiednio 6,5 i 12 dla serogrupy C, 19 i 26 dla serogrupy W135 i 8,13 oraz 10 dla serogrupy Y. W przypadku serogrupy A odpowiednio 14% i 22% pacjentów w wieku od 2 do 5 i od 6 do 10 lat zgłosiło hSBA ≥1: 8 (GMT 2,95 i 3,73).
Pięć lat po pierwszym szczepieniu pojedynczą dawką dzieciom podano również dawkę przypominającą Menveo. Wszyscy badani w obu grupach wiekowych wykazali hSBA ≥1: 8 dla wszystkich grup serologicznych, z mianami przeciwciał kilkakrotnie wyższymi niż te obserwowane po szczepieniu pierwotnym (Tabela 3).
Tabela 3: Utrzymywanie się odpowiedzi immunologicznej 5 lat po pierwszym szczepieniu szczepionką Menveo i odpowiedź immunologiczna 1 miesiąc po podaniu dawki przypominającej u osób w wieku 2 do 5 lat i 6 do 10 lat w momencie pierwszego szczepienia
Immunogenność u osób w wieku 11 lat lub starszych
W głównym badaniu (V59P13) młodzież lub dorośli otrzymali jedną dawkę szczepionki Menveo (n = 2649) lub szczepionki porównawczej ACWY-D (n = 875). Surowice pobrano przed szczepieniem i miesiąc po szczepieniu.
W innym badaniu (V59P6) przeprowadzonym u 524 nastolatków porównywano immunogenność Menveo z ACWY-PS.
Immunogenność u młodzieży
W populacji w wieku 11-18 lat w głównym badaniu V59P13 immunogenność pojedynczej dawki szczepionki Menveo miesiąc po szczepieniu została porównana z immunogennością szczepionki ACWY-D.
Wyniki immunogenności miesiąc po podaniu Menveo podsumowano poniżej w Tabeli 4.
Tabela 4: Bakteriobójcze przeciwciała w surowicy po podaniu szczepionki Menveo miesiąc po szczepieniu u osób w wieku od 11 do 18 lat
W podgrupie osób w wieku od 11 do 18 lat, które były seronegatywne na początku badania (hSBA
W badaniu non-inferiority V59P6 immunogenność oceniano u młodzieży w wieku 11-17 lat, która została przydzielona losowo do grupy otrzymującej Menveo lub ACWY-PS. C, W135 i Y) na podstawie odpowiedzi serologicznej, z odsetkami osiągającymi hSBA ≥1:8 i GMT.
Tabela 5: Immunogenność dawki szczepionki Menveo lub ACWY-PS u młodzieży, mierzona jeden miesiąc po szczepieniu
Rok po szczepieniu u tych samych osób, w porównaniu z ACWY-PS, wyższy odsetek osób zaszczepionych szczepionką Menveo miał hSBA ≥1:8 dla serogrup C, W135 i Y, przy porównywalnych poziomach dla serogrupy A. Podobne wyniki zaobserwowano. porównanie hSBA GMT.
Utrzymywanie się odpowiedzi immunologicznej i odpowiedź na dawkę przypominającą u młodzieży
W badaniu V59P13E1 utrzymywanie się odpowiedzi immunologicznej przeciwko serogrupom A, C, W135 i Y po 21 miesiącach, 3 latach i 5 latach po szczepieniu podstawowym oceniano u osób w wieku od 11 do 18 lat w momencie szczepienia. Odsetki osób z hSBA ≥1: 8 pozostawały stałe dla przeciwciał przeciwko serogrupom C, W135 i Y od 21 miesięcy do 5 lat po szczepieniu w grupie Menveo, podczas gdy odsetek przeciwciał przeciwko serogrupie A nieznacznie malał w czasie (Tabela 6). . 5 lat po szczepieniu pierwotnym istotnie wyższy odsetek osób z hSBA ≥1: 8 zaobserwowano w grupie Menveo w porównaniu z osobami, które nie otrzymały wcześniej szczepionki, we wszystkich czterech grupach serologicznych.
Tabela 6: Utrzymywanie się odpowiedzi immunologicznej po około 21 miesiącach, 3 i 5 latach po szczepieniu szczepionką Menveo (osoby w wieku od 11 do 18 lat w momencie szczepienia)
Dawkę przypominającą Menveo podano 3 lata po szczepieniu podstawowym preparatem Menveo lub ACWY-D. Obie grupy wykazały silną odpowiedź na dawkę przypominającą Menveo miesiąc po szczepieniu (100% badanych miało hSBA ≥1: 8 dla wszystkich serogrup) i ta odpowiedź utrzymywała się w dużej mierze przez 2 lata po podaniu dawki przypominającej dla serogrup C, W135 i Y (87% -100% badanych miało hSBA ≥1: 8 dla serogrup).
Odnotowano nieznaczny spadek odsetka osób z hSBA ≥1:8 dla serogrupy A, chociaż odsetek ten był nadal wysoki (77% -79%). Zgodnie z oczekiwaniami GMT z czasem spadły, ale pozostały od 2 do 8 razy wyższe niż wartości sprzed wzmocnienia (Tabela 8).
W badaniu V59P6E1 rok po szczepieniu odsetek osób, które otrzymały Menveo z hSBA ≥1: 8, pozostawał istotnie wyższy niż tych, które otrzymały ACWY-PS dla serogrup C, W135 i Y i podobnie między dwiema badanymi grupami dla serogrupy A. hSBA GMT dla serogrup W135 i Y były wyższe wśród osób, które otrzymały Menveo. 5 lat po szczepieniu odsetek osób, które otrzymały Menveo z hSBA ≥1: 8, pozostał znacząco wyższy niż tych, które otrzymały ACWY-PS dla serogrup C i Y. Wyższe wartości hSBA GMTs obserwowano dla serogrup W135 i Y (Tabela 7).
Tabela 7: Utrzymywanie się odpowiedzi immunologicznych około 12 miesięcy i 5 lat po szczepieniu szczepionką Menveo i ACWY-PS (osoby w wieku od 11 do 18 lat w momencie szczepienia)
Dawkę przypominającą Menveo podano 5 lat po szczepieniu podstawowym preparatem Menveo lub ACWY-PS. 7 dni po dawce przypominającej u 98% -100% pacjentów, którzy wcześniej otrzymywali Menveo i 73% -84% pacjentów, którzy wcześniej otrzymywali ACWY-PS, hSBA ≥1: 8 w porównaniu z serogrupami A, C, W135 i Y. Miesiąc później po szczepieniu odsetek osób z hSBA≥1:8 wynosił odpowiednio 98% -100% i 84% -96% 7 i 28 dni po podaniu dawki przypominającej nastąpił istotny wzrost wartości hSBA GMTs w stosunku do wszystkich czterech serogrup (tab. 8) .
Tabela 8: Odpowiedzi na dawkę przypominającą: Odpowiedź przeciwciał bakteriobójczych na dawkę przypominającą szczepionki Menveo podaną 3 i 5 lat po szczepieniu podstawowym szczepionką Menveo i ACWY-PS u osób w wieku od 11 do 17 lat
Immunogenność u dorosłych
W głównym badaniu immunogenności V59P13 odpowiedź immunologiczną na Menveo oceniano u osób dorosłych w wieku od 19 do 55 lat. Wyniki przedstawiono w Tabeli 9. W podgrupie osób w wieku od 19 do 55 lat, które były seronegatywne na początku badania, odsetek osób, które uzyskały hSBA ≥ 1:8 po dawce Menveo przedstawiały się następująco: serogrupa A 67% (582/875); serogrupa C 71% (401/563); serogrupa W135 82% (131/160); serogrupa Y 66% (173/263). ).
Tabela 9: Przeciwciała bakteriobójcze w surowicy po podaniu szczepionki Menveo miesiąc po szczepieniu u osób w wieku od 19 do 55 lat
W badaniu V59P6E1 oceniano pojawianie się odpowiedzi immunologicznej po szczepieniu podstawowym produktem Menveo u zdrowych osób w wieku 18-22 lat. 7 dni po szczepieniu u 64% osób wystąpiło hSBA ≥1: 8 przeciwko serogrupie A, a od 88% do 90% osób miało przeciwciała bakteriobójcze przeciwko serogrupom C, W135 i Y. Miesiąc po szczepieniu u 92% -98% osób hSBA ≥1: 8 przeciwko serogrupom A, C, W135 i Y. Obserwowano również silną odpowiedź immunologiczną mierzoną jako hSBA GMT przeciwko wszystkim serogrupom po 7 dniach (GMT od 34 do 70) oraz po 28 dniach (GMT od 79 do 127) po pojedyncza dawka szczepionki.
Immunogenność u osób starszych
Porównawczą immunogenność Menveo vs. ACWY-PS oceniano u osób w wieku od 56 do 65 lat w badaniu V59P17. Odsetek osób z hSBA ≥ 1:8 był nie mniejszy niż ACWY-PS dla wszystkich czterech serogrup i statystycznie lepszy dla serogrup A i Y (tabela 10).
Tabela 10: Immunogenność dawki szczepionki Menveo lub ACWY-PS u dorosłych w wieku od 56 do 65 lat, mierzona miesiąc po szczepieniu
Dostępne dane u dzieci w wieku 2-23 miesięcy
Immunogenność szczepionki Menveo u dzieci w wieku od 2 do 23 miesięcy była oceniana w kilku badaniach, chociaż miano hSBA większe niż 1:8 osiągnięto u dużego odsetka osób immunizowanych szczepionką Menveo w schemacie 4-dawkowym, przy niższych wskaźnikach uzyskane w badaniach z 2-dawkowym, jednodawkowym schematem, Menveo porównywano z inną szczepionką przeciwko meningokokom tylko w jednym głównym badaniu, w którym nie wykazano odpowiedzi co najmniej równoważnej do odpowiedzi na monowalentną skoniugowaną szczepionkę serogrupy C (po podaniu pojedynczej dawki 12 miesięcy). Obecnie dostępne dane są niewystarczające do ustalenia skuteczności Menveo u dzieci w wieku poniżej 2 lat Informacje dotyczące stosowania u dzieci, patrz punkt 4.2.
05.2 "Właściwości farmakokinetyczne -
Nieistotne.
05.3 Przedkliniczne dane o bezpieczeństwie -
Dane niekliniczne wynikające z konwencjonalnych badań toksyczności po podaniu wielokrotnym oraz toksycznego wpływu na reprodukcję i rozwój nie ujawniają żadnego szczególnego zagrożenia dla człowieka.
U zwierząt laboratoryjnych nie stwierdzono działań niepożądanych u szczepionych ciężarnych królików ani ich potomstwa do 29. dnia po urodzeniu.
Nie zaobserwowano wpływu na płodność samic królików, które otrzymywały Menveo przed kryciem iw czasie ciąży.
06.0 INFORMACJE FARMACEUTYCZNE -
06.1 Substancje pomocnicze -
Pył
Sacharoza
Fosforan potasu jednozasadowy
Rozwiązanie
Monohydrat jednozasadowego fosforanu sodu
Dwuwodny fosforan disodowy
Chlorek sodu
Woda do wstrzykiwań
06.2 Niezgodność "-
Tego produktu leczniczego nie wolno mieszać z innymi produktami leczniczymi oprócz wymienionych w punkcie 6.6.
06.3 Okres ważności "-
3 lata.
Produkt leczniczy należy zużyć natychmiast po rekonstytucji. Wykazano jednak stabilność fizykochemiczną przez 8 godzin po rekonstytucji w temperaturze poniżej 25°C.
06.4 Specjalne środki ostrożności przy przechowywaniu -
Przechowywać w lodówce (2°C - 8°C). Nie zamrażać.
Fiolki przechowywać w tekturowym pudełku, aby chronić lek przed światłem.
Warunki przechowywania produktu leczniczego po rekonstytucji, patrz punkt 6.3.
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania -
Proszek w fiolce (szkło typu I) z korkiem (guma halobutylowa) i roztwór w fiolce (szkło typu I) z korkiem (guma butylowa).
Wielkość opakowania to jedna dawka (2 fiolki) lub pięć dawek (10 fiolek).
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
06.6 Instrukcje użytkowania i obsługi -
Menveo należy przygotować do podania poprzez rozpuszczenie proszku (w fiolce) z roztworem (w fiolce).
Zawartość dwóch różnych fiolek (proszek MenA i roztwór MenCWY) należy wymieszać przed szczepieniem, aby uzyskać 1 dawkę 0,5 ml.
Składniki szczepionki należy sprawdzić wzrokowo przed i po rekonstytucji.
Za pomocą strzykawki i odpowiedniej igły (21G, długość 40 mm lub 21G, długość 1½") pobrać całą zawartość fiolki z roztworem i wstrzyknąć ją do fiolki z proszkiem w celu odtworzenia skoniugowanego składnika MenA.
Odwrócić fiolkę i energicznie wstrząsnąć, a następnie pobrać 0,5 ml zrekonstytuowanego produktu. Należy zauważyć, że niewielka ilość płynu pozostaje we fiolce po pobraniu dawki.
Po rekonstytucji szczepionka jest przezroczystym, bezbarwnym do jasnożółtego roztworem, wolnym od widocznych ciał obcych. W przypadku zaobserwowania jakichkolwiek obcych cząstek stałych i (lub) zmiany wyglądu fizycznego, szczepionkę należy wyrzucić.
Przed wstrzyknięciem wymienić igłę na odpowiednią do podania szczepionki. Przed wstrzyknięciem szczepionki sprawdzić, czy w strzykawce nie ma pęcherzyków powietrza.
Niewykorzystany lek i odpady pochodzące z tego leku należy usunąć zgodnie z lokalnymi przepisami.
07.0 POSIADACZ „POZWOLENIA NA DOPUSZCZENIE DO OBROTU” -
Szczepionki GSK S.r.l.
Via Fiorentina 1
53100 Siena, Włochy
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU -
UE / 1/10/614/002
039766023
UE / 1/10/614/003
039766035
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA -
Data pierwszego zezwolenia: 15 marca 2010 r.
Data ostatniego przedłużenia: 4 grudnia 2014 r.