Składniki aktywne: Walacyklowir
Valtrex 250 mg tabletki powlekane
Valtrex 500 mg tabletki powlekane
Valtrex 1000 mg tabletki powlekane
Dlaczego stosuje się Valtrex? Po co to jest?
Valtrex należy do grupy leków zwanych lekami przeciwwirusowymi. Działa poprzez zabijanie lub zatrzymanie wzrostu wirusów zwanych herpes simplex (HSV), ospy wietrznej półpaśca (VZV) i cytomegalowirusa (CMV).
Valtrex może być używany do:
- leczyć półpasiec (u dorosłych)
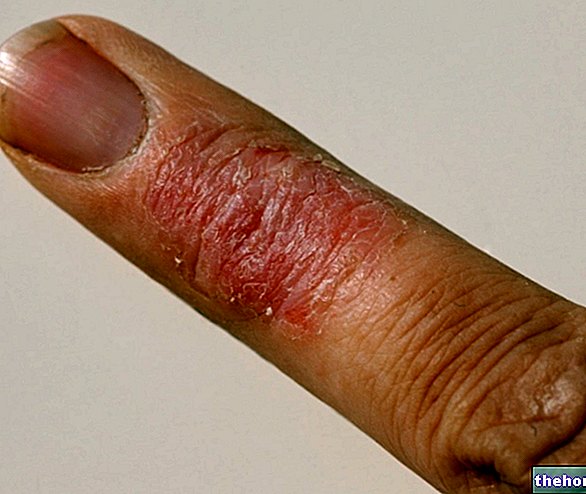
- w leczeniu zakażeń skóry i opryszczki narządów płciowych HSV (u dorosłych i młodzieży w wieku powyżej 12 lat) Jest również stosowany w zapobieganiu nawrotom tych zakażeń.
- leczyć opryszczkę wargową (u dorosłych i młodzieży powyżej 12 roku życia)
- zapobiegać zakażeniom CMV po przeszczepieniu narządów (u dorosłych i młodzieży powyżej 12 roku życia)
- leczyć i zapobiegać nawracającym infekcjom oka HSV (u dorosłych i młodzieży w wieku powyżej 12 lat).
Przeciwwskazania Kiedy nie należy stosować preparatu Valtrex
Nie należy przyjmować leku Valtrex
- Jeśli pacjent ma uczulenie na walacyklowir lub acyklowir lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6).
- Nie należy przyjmować leku Valtrex, jeśli powyższe dotyczy pacjenta. W razie wątpliwości należy porozmawiać z lekarzem lub farmaceutą przed zastosowaniem leku Valtrex.
Środki ostrożności dotyczące stosowania Informacje ważne przed zastosowaniem leku Valtrex
Przed rozpoczęciem stosowania leku Valtrex należy porozmawiać z lekarzem lub farmaceutą, jeśli:
- masz problemy z nerkami
- masz problemy z wątrobą
- ma ponad 65 lat
- jego układ odpornościowy jest słaby
Jeśli nie masz pewności, czy powyższe odnosi się do Ciebie, porozmawiaj z lekarzem lub farmaceutą przed zastosowaniem leku Valtrex.
Aby zapobiec przenoszeniu opryszczki narządów płciowych na inne osoby
Jeśli pacjent przyjmuje Valtrex w celu leczenia lub zapobiegania opryszczce narządów płciowych lub jeśli w przeszłości chorował na opryszczkę narządów płciowych, należy odbyć bezpieczny stosunek seksualny, w tym prezerwatywy, co jest ważne, aby zapobiec przeniesieniu zakażenia na inne osoby. Nie powinieneś uprawiać seksu, jeśli masz ból lub pęcherze na genitaliach.
Interakcje Jakie leki lub pokarmy mogą zmienić działanie Valtrex?
Należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent przyjmuje lub ostatnio przyjmował jakiekolwiek inne leki, w tym leki wydawane bez recepty i leki ziołowe.
Należy powiedzieć lekarzowi lub farmaceucie o przyjmowaniu jakichkolwiek innych leków wpływających na nerki. Należą do nich: aminoglikozydy, związki platyny, jodowane środki kontrastowe, metotreksat, pentamidyna, foskarnet, cyklosporyna, takrolimus, cymetydyna i probenecyd.
Zawsze należy powiedzieć lekarzowi lub farmaceucie o wszelkich innych lekach podczas przyjmowania leku Valtrex w leczeniu półpaśca lub po przeszczepieniu narządu.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
Ciąża i karmienie piersią
Generalnie nie zaleca się stosowania leku Valtrex w czasie ciąży.Jeśli jesteś w ciąży, lub podejrzewasz, że może być lub planujesz zajść w ciążę, nie zażywaj Valtrex bez konsultacji z lekarzem.Lekarz oceni korzyści dla Ciebie i ryzyko dla dziecka związane z przyjmowaniem leku Valtrex podczas ciąży lub karmienia piersią.
Prowadzenie i używanie maszyn
Valtrex może powodować działania niepożądane, które wpływają na zdolność prowadzenia pojazdów. Nie należy prowadzić pojazdów ani obsługiwać maszyn, chyba że jesteś pewien, że nie zostanie to naruszone.
Dawka, metoda i czas podawania Jak stosować Valtrex: dawkowanie
Lek należy zawsze stosować zgodnie z zaleceniami lekarza. W razie wątpliwości skonsultuj się z lekarzem lub farmaceutą.
Dawka, którą musisz przyjąć, będzie zależeć od tego, dlaczego lekarz przepisał Ci Valtrex. Twój lekarz omówi to z Tobą.
Leczenie „półpaśca (ogień św. Antoniego)”
- Zazwyczaj stosowana dawka to 1000 mg (jedna tabletka 1000 mg lub dwie tabletki 500 mg) trzy razy na dobę.
- Musisz przyjmować Valtrex przez siedem dni.
Leczenie opryszczki
- Zalecana dawka to 2000 mg (dwie tabletki 1000 mg lub cztery tabletki 500 mg) dwa razy na dobę.
- Drugą dawkę należy przyjąć 12 godzin (nie wcześniej niż 6 godzin) po pierwszej dawce
- Valtrex należy przyjmować tylko przez jeden dzień (dwie dawki).
Leczenie infekcji HSV skóry i opryszczki narządów płciowych
- Zalecana dawka to 500 mg (jedna tabletka 500 mg lub dwie tabletki 250 mg) dwa razy na dobę.
- W przypadku pierwszej infekcji należy przyjmować Valtrex przez pięć dni lub do dziesięciu dni, jeśli tak zaleci lekarz. W przypadku nawracających infekcji czas leczenia wynosi zwykle od 3 do 5 dni.
Aby zapobiec nawrotom infekcji HSV po ich wystąpieniu
- Zalecana dawka to jedna tabletka 500 mg raz na dobę.
- Dla niektórych osób z częstymi nawracającymi infekcjami korzystne jest przyjmowanie jednej tabletki 250 mg dwa razy dziennie.
- Należy przyjmować Valtrex, dopóki lekarz nie zaleci przerwania leczenia.
Aby zapobiec zakażeniu CMV (Cytomegalovirus)
- Zalecana dawka to 2000 mg (dwie tabletki 1000 mg lub cztery tabletki 500 mg) cztery razy dziennie.
- Każdą dawkę należy przyjmować w odstępie około 6 godzin.
- Zwykle zaczniesz przyjmować Valtrex tak szybko, jak to możliwe po operacji.
- Będziesz musiał zażywać Valtrex przez około 90 dni po operacji, dopóki lekarz nie zaleci jej przerwania.
Lekarz może zmienić dawkę leku Valtrex, jeśli:
- ma ponad 65 lat
- ma słaby układ odpornościowy
- mają problemy z nerkami.
Należy poinformować lekarza przed przyjęciem leku Valtrex, jeśli którakolwiek z sytuacji wymienionych powyżej dotyczy pacjenta.
Przyjmowanie leku
- Lek należy przyjmować doustnie.
- Tabletki połykać w całości popijając wodą.
- Lek Valtrex należy przyjmować o tej samej porze każdego dnia.
- Lek Valtrex należy przyjmować zgodnie z zaleceniami lekarza lub farmaceuty.
Osoby powyżej 65 roku życia lub z problemami z nerkami
Podczas przyjmowania leku Valtrex bardzo ważne jest regularne picie wody w ciągu dnia. Pomoże to zmniejszyć niepożądane skutki, które mogą wpływać na nerki lub układ nerwowy. Lekarz będzie uważnie monitorował objawy tych efektów. Działania niepożądane ze strony układu nerwowego mogą obejmować uczucie splątania lub pobudzenia, niezwykłe uczucie senności lub drętwienia.
Przedawkowanie Co zrobić w przypadku przyjęcia zbyt dużej dawki leku Valtrex
Przyjęcie większej niż zalecana dawki leku Valtrex
Valtrex zwykle nie jest szkodliwy, chyba że bierzesz za dużo i przez kilka dni. W przypadku zażycia zbyt wielu tabletek mogą wystąpić nudności, wymioty, problemy z nerkami, splątanie, pobudzenie lub uczucie mniejszej świadomości, zobaczenie rzeczy, których nie ma lub utrata przytomności. Należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent przyjął zbyt dużą dawkę leku Valtrex. Zabierz ze sobą opakowanie leku.
Pominięcie przyjęcia leku Valtrex
- Jeśli zapomnisz wziąć Valtrex, zażyj go tak szybko, jak sobie przypomnisz. Jeśli jednak zbliża się pora przyjęcia następnej dawki, pomiń pominiętą dawkę.
- Nie należy stosować dawki podwójnej w celu uzupełnienia pominiętej dawki.
Skutki uboczne Jakie są skutki uboczne Valtrex?
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią. Podczas stosowania tego leku mogą wystąpić następujące działania niepożądane:
Warunki, na które należy zwrócić uwagę
- ciężkie reakcje alergiczne (anafilaksja). Są to rzadkie u osób przyjmujących Valtrex. Szybki rozwój objawów, do których należą:
- zaczerwienienie, swędząca wysypka
- obrzęk warg, twarzy, szyi i gardła powodujący trudności w oddychaniu (obrzęk naczynioruchowy)
- nagły spadek ciśnienia krwi prowadzący do zapaści.
W przypadku wystąpienia reakcji alergicznej należy przerwać stosowanie leku Valtrex i natychmiast skontaktować się z lekarzem.
Bardzo często (może dotyczyć więcej niż 1 na 10 osób):
- bół głowy
Często (mogą dotyczyć do 1 na 10 osób):
- mdłości
- zawroty głowy
- On wymiotował
- biegunka
- reakcja skórna po ekspozycji na światło słoneczne (światłoczułość)
- wysypka
- swędzenie
Niezbyt często (może dotyczyć nie więcej niż 1 na 100 osób):
- stan zamętu
- widzenie lub słyszenie rzeczy, których nie ma (omamy)
- stan silnego odrętwienia
- drżenia
- stan wzburzenia
Te działania niepożądane ze strony układu nerwowego zwykle występują u osób z problemami z nerkami, osób starszych lub pacjentów po przeszczepieniu narządów, którzy przyjmują duże dawki Valtrexu dziennie, 8 gramów lub więcej.Skutki te zwykle ustępują po zatrzymaniu lub przyjęciu Valtrexu.
Inne niezbyt częste działania niepożądane:
- duszność (duszność)
- niestrawność
- wysypka, czasami swędzenie, pokrzywka
- ból w dolnej części pleców (ból nerek)
- krew w moczu (krwiomocz)
Niezbyt częste działania niepożądane, które mogą ujawnić się w badaniach krwi:
- zmniejszona liczba białych krwinek (leukopenia)
- zmniejszenie liczby płytek krwi, które są komórkami niezbędnymi do krzepnięcia (małopłytkowość)
- wzrost substancji wytwarzanych przez wątrobę.
Rzadko (może dotyczyć do 1 na 1000 osób):
- niestabilność w chodzeniu i brak koordynacji (ataksja)
- słowa wypowiadane w sposób powolny i wadliwy (dyzartria)
- konwulsje
- upośledzona funkcja mózgu (encefalopatia)
- utrata przytomności (śpiączka)
- zdezorientowane lub zaburzone myślenie (delirium)
Te działania niepożądane ze strony układu nerwowego zwykle występują u osób z problemami z nerkami, osób starszych lub pacjentów po przeszczepieniu narządów, którzy przyjmują duże dawki Valtrexu dziennie, 8 gramów lub więcej.Skutki te zwykle ustępują po zatrzymaniu lub przyjęciu Valtrexu.
Inne rzadkie skutki uboczne
- problemy z nerkami z niewielkim lub brakiem oddawania moczu.
Zgłaszanie skutków ubocznych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe działania niepożądane niewymienione w tej ulotce, należy porozmawiać z lekarzem lub farmaceutą. Działania niepożądane można również zgłaszać bezpośrednio za pośrednictwem systemu zgłaszania na stronie https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse Zgłaszanie działań niepożądanych może pomóc w uzyskaniu dodatkowych informacji na temat bezpieczeństwa stosowania tego leku.
Wygaśnięcie i przechowywanie
- Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
- Nie stosować tego leku po upływie terminu ważności zamieszczonego na pudełku. Data ważności (EXP) odnosi się do ostatniego dnia tego miesiąca.
- Przechowywać w temperaturze poniżej 30°C.
- Nie należy wyrzucać żadnych leków do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa.Pomoże to chronić środowisko.
Skład i postać farmaceutyczna
Co zawiera Valtrex
- Substancją czynną jest walacyklowir. Każda tabletka zawiera 250 mg, 500 mg lub 1000 mg walacyklowiru (w postaci chlorowodorku walacyklowiru).
Pozostałe składniki to:
Rdzeń tabletu
Celuloza mikrokrystaliczna
Krospowidon
Powidon
Stearynian magnezu
Bezwodna krzemionka koloidalna
Powłoka
Hypromeloza
Dwutlenek tytanu
Makrogol 400
Polisorbat 80 (tylko dla tabletek 500 mg i 1000 mg)
Wosk Carnauba
Jak wygląda Valtrex i co zawiera opakowanie
Tabletki Valtrex są pakowane w blistry z polichlorku winylu/aluminium.
Tabletki Valtrex 250 mg są dostarczane w opakowaniach zawierających 20 lub 60 tabletek powlekanych. Są koloru białego i oznaczone „GX CE7” z jednej strony.
Tabletki Valtrex 500 mg są dostarczane w opakowaniach zawierających 10, 24, 30, 42, 90 lub 112 tabletek powlekanych. Są koloru białego i oznaczone „GX CF1” z jednej strony.
Tabletki Valtrex 1000 mg są dostarczane w opakowaniach zawierających 21 tabletek powlekanych. Są koloru białego i oznaczone „GX CF2” z jednej strony.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO
TABLETKI ZELITREX POWLEKANE FOLIĄ
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY
Każda tabletka zawiera chlorowodorek walacyklowiru w ilości odpowiadającej 250 mg walacyklowiru.
Każda tabletka zawiera chlorowodorek walacyklowiru w ilości odpowiadającej 500 mg walacyklowiru.
Każda tabletka zawiera chlorowodorek walacyklowiru w ilości odpowiadającej 1000 mg walacyklowiru.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
03.0 POSTAĆ FARMACEUTYCZNA
Tabletka powlekana
250 mg tabletka
Biała, podłużna, obustronnie wypukła tabletka z białym lub ciemnobiałym rdzeniem z wytłoczonym napisem „GX CE7” po jednej stronie.
Tabletka 500 mg
Biała, podłużna, dwuwypukła tabletka z białym lub ciemnobiałym rdzeniem z wytłoczonym napisem „GX CF 1” po jednej stronie.
Tabletka 1000 mg
Biała, podłużna, obustronnie wypukła tabletka z białym lub ciemnobiałym rdzeniem z częściową linią podziału po obu stronach iz wytłoczonym napisem „GX CF2” po jednej stronie.
04.0 INFORMACJE KLINICZNE
04.1 Wskazania terapeutyczne
Zakażenia wirusem Varicella zoster (VZV) - półpasiec
Valtrex jest wskazany w leczeniu półpaśca i półpaśca ocznego u osób dorosłych z prawidłową odpornością (patrz punkt 4.4).
Valtrex jest wskazany w leczeniu półpaśca u dorosłych pacjentów z łagodną lub umiarkowaną immunosupresją (patrz punkt 4.4).
Zakażenia wirusem opryszczki pospolitej (HSV)
Wskazany jest Valtrex
• do leczenia i tłumienia infekcji HSV skóry i błon śluzowych, które obejmują:
- leczenie pierwszego epizodu opryszczki narządów płciowych u dorosłych i młodzieży z prawidłową odpornością oraz u osób dorosłych z obniżoną odpornością
- leczenie nawracających zakażeń wirusem opryszczki narządów płciowych u osób dorosłych i młodzieży z prawidłową odpornością oraz osób dorosłych z obniżoną odpornością
- tłumienie nawrotów opryszczki narządów płciowych u dorosłych i młodzieży z prawidłową odpornością oraz osób dorosłych z obniżoną odpornością
• w leczeniu i zwalczaniu nawracających zakażeń oka wywołanych przez wirus HSV (patrz punkt 4.4).
Nie przeprowadzono badań klinicznych u pacjentów zakażonych wirusem HSV, którzy mają obniżoną odporność z przyczyn innych niż zakażenie wirusem HIV (patrz punkt 5.1).
Zakażenia wirusem cytomegalii (CMV)
Valtrex jest wskazany w profilaktyce zakażenia i choroby CMV po przeszczepieniu narządu litego u dorosłych i młodzieży (patrz punkt 4.4).
04.2 Dawkowanie i sposób podawania
Zakażenia wirusem Varicella zoster (VZV) - półpasiec i półpasiec oczny
Pacjentom należy zalecić jak najszybsze rozpoczęcie leczenia po rozpoznaniu półpaśca. Brak danych dotyczących leczenia rozpoczętego po upływie 72 godzin od wystąpienia półpaśca.
Dorośli immunokompetentni
Dawka u pacjentów z prawidłową odpornością wynosi 1000 mg trzy razy dziennie przez siedem dni (całkowita dawka dobowa 3000 mg). Dawkę tę należy zmniejszyć na podstawie klirensu kreatyniny (patrz poniżej Zaburzenia czynności nerek).
Dorośli z obniżoną odpornością
Dawka u pacjentów z obniżoną odpornością wynosi 1000 mg trzy razy na dobę przez co najmniej siedem dni (całkowita dawka dobowa 3000 mg) i przez 2 dni po zaskorupianiu zmian.
Dawkę tę należy zmniejszyć na podstawie klirensu kreatyniny (patrz poniżej Zaburzenia czynności nerek).
U pacjentów z obniżoną odpornością leczenie przeciwwirusowe jest zalecane u pacjentów, u których pojawiają się pęcherze w ciągu jednego tygodnia lub w dowolnym momencie przed pojawieniem się strupów.
Leczenie zakażeń wirusem opryszczki pospolitej (HSV) u dorosłych i młodzieży (≥ 12 lat)
Dorośli i młodzież z prawidłową odpornością (≥ 12 lat)
Dawka wynosi 500 mg preparatu Valtrex, przyjmowana dwa razy na dobę (całkowita dawka dobowa 1000 mg). Dawkę tę należy zmniejszyć na podstawie klirensu kreatyniny (patrz poniżej Zaburzenia czynności nerek).
W nawracających epizodach leczenie powinno trwać od trzech do czterech dni. W przypadku początkowych epizodów, które mogą być cięższe, leczenie może wymagać przedłużenia do dziesięciu dni. Terapia powinna rozpocząć się jak najszybciej. W przypadku nawracających epizodów opryszczki pospolitej, leczenie najlepiej rozpocząć w fazie prodromalnej lub natychmiast po pojawieniu się pierwszych objawów przedmiotowych lub podmiotowych.Valtrex może zapobiegać rozwojowi zmian, jeśli zostanie przyjęty przy pierwszych oznakach i objawach nawracającej infekcji HSV.
Opryszczka
W przypadku opryszczki, skutecznym leczeniem u dorosłych i młodzieży jest walacyklowir w dawce 2000 mg dwa razy na dobę przez jeden dzień. Drugą dawkę należy przyjąć około 12 godzin (nie wcześniej niż 6 godzin) po pierwszej dawce. Należy ją zmniejszyć na podstawie klirensu kreatyniny ( patrz Niewydolność nerek poniżej).
W przypadku stosowania tego schematu dawkowania leczenie nie powinno przekraczać jednego dnia, ponieważ nie wykazano, aby zapewniało to „dodatkowe korzyści kliniczne. Leczenie należy rozpocząć przy pierwszych objawach opryszczki (np. mrowienie, swędzenie lub pieczenie).”.
Dorośli z obniżoną odpornością
W leczeniu HSV u osób dorosłych z obniżoną odpornością dawka wynosi 1000 mg dwa razy na dobę przez co najmniej 5 dni, po ocenie ciężkości stanu klinicznego i stanu immunologicznego pacjenta. do dziesięciu dni. Dawkowanie należy rozpocząć tak szybko, jak to możliwe. Dawkę tę należy zmniejszyć na podstawie klirensu kreatyniny (patrz poniżej Zaburzenia czynności nerek). W celu uzyskania maksymalnej korzyści klinicznej leczenie należy rozpocząć w ciągu 48 godzin. Zaleca się ścisłe monitorowanie rozwoju zmian.
Tłumienie nawracających zakażeń wirusem opryszczki pospolitej (HSI) u dorosłych i młodzieży (≥ 12 lat)
Dorośli i młodzież z prawidłową odpornością (≥ 12 lat)
Dawka wynosi 500 mg Valtrex do przyjmowania raz na dobę. Niektórzy pacjenci z bardzo częstymi epizodami nawrotów (≥10/rok w przypadku braku leczenia) mogą odnieść większe korzyści z przyjmowania dawki dobowej 500 mg podzielonej na dwie dawki (250 mg dwa razy na dobę).Tę dawkę należy zmniejszyć na podstawie klirensu kreatyniny (patrz poniżej Zaburzenia czynności nerek) Leczenie należy ponownie ocenić po 6-12 miesiącach leczenia.
Dorośli z obniżoną odpornością
Dawka wynosi 500 mg Valtrexu dwa razy dziennie. Dawkę tę należy zmniejszyć na podstawie klirensu kreatyniny (patrz poniżej Zaburzenia czynności nerek). Leczenie należy ponownie ocenić po 6-12 miesiącach terapii.
Profilaktyka zakażenia i choroby wirusem cytomegalii (CMI) u dorosłych i młodzieży (≥ 12 lat)
Dawkowanie preparatu Valtrex wynosi 2000 mg cztery razy dziennie, aby rozpocząć jak najszybciej po przeszczepie. Dawkę tę należy zmniejszyć na podstawie klirensu kreatyniny (patrz poniżej Zaburzenia czynności nerek).
Czas trwania leczenia wynosi zazwyczaj 90 dni, ale u pacjentów wysokiego ryzyka może być konieczne jego przedłużenie.
Populacje specjalne
Dzieci
Nie oceniano skuteczności preparatu Valtrex u dzieci w wieku poniżej 12 lat.
Starsi mieszkańcy
U osób w podeszłym wieku należy wziąć pod uwagę możliwość wystąpienia niewydolności nerek i odpowiednio dostosować dawkę (patrz Niewydolność nerek poniżej). Należy utrzymywać odpowiednie nawodnienie.
Niewydolność nerek
Zaleca się ostrożność podczas podawania preparatu Valtrex pacjentom z zaburzeniami czynności nerek. Należy utrzymywać odpowiednie nawodnienie.Dawkę preparatu Valtrex należy zmniejszyć u pacjentów z zaburzeniami czynności nerek, jak pokazano w Tabeli 1 poniżej.
U pacjentów poddawanych przerywanej hemodializie dawka preparatu Valtrex powinna być podana po przeprowadzeniu hemodializy.Klirens kreatyniny należy często monitorować, zwłaszcza w okresach, gdy czynność nerek zmienia się gwałtownie, na przykład bezpośrednio po przeszczepieniu nerki lub jej wszczepieniu. odpowiednio dostosowane.
Niewydolność wątroby
Badania przeprowadzone z zastosowaniem dawki 1000 mg walacyklowiru u dorosłych pacjentów wykazały, że u pacjentów z lekką lub umiarkowaną marskością wątroby nie jest wymagana modyfikacja dawki (utrzymana funkcja syntezy wątroby). Dane farmakokinetyczne u dorosłych pacjentów z zaawansowaną marskością wątroby (upośledzona funkcja syntezy wątrobowej i dowody)
przecieku wrotno-systemowego) nie wskazują na potrzebę modyfikacji dawki; jednak doświadczenie kliniczne jest ograniczone.W przypadku większych dawek (4000 mg lub więcej na dobę) patrz punkt 4.4.
Tabela 1: KOREKTA DAWKOWANIA W „NIEWYDOLNOŚCI NEREK
a W przypadku pacjentów poddawanych hemodializie przerywanej dawkę należy podawać po dializie w dni dializy.
bW przypadku supresji HSV u osób immunokompetentnych z wywiadem nawrotów w ciągu roku ≥10 lepsze wyniki można uzyskać podając 250 mg dwa razy na dobę.
04.3 Przeciwwskazania
Nadwrażliwość na walacyklowir lub acyklowir lub na którąkolwiek substancję pomocniczą (patrz punkt 6.1).
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania
Stan nawodnienia
Należy zadbać o to, aby pacjenci zagrożeni odwodnieniem, zwłaszcza w podeszłym wieku, otrzymywali odpowiednią ilość płynów.
Stosowanie u pacjentów z niewydolnością nerek i pacjentów w podeszłym wieku
Acyklowir jest eliminowany przez klirens nerkowy, dlatego dawkę walacyklowiru należy zmniejszyć u pacjentów z niewydolnością nerek (patrz punkt 4.2). Pacjenci w podeszłym wieku mogą mieć zaburzenia czynności nerek, dlatego w tej grupie pacjentów należy rozważyć konieczność zmniejszenia dawki. Zarówno pacjenci w podeszłym wieku, jak i pacjenci z niewydolnością nerek są narażeni na zwiększone ryzyko wystąpienia neurologicznych działań niepożądanych i powinni być uważnie obserwowani pod kątem tych działań. W zgłoszonych raportach reakcje te były na ogół odwracalne po przerwaniu leczenia (patrz punkt 4.8).
Stosowanie większych dawek walacyklowiru w niewydolności wątroby i przeszczepieniu wątroby
Brak danych dotyczących stosowania większych dawek walacyklowiru (4000 mg lub więcej na dobę) u pacjentów z chorobami wątroby.Nie przeprowadzono specjalnych badań z zastosowaniem walacyklowiru w przeszczepieniu wątroby i dlatego należy zachować ostrożność przy podawaniu dawek dobowych większych niż 4000 mg tym pacjentom.
Użyj do leczenia półpaśca
Odpowiedź kliniczna musi być ściśle monitorowana, zwłaszcza u pacjentów z obniżoną odpornością. Należy rozważyć dożylne leczenie przeciwwirusowe, jeśli odpowiedź na terapię doustną zostanie uznana za niewystarczającą.
Pacjenci z powikłanym półpaścem, np. z zajęciem narządów trzewnych, rozsianym półpaścem, neuropatią ruchową, zapaleniem mózgu i powikłaniami naczyniowo-mózgowymi, powinni być leczeni dożylną terapią przeciwwirusową.
Ponadto pacjenci z obniżoną odpornością z półpaścem ocznym lub z wysokim ryzykiem rozsiewu choroby i zajęcia narządów trzewnych powinni być leczeni dożylną terapią przeciwwirusową.
Przenoszenie opryszczki narządów płciowych
Pacjentom należy zalecić, aby unikali współżycia w przypadku wystąpienia objawów, nawet jeśli rozpoczęto leczenie lekiem przeciwwirusowym. Podczas leczenia supresyjnego środkiem przeciwwirusowym częstość wydalania wirusa jest znacznie zmniejszona. Jednak ryzyko transmisji jest nadal możliwe. Dlatego też, oprócz terapii walacyklowirem, zaleca się, aby pacjent odbywał bezpieczny stosunek płciowy.
Stosowanie w zakażeniach oczu HSV
U tych pacjentów odpowiedź kliniczna musi być ściśle monitorowana. Należy rozważyć dożylne leczenie przeciwwirusowe, jeśli odpowiedź na terapię doustną zostanie uznana za niewystarczającą.
Stosowanie w zakażeniach CMV
Dane dotyczące skuteczności walacyklowiru u pacjentów po przeszczepieniu (≥ 200) z wysokim ryzykiem choroby CMV (np. dawca CMV-dodatni / biorca CMV-ujemny lub zastosowanie terapii indukcyjnej globuliną antytymocytową) wskazują, że walacyklowir należy stosować tylko w tych pacjentów, u których problemy z tolerancją wykluczają stosowanie walgancyklowiru lub gancyklowiru.
Duża dawka walacyklowiru wymagana w profilaktyce CMV może powodować częstsze występowanie działań niepożądanych, w tym zaburzeń ośrodkowego układu nerwowego, niż obserwowane po niższych dawkach podawanych w innych wskazaniach (patrz punkt 4.8). Pacjentów należy ściśle monitorować. funkcję i dawkę odpowiednio dostosować (patrz punkt 4.2).
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji
Jednoczesne podawanie walacyklowiru z nefrotoksycznymi produktami leczniczymi należy prowadzić z ostrożnością, zwłaszcza u osób z zaburzeniami czynności nerek i wymaga regularnego monitorowania czynności nerek. Dotyczy to jednoczesnego podawania aminoglikozydów, związków platyny, jodowych środków kontrastowych, metotreksatu, pentamidyny, foskarnetu, cyklosporyny i trakolimusu.
Acyklowir jest wydalany w postaci niezmienionej głównie z moczem poprzez aktywne wydzielanie w kanalikach nerkowych. Po podaniu 1000 mg walacyklowiru cymetydyna i probenecyd zmniejszają klirens nerkowy acyklowiru i zwiększają AUC acyklowiru odpowiednio o około 25% i 45%, hamując czynne wydzielanie acyklowiru przez nerki. Cymetydyna i probenecyd przyjmowane razem z walacyklowirem zwiększają AUC acyklowiru o około 65%. Inne leki (w tym np. tenofowir) podawane jednocześnie, które konkurują z lub hamują aktywne wydzielanie kanalikowe, mogą zwiększać stężenie acyklowiru w wyniku tego mechanizmu. Podobnie, podawanie walacyklowiru może zwiększać stężenia innych jednocześnie podawanych substancji w osoczu.
U pacjentów narażonych na większe dawki acyklowiru z walacyklowiru (np. w dawkach stosowanych w leczeniu półpaśca lub w profilaktyce CMV) należy zachować ostrożność podczas jednoczesnego podawania z lekami hamującymi czynne wydzielanie kanalików nerkowych.
Podczas jednoczesnego podawania tych produktów leczniczych obserwowano zwiększenie wartości AUC acyklowiru i nieaktywnego metabolitu mykofenolanu mofetylu, leku immunosupresyjnego stosowanego u pacjentów po przeszczepie. Podczas jednoczesnego podawania walacyklowiru i mykofenolanu mofetylu zdrowym ochotnikom nie zaobserwowano zmian w stężeniach maksymalnych ani AUC.Doświadczenie kliniczne dotyczące stosowania tego połączenia jest ograniczone.
04.6 Ciąża i laktacja
Ciąża
Istnieją ograniczone dane dotyczące stosowania walacyklowiru i umiarkowane dane dotyczące stosowania acyklowiru w ciąży pochodzące z rejestrów stosowania w ciąży (w których udokumentowano przebieg ciąży u kobiet narażonych na walacyklowir lub acyklowir drogą doustną lub doustną. dożylnie – aktywny metabolit walacyklowir); 111 i 1246 punktów końcowych (odpowiednio 29 i 756 narażonych w pierwszym trymestrze ciąży) oraz „doświadczenia po wprowadzeniu do obrotu” nie wykazały żadnych wad rozwojowych lub działania toksycznego na płód/noworodka. zwierzęta nie wykazują szkodliwego działania walacyklowiru na reprodukcję (patrz punkt 5.3). . Walacyklowir należy stosować w ciąży tylko wtedy, gdy potencjalne korzyści z leczenia przewyższają potencjalne ryzyko.
Czas karmienia
Acyklowir, główny metabolit walacyklowiru, przenika do mleka matki. Jednakże nie oczekuje się wpływu walacyklowiru w dawkach terapeutycznych na noworodki/niemowlęta karmione piersią, ponieważ dawka przyjmowana przez niemowlę jest mniejsza niż 2% dawki terapeutycznej podawanego dożylnie acyklowiru w leczeniu opryszczki noworodków (patrz punkt 5.2). z ostrożnością podczas karmienia piersią i tylko wtedy, gdy jest to wskazane klinicznie.
Płodność
Walacyklowir nie ma wpływu na płodność szczurów leczonych doustnie. Zanik jąder i aspermatogenezę obserwowano u szczurów i psów po podaniu dużych dawek acyklowiru podawanego pozajelitowo. Nie przeprowadzono badań płodności u ludzi z użyciem walacyklowiru, ale nie zgłoszono zmian w liczbie, ruchliwości i morfologii plemników u 20 pacjentów po 6 miesiącach codziennego leczenia acyklowirem w dawce od 400 mg do 1000 mg.
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Nie przeprowadzono badań dotyczących zdolności prowadzenia pojazdów i obsługiwania maszyn.
Przy rozważaniu zdolności pacjenta do prowadzenia pojazdów i obsługiwania maszyn należy wziąć pod uwagę stan kliniczny pacjenta i profil działań niepożądanych preparatu Valtrex. Dalszego szkodliwego wpływu na te czynności nie można przewidzieć na podstawie farmakologii składnika aktywnego.
04.8 Działania niepożądane
Najczęstszymi działaniami niepożądanymi zgłaszanymi w co najmniej jednym wskazaniu przez pacjentów leczonych preparatem Valtrex w badaniach klinicznych były bóle głowy i nudności. Bardziej szczegółowo opisano poważniejsze działania niepożądane, takie jak zakrzepowa plamica małopłytkowa / zespół hemolityczno-mocznicowy, ostra niewydolność nerek i zaburzenia neurologiczne. w innych punktach Charakterystyki Produktu Leczniczego.
Działania niepożądane są wymienione poniżej według narządu i częstości występowania. Do klasyfikacji niepożądanych efektów stosuje się następujące kategorie częstotliwości:
W celu przypisania kategorii częstości do działań niepożądanych wykorzystano dane z badań klinicznych, jeśli w badaniach istniały dowody na związek z walacyklowirem.
W przypadku działań niepożądanych zidentyfikowanych po wprowadzeniu produktu do obrotu, ale nie zaobserwowanych w badaniach klinicznych, do przypisania kategorii częstości występowania działań niepożądanych zastosowano bardziej konserwatywną wartość punktu szacunkowego („zasada trzech”). W przypadku działań niepożądanych zidentyfikowanych jako związane z walacyklowirem na podstawie doświadczeń po wprowadzeniu do obrotu i obserwowanych w badaniach klinicznych, częstość występowania zgłaszana w badaniu została wykorzystana do przypisania kategorii częstości występowania działań niepożądanych. badania obejmujące wiele wskazań (leczenie półpaśca, leczenie/hamowanie opryszczki narządów płciowych oraz leczenie opryszczki wargowej).
Dane z badań klinicznych
Zaburzenia układu nerwowego
Bardzo często: ból głowy
Zaburzenia żołądkowo-jelitowe
Często: nudności
Opublikuj dane marketingowe
Zaburzenia układu krwionośnego i limfatycznego
Niezbyt często: leukopenia, trombocytopenia
Leukopenia jest zgłaszana w większości przypadków u pacjentów z obniżoną odpornością.
Zaburzenia układu odpornościowego
Rzadko: anafilaksja
Zaburzenia psychiczne i patologie układu nerwowego
Często: zawroty głowy
Niezbyt często: stan splątania, omamy, depresyjny stan świadomości, drżenie,
podniecenie
Rzadko: ataksja, dyzartria, drgawki, encefalopatia, śpiączka, objawy psychotyczne, majaczenie.
Zaburzenia neurologiczne, czasami ciężkie, mogą być związane z encefalopatią i obejmują splątanie, pobudzenie, drgawki, omamy, śpiączkę.Zdarzenia te są zwykle odwracalne i są na ogół obserwowane u pacjentów z niewydolnością nerek lub innymi czynnikami predysponującymi (patrz punkt 4.4).U pacjentów po przeszczepieniu narządu otrzymujących duże dawki preparatu Valtrex (8000 mg na dobę) w profilaktyce CMV, reakcje neurologiczne występowały częściej w porównaniu z mniejszymi dawkami stosowanymi w innych wskazaniach.
Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia
Niezbyt często: duszność
Zaburzenia żołądkowo-jelitowe
Często: wymioty, biegunka
Niezbyt często: dyskomfort w jamie brzusznej
Zaburzenia wątroby i dróg żółciowych
Niezbyt często: odwracalne zmiany w testach czynności wątroby (np. stężenia bilirubiny, enzymów
choroba wątroby)
Zaburzenia skóry i tkanki podskórnej
Często: wysypka skórna, w tym nadwrażliwość na światło, świąd
Niezbyt często: pokrzywka
Rzadko: obrzęk naczynioruchowy
Zaburzenia nerek i dróg moczowych
Niezbyt często: ból nerek, krwiomocz (często związany z innymi zdarzeniami dotyczącymi nerek)
Rzadko: zaburzenia czynności nerek, ostra niewydolność nerek (szczególnie
u pacjentów w podeszłym wieku lub u pacjentów z niewydolnością nerek otrzymujących dawki większe niż zalecane).
Ból nerek może być związany z niewydolnością nerek.
Odnotowano również wewnątrzkanalikowe wytrącanie kryształów acyklowiru w nerkach. Podczas leczenia należy zapewnić odpowiednią podaż płynów (patrz punkt 4.4).
Dowiedz się więcej o specjalnych populacjach pacjentów
U dorosłych pacjentów z ciężkim upośledzeniem odporności, zwłaszcza z zaawansowaną chorobą HIV, otrzymujących duże dawki (8000 mg na dobę) walacyklowiru przez dłuższy czas w badaniach klinicznych, zgłaszano przypadki niewydolności nerek, mikroangiopatycznej niedokrwistości hemolitycznej i trombocytopenii (czasami związanej). Obserwacje te obserwowano również u pacjentów nieleczonych walacyklowirem z tymi samymi chorobami podstawowymi lub współistniejącymi.
04.9 Przedawkowanie
Objawy i oznaki
U pacjentów, którzy otrzymali przedawkowanie walacyklowiru, zgłaszano ostrą niewydolność nerek i objawy neurologiczne, w tym splątanie, omamy, pobudzenie, zmniejszoną świadomość i śpiączkę. Zgłaszano również nudności i wymioty. Należy zachować ostrożność, aby zapobiec przypadkowemu przedawkowaniu. Wiele z tych zgłoszonych przypadków dotyczyło pacjentów w podeszłym wieku i pacjentów z zaburzeniami czynności nerek, którym wielokrotnie przedawkowano z powodu braku odpowiedniego zmniejszenia dawki.
Leczenie
Pacjenci powinni być uważnie obserwowani pod kątem objawów toksyczności. Hemodializa znacząco przyczynia się do usunięcia acyklowiru z krwi i dlatego może być rozważona jako opcja w przypadku objawowego przedawkowania.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE
05.1 Właściwości farmakodynamiczne
Grupa farmakoterapeutyczna: Nukleozydy i nukleotydy z wyłączeniem inhibitorów odwrotnej transkryptazy. Kod ATC: J05AB 11.
Mechanizm akcji
Walacyklowir, środek przeciwwirusowy, jest estrem acyklowiru z L-waliną. Acyklowir jest analogiem nukleozydowym puryn (guaniny).
U ludzi walacyklowir jest szybko i prawie całkowicie przekształcany w acyklowir i walinę, prawdopodobnie przez enzym znany jako hydrolaza walacyklowiru.
Acyklowir jest specyficznym inhibitorem wirusów opryszczki o działaniu, in vitroprzeciwko wirusom opryszczki pospolitej (HSV) typu 1 i 2, wirusowi Varicella zoster (VZV), wirusowi cytomegalii (CMV), wirusowi Epsteina-Barra (EBV) i ludzkiemu wirusowi opryszczki klasy 6 (HHV-6)). Acyklowir, po ufosforylowaniu w swojej aktywnej formie trifosforanowej, hamuje syntezę DNA wirusów opryszczki.
Pierwszy etap fosforylacji wymaga działania specyficznego enzymu wirusowego, którym w przypadku wirusów HSV, VZV i EBV jest wirusowa kinaza tymidynowa (TK), która występuje tylko w komórkach zakażonych wirusem. selektywność jest utrzymywana przez przynajmniej częściowo pośredniczoną fosforylację genu fosfotransferazy UL 97. Potrzeba aktywacji acyklowiru przez specyficzny enzym wirusowy w dużej mierze wyjaśnia jego selektywność działania.
Proces fosforylacji (od monofosforanu acyklowiru do trifosforanu) dopełniają kinazy komórkowe. Trifosforan acyklowiru kompetycyjnie hamuje wirusową polimerazę DNA, a włączenie tego analogu nukleozydu do wirusowego DNA powoduje przerwanie procesu wydłużania łańcucha tego ostatniego, aw konsekwencji zablokowanie syntezy DNA i replikacji wirusa.
Efekty farmakodynamiczne
Oporność na acyklowir jest zwykle spowodowana fenotypowym niedoborem kinazy tymidynowej, co skutkuje wirusem, który jest w niekorzystnej sytuacji u naturalnego gospodarza. Zmniejszoną wrażliwość na acyklowir opisano jako wynik minimalnych zmian w wirusowej kinazie tymidynowej lub wirusowej polimerazie DNA.Zjadliwość tych wariantów fenotypów jest podobna do dzikiego wirusa.
Monitorowanie klinicznych izolatów HSV i VZV pacjentów poddawanych leczeniu lub profilaktyce acyklowirem wykazało, że zmniejszenie wrażliwości wirusa na acyklowir jest niezwykle rzadkie u gospodarzy immunokompetentnych i jest obserwowane tylko rzadko u pacjentów z ciężkim upośledzeniem odporności, takich jak na przykład pacjenci poddawani przeszczepionych narządów lub szpiku kostnego, pacjentów poddawanych chemioterapii z powodu nowotworów złośliwych oraz pacjentów zakażonych ludzkim wirusem niedoboru odporności (HIV).
Studia kliniczne
Zakażenie wirusem Varicella Zoster
Valtrex przyspiesza ustępowanie bólu: zmniejsza czas trwania bólu związanego z półpaścem i zmniejsza liczbę pacjentów z bólem związanym z półpaścem, w tym ostrą neuralgią i, u pacjentów powyżej 50. roku życia, neuralgią poopryszczkową. Valtrex zmniejsza ryzyko powikłań ocznych półpaśca ocznego.
Terapia dożylna jest ogólnie uważana za standard leczenia półpaśca u pacjentów z obniżoną odpornością. Jednak ograniczone dane wskazują na kliniczną korzyść ze stosowania walacyklowiru w leczeniu zakażenia VZV (półpasiec) u niektórych pacjentów z obniżoną odpornością, w tym z rakiem narządu litego, HIV, chorobami autoimmunologicznymi, chłoniakiem, białaczką i przeszczepami komórek macierzystych.
Zakażenie wirusem opryszczki pospolitej
Walacyklowir w zakażeniach oczu wywołanych wirusem HSV należy podawać zgodnie z obowiązującymi wytycznymi dotyczącymi leczenia.
W zahamowanie nawrotów objawowych walacyklowiru w dawce 1000 mg dwa razy na dobę w leczeniu nawrotów podczas epizodu opryszczki było porównywalne z podawaniem 200 mg acyklowiru podawanego doustnie pięć razy na dobę. Nie badano go u pacjentów z ciężkim niedoborem odporności.
Udokumentowano skuteczność walacyklowiru w leczeniu innych zakażeń skóry wywołanych wirusem HSV.Wykazano skuteczność walacyklowiru w leczeniu opryszczki wargowej, zapalenia błon śluzowych spowodowanego chemioterapią lub radioterapią, reaktywacji wirusa HSV w wyniku zmiany powierzchni twarzy, opryszczki gladiatorskiej. Na podstawie historycznych doświadczeń dotyczących acyklowiru wydaje się, że walacyklowir jest tak samo skuteczny jak acyklowir w leczeniu rumienia wielopostaciowego, wyprysku opryszczkowego i zanokcicy opryszczkowej.
Wykazano, że walacyklowir zmniejsza ryzyko przeniesienia opryszczki narządów płciowych u osób dorosłych z prawidłową odpornością, gdy jest przyjmowany jako terapia supresyjna i w połączeniu z zabezpieczonym stosunkiem płciowym.Badanie z podwójnie ślepą próbą, kontrolowane placebo, przeprowadzono na 1484 dorosłych parach z prawidłową odpornością, heteroseksualnych i niezgodnych. lub nie występuje zakażenie HSV-2. Wyniki wykazały istotne zmniejszenie ryzyka przeniesienia: 75% (objawowe nabycie HSV-2), 50% (serokonwersja HSV-2) i 48% (całkowite nabycie HSV-2) dla walacyklowiru w porównaniu z placebo. Wśród pacjentów biorących udział w podbadaniu wydalania wirusa, walacyklowir znacznie zmniejszył wydalanie wirusa o 73% w porównaniu z placebo (więcej informacji na temat zmniejszenia przenoszenia wirusa, patrz punkt 4.4).
Zakażenie wirusem cytomegalii (patrz punkt 4.4)
Profilaktyka CMV z użyciem walacyklowiru u pacjentów po przeszczepieniu narządu litego (nerki, serca) zmniejsza występowanie ostrego odrzucania przeszczepu, zakażeń oportunistycznych i innych zakażeń opryszczkowych (HSV, VZV).Nie ma bezpośredniego badania porównawczego z walgancyklowirem w celu określenia optymalnego leczenia postępowanie u pacjentów po przeszczepieniu narządu litego.
05.2 „Właściwości farmakokinetyczne
Wchłanianie
Walacyklowir jest prolekiem acyklowiru. Biodostępność acyklowiru z walacyklowiru jest około 3,3-5,5 razy większa niż obserwowana w przeszłości dla acyklowiru podawanego doustnie. Po podaniu doustnym walacyklowir jest dobrze i szybko wchłaniany i prawie całkowicie przekształcany w acyklowir i walinę. W tej konwersji prawdopodobnie pośredniczy enzym wyizolowany z ludzkiej wątroby, znany jako hydrolaza walacyklowiru. Biodostępność acyklowiru z dawki 1000 mg walacyklowiru wynosi 54% i nie jest zmniejszana przez pokarm Farmakokinetyka walacyklowiru nie jest proporcjonalna do dawki Szybkość i stopień wchłaniania zmniejsza się wraz ze wzrostem dawki, co powoduje mniej niż proporcjonalny wzrost Cmax poza zakresem dawek terapeutycznych i zmniejszoną biodostępność po dawkach powyżej 500 mg. Poniżej przedstawiono przewidywania parametrów farmakokinetycznych (PK) acyklowiru po podaniu pojedynczej dawki 250-2000 mg walacyklowiru u zdrowych ochotników z prawidłową czynnością nerek.
Cmax = stężenie szczytowe; Tmax = czas do maksymalnego stężenia; AUC = powierzchnia pod krzywą czas-stężenie. Wartości Cmax i AUC wskazują średnią ± odchylenie standardowe. Wartości Tmax wskazują medianę i interwał.
Maksymalne stężenie niezmienionego walacyklowiru w osoczu wynosi tylko 4% maksymalnych stężeń acyklowiru, jest osiągane po upływie mediany 30-100 minut po podaniu dawki i jest równe lub poniżej granicy oznaczalności po 3 godzinach od podania dawki.Profile farmakokinetyczne walacyklowiru i acyklowiru są podobnie po dawkach pojedynczych i wielokrotnych. Półpasiec i zakażenie wirusem opryszczki HIV nie zmieniają znacząco farmakokinetyki walacyklowiru i acyklowiru po doustnym podaniu walacyklowiru w porównaniu ze zdrowymi dorosłymi. te obecne u zdrowych ochotników otrzymujących tę samą dawkę. Przypuszczalne dzienne AUC są znacznie wyższe.
Dystrybucja
Wiązanie walacyklowiru z białkami osocza jest bardzo niskie (15%).
Penetracja płynu mózgowo-rdzeniowego (CSF) określona przez stosunek CSF/AUC w osoczu jest niezależna od czynności nerek i wynosiła około 25% dla acyklowiru i metabolitu 8-OH-ACV oraz około 2,5% dla metabolitu CMMG.
Biotransformacja
Po podaniu doustnym walacyklowir jest przekształcany w acyklowir e L-walina z pierwszego pasażu jelitowego i/lub z metabolizmu wątrobowego. Acyklowir jest przekształcany w niewielką ilość metabolitów w:
9 (karboksymetoksy)metyloguanina (CMMG) z alkoholu i dehydrogenazy aldehydowej, w 8-hydroksy-acyklowir (8-OH-ACV) z oksydazy aldehydowej. Około 88% łącznej całkowitej ekspozycji w osoczu jest przypisywane acyklowirowi, 11% CMMG i 1% do 8-OH-ACV Ani walacyklowir, ani acyklowir nie są metabolizowane przez cytochrom P450.
Eliminacja
Walacyklowir jest wydalany głównie z moczem jako acyklowir (ponad 80% odzyskanej dawki) oraz jako metabolit acyklowiru CMMG (około 14% odzyskanej dawki). Metabolit 8-OH-ACV jest wykrywalny w moczu tylko w niewielkich ilościach (okres półtrwania acyklowiru w fazie eliminacji z osocza po podaniu pojedynczej i wielokrotnej dawki walacyklowiru wynosi około 3 godziny.
Populacje specjalne
Niewydolność nerek
Eliminacja acyklowiru jest związana z czynnością nerek i ekspozycja na acyklowir wzrośnie
wraz ze wzrostem niewydolności nerek. U pacjentów ze schyłkową niewydolnością nerek średni okres półtrwania acyklowiru w fazie eliminacji po podaniu walacyklowiru wynosi około 14 godzin, w porównaniu z około 3 godzinami w przypadku prawidłowej czynności nerek (patrz punkt 4.2).
Narażenie na acyklowir i jego metabolity CMMG i 8-OH-ACV w osoczu i płynie mózgowo-rdzeniowym (CSF) oceniano po stan stabilny po wielokrotnym podaniu walacyklowiru u 6 osób z prawidłową czynnością nerek (średni klirens kreatyniny 111 ml/min, zakres 91-144 ml/min) leczonych dawką 2000 mg co 6 godzin oraz u 3 osób z ciężkimi zaburzeniami czynności nerek (średni klirens kreatyniny 26 ml/min, zakres 17-31 ml/min) leczony 1500 mg co 12 godzin. W osoczu, jak również w płynie mózgowo-rdzeniowym, stężenia acyklowiru i metabolitów CMMG i 8-OH-ACV były średnio odpowiednio 2, 4 i 5-6 razy wyższe w ciężkiej niewydolności nerek niż w prawidłowej czynności nerek.
Niewydolność wątroby
Dane farmakokinetyczne wskazują, że niewydolność wątroby zmniejsza szybkość przemiany walacyklowiru w acyklowir, ale nie całkowitą przemianę.Nie ma wpływu na okres półtrwania acyklowiru.
Kobiety w ciąży
Badanie farmakokinetyczne walacyklowiru i acyklowiru przeprowadzone w późnej ciąży wskazuje, że ciąża nie ma wpływu na farmakokinetykę walacyklowiru.
Przenieść do mleka matki
Po podaniu doustnym dawki 500 mg walacyklowiru maksymalne stężenie acyklowiru Cmax osiągane w mleku matki było od 0,5 do 2,3 razy większe niż odpowiednie stężenie acyklowiru w surowicy matki. Średnie stężenie acyklowiru w mleku matki wynosiło 2,24 mcg/ml (9,95 mikromol/l). Przy dawkowaniu matczynym 500 mg walacyklowiru dwa razy na dobę, taki poziom może narazić niemowlę karmione piersią na dzienną dawkę doustną acyklowiru wynoszącą około 0,6 1 mg/kg/dobę. Okres półtrwania acyklowiru w fazie eliminacji z mleka kobiecego był podobny do okresu półtrwania w surowicy.Nie wykryto niezmienionego walacyklowiru w surowicy matki, mleku matki lub moczu niemowląt.
05.3 Przedkliniczne dane o bezpieczeństwie
Dane niekliniczne, oparte na konwencjonalnych badaniach bezpieczeństwo farmakologia, toksyczność po podaniu wielokrotnym, genotoksyczność i potencjał rakotwórczy.
Walacyklowir nie ma wpływu na płodność samców i samic szczurów leczonych doustnie.
Walacyklowir nie wykazywał działania teratogennego u szczurów ani królików. Walacyklowir jest prawie całkowicie metabolizowany do acyklowiru. Podskórne podawanie acyklowiru w testach międzynarodowych nie powodowało działania teratogennego u szczurów i królików. W dalszych badaniach na szczurach obserwowano nieprawidłowości płodu i toksyczność dla matki po podaniu podskórnych dawek, które powodowały stężenie acyklowiru w osoczu 100 μg/ml (ponad 10-krotnie wyższe niż po podaniu pojedynczej dawki 2000 mg walacyklowiru u ludzi z prawidłową czynnością nerek).
06.0 INFORMACJE FARMACEUTYCZNE
06.1 Zaróbki
Rdzeń tabletu
Celuloza mikrokrystaliczna
Krospowidon
Powidon
Stearynian magnezu
Koloidalny dwutlenek krzemu
Powłoka
Hypromeloza
Dwutlenek tytanu
Makrogol
Polisorbat 80 (tylko dla tabletek 500 mg i 1000 mg)
Wosk Carnauba
06.2 Niezgodność
Nieistotne.
06.3 Okres ważności
Tabletki 250 mg, tabletki 1000 mg
Dwa lata
Tabletki 500 mg
Trzy lata
06.4 Specjalne środki ostrożności przy przechowywaniu
Przechowywać w temperaturze poniżej 30°C
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania
Blistry z polichlorku winylu/aluminium.
250 mg tabletki
Opakowanie 20 lub 60 tabletek
Tabletki 500 mg
Opakowania po 10, 24, 30, 42, 90 lub 112 tabletek
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
Tabletki 1000 mg
Opakowanie 21 tabletek
06.6 Instrukcje użytkowania i obsługi
Brak specjalnych instrukcji.
07.0 PODMIOT POZWOLENIA NA DOPUSZCZENIE DO OBROTU
GlaxoSmithKline S.p.A. - Via A. Fleming 2 - Werona.
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
ZELITREX 250 mg tabletki powlekane - 60 tabletek A.I.C.: 029503048
ZELITREX 500 mg tabletki powlekane - 42 tabletki A.I.C.: 029503012
ZELITREX 500 mg tabletki powlekane - 10 tabletek A.I.C.: 029503036
ZELITREX 1000 mg tabletki powlekane - 21 tabletek A.I.C.: 029503024
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA
42 tabletki po 500 mg - 21 tabletek po 1000 mg: 19 stycznia 1998 / listopad 2002
60 tabletek po 250 mg -10 tabletek po 500 mg: 9 maja 2002 / listopad 2002
10.0 DATA ZMIAN TEKSTU
23 września 2011



















-e-ruscogenina.jpg)